Развитие нервной системы у человека, или нейронное развитие, или нейроразвитие включает в себя исследования эмбриологии , биологии развития и нейронауки . Они описывают клеточные и молекулярные механизмы, посредством которых сложная нервная система формируется у человека, развивается во время пренатального развития и продолжает развиваться постнатально.
Некоторые основные этапы развития нервной системы у эмбриона включают в себя:
Как правило, эти процессы нейроразвития можно условно разделить на два класса:
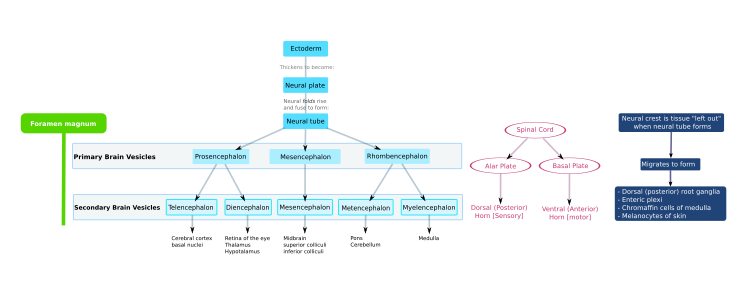
Центральная нервная система (ЦНС) происходит из эктодермы — самого внешнего слоя ткани эмбриона. На третьей неделе эмбрионального развития человека появляется нейроэктодерма и образует нервную пластинку вдоль дорсальной стороны эмбриона. Нервная пластинка является источником большинства нейронов и глиальных клеток ЦНС. Вдоль длинной оси нервной пластинки образуется бороздка, и к четвертой неделе развития нервная пластинка заворачивается сама в себя, давая начало нервной трубке , которая заполнена спинномозговой жидкостью (СМЖ). [1] По мере развития эмбриона передняя часть нервной трубки образует три первичных мозговых пузыря , которые становятся первичными анатомическими областями мозга: передний мозг ( prosencephalon ), средний мозг ( mesencephalon ) и задний мозг ( rhombencephalon ). [2] Эти простые ранние пузырьки увеличиваются и далее делятся на пять вторичных мозговых пузырьков — конечный мозг (будущая кора головного мозга и базальные ганглии ), промежуточный мозг (будущие таламус и гипоталамус ), средний мозг (будущие холмики ), задний мозг (будущие мост и мозжечок ) и продолговатый мозг (будущий продолговатый мозг ). [3] Центральная камера, заполненная цереброспинальной жидкостью, непрерывна от конечного мозга до спинного мозга и представляет собой развивающуюся желудочковую систему ЦНС. Поскольку нервная трубка дает начало головному и спинному мозгу, любые мутации на этой стадии развития могут привести к фатальным деформациям, таким как анэнцефалия , или к пожизненным нарушениям, таким как spina bifida . В это время стенки нервной трубки содержат нервные стволовые клетки , которые стимулируют рост мозга, поскольку они делятся много раз. Постепенно некоторые клетки перестают делиться и дифференцируются в нейроны и глиальные клетки , которые являются основными клеточными компонентами ЦНС. [2] Вновь образованные нейроны мигрируют в различные части развивающегося мозга, чтобы самоорганизоваться в различные структуры мозга. Как только нейроны достигают своих региональных положений, они удлиняют аксоныи дендриты , которые позволяют им общаться с другими нейронами через синапсы . Синаптическая связь между нейронами приводит к установлению функциональных нейронных цепей , которые опосредуют сенсорную и моторную обработку и лежат в основе поведения. [4]
В ходе раннего эмбрионального развития эктодерма становится специализированной для образования эпидермиса (кожи) и нервной пластинки. Превращение недифференцированной эктодермы в нейроэктодерму требует сигналов от мезодермы . В начале гаструляции предполагаемые мезодермальные клетки перемещаются через дорсальную губу бластопора и образуют слой между энтодермой и эктодермой. Эти мезодермальные клетки, которые мигрируют вдоль дорсальной средней линии, дают начало структуре, называемой хордой . Эктодермальные клетки, покрывающие хорду, развиваются в нервную пластинку в ответ на диффузный сигнал, производимый хордой. Оставшаяся часть эктодермы дает начало эпидермису (коже). Способность мезодермы преобразовывать вышележащую эктодерму в нервную ткань называется нервной индукцией.
Нервная пластинка сгибается наружу в течение третьей недели беременности, образуя нервную бороздку . Начиная с будущей шейной области, нервные складки этой бороздки смыкаются, образуя нервную трубку . Формирование нервной трубки из эктодермы называется нейруляцией . Вентральная часть нервной трубки называется базальной пластинкой ; дорсальная часть называется крыловидной пластинкой . Полая внутренняя часть называется нервным каналом . К концу четвертой недели беременности открытые концы нервной трубки, называемые нейропорами, закрываются. [5]
Трансплантированная губа бластопора может преобразовать эктодерму в нервную ткань и, как говорят, имеет индуктивный эффект. Нейральные индукторы — это молекулы, которые могут индуцировать экспрессию нейральных генов в эксплантатах эктодермы, не индуцируя также мезодермальные гены. Нейральная индукция часто изучается на эмбрионах ксенопуса , поскольку у них простая структура тела и существуют хорошие маркеры для различения нервной и не нервной ткани. Примерами нейральных индукторов являются молекулы ноггин и хордин .
Когда эмбриональные эктодермальные клетки культивируются при низкой плотности в отсутствие мезодермальных клеток, они подвергаются нейральной дифференциации (экспрессируют нейральные гены), что позволяет предположить, что нейральная дифференциация является судьбой эктодермальных клеток по умолчанию. В культурах эксплантатов (которые допускают прямое взаимодействие клеток) те же клетки дифференцируются в эпидермис. Это происходит из-за действия BMP4 ( белка семейства TGF-β ), который побуждает эктодермальные культуры дифференцироваться в эпидермис. Во время нейральной индукции ноггин и хордин вырабатываются дорсальной мезодермой (хордой) и диффундируют в вышележащую эктодерму, чтобы ингибировать активность BMP4. Это ингибирование BMP4 заставляет клетки дифференцироваться в нейральные клетки. Ингибирование сигнализации TGF-β и BMP (костный морфогенетический белок) может эффективно индуцировать нервную ткань из человеческих плюрипотентных стволовых клеток [6] , модели раннего развития человека.
В конце четвертой недели верхняя часть нервной трубки изгибается на уровне будущего среднего мозга — мезэнцефалона . Над мезэнцефалоном находится прозэнцефалон (будущий передний мозг), а под ним — ромбовидный мозг (будущий задний мозг). Зрительный пузырек (который в конечном итоге станет зрительным нервом, сетчаткой и радужной оболочкой) формируется на базальной пластинке прозэнцефалона.
Спинной мозг формируется из нижней части нервной трубки. Стенка нервной трубки состоит из нейроэпителиальных клеток, которые дифференцируются в нейробласты, образуя мантийный слой (серое вещество). Нервные волокна выходят из этих нейробластов, образуя краевой слой (белое вещество). Вентральная часть мантийного слоя (базальные пластинки) формирует двигательные области спинного мозга, в то время как дорсальная часть (крыльчатые пластинки) формирует сенсорные области. Между базальными и крыловидными пластинками находится промежуточный слой, содержащий нейроны автономной нервной системы. [7]
На пятой неделе крыловидная пластинка переднего мозга расширяется, образуя полушария головного мозга ( теленцефалон ). Базальная пластинка становится промежуточным мозгом .
Промежуточный мозг, средний мозг и ромбовидный мозг составляют мозговой ствол эмбриона. Он продолжает изгибаться в среднем мозге. Ромбовидный мозг сгибается назад, что заставляет его крыловидную пластинку расширяться и образовывать четвертый желудочек мозга. В верхней части ромбовидного мозга формируются мост и мозжечок , а в нижней — продолговатый мозг.
Нейровизуализация ответственна за большие достижения в понимании того, как развивается мозг. ЭЭГ и ЭРП являются эффективными процессами визуализации, используемыми в основном для младенцев и маленьких детей, поскольку они более щадящие. Младенцы обычно проходят тестирование с помощью fNIRS . МРТ и фМРТ широко используются для исследования мозга из-за качества изображений и анализа, которые они могут дать.
МРТ полезны для анализа многих аспектов мозга. Коэффициент переноса намагниченности (MTR) измеряет целостность с помощью намагничивания. Дробная анизотропия (FA) измеряет организацию с помощью диффузии молекул воды. Кроме того, средняя диффузность (MD) измеряет силу трактов белого вещества . [8]
Используя структурную МРТ, можно провести количественную оценку ряда процессов развития, включая определение моделей роста [9] и характеристику последовательности миелинизации. [10] Эти данные дополняют доказательства исследований диффузионно-тензорной визуализации (DTI), которые широко использовались для изучения развития белого вещества.
Тест фМРТ ментализация, который является теорией разума путем активации сети. Задняя верхняя височная борозда (pSTS) и височно-теменной узел (TPJ) полезны для прогнозирования движения. У взрослых правая pSTS показала большую реакцию, чем та же область у подростков при тестировании на преднамеренную причинность. Эти области также активировались во время упражнения «разум в глазах», где эмоции должны оцениваться на основе разных изображений глаз. Еще одна ключевая область — передняя височная кора (ATC) в задней области. У взрослых левая ATC показала большую реакцию, чем та же область у подростков при тестировании на эмоциональные тесты ментализации. Наконец, медиальная префронтальная кора (MPFC) и передняя дорсальная MPFC (dMPFC) активируются, когда разум стимулируется психологией. [8]
Более высокое разрешение изображений позволило трехмерному ультразвуку помочь идентифицировать развитие человеческого мозга на эмбриональных стадиях. Исследования сообщают, что три первичные структуры формируются на шестой неделе беременности . Это передний мозг , средний мозг и задний мозг , также известные как передний мозг, средний мозг и ромбовидный мозг соответственно. Пять вторичных структур из них на седьмой неделе беременности. Это конечный мозг, промежуточный мозг, средний мозг, задний мозг и продолговатый мозг, которые позже становятся боковыми желудочками, третьими желудочками, водопроводом и верхней и нижней частями четвертого желудочка от конечного мозга до продолговатого мозга во взрослом возрасте. 3D ультразвуковое изображение позволяет получать изображения идеального развития мозга in vivo, что может помочь распознать нарушения во время беременности. [11]
Исследования с использованием МРТ показали, что в то время как белое вещество увеличивается с детства (~9 лет) до подросткового возраста (~14 лет), серое вещество уменьшается. Это наблюдалось в основном в лобной и теменной коре. Теории относительно того, почему это происходит, различаются. Одна из мыслей заключается в том, что интракортикальная миелинизация в сочетании с увеличенным калибром аксонов увеличивает объем ткани белого вещества. Другая мысль заключается в том, что синаптическая реорганизация происходит из пролиферации и затем обрезки. [8]
Рост и падение объема серого вещества в лобных и теменных долях достигали пика в возрасте ~12 лет. Пик для височных долей был ~17 лет, причем верхняя височная кора созревала последней. Сенсорные и двигательные области созревали первыми, после чего развивалась остальная часть коры. Это характеризовалось потерей серого вещества и происходило от задней к передней области. Эта потеря серого вещества и увеличение белого вещества могут происходить на протяжении всей жизни, хотя более существенные изменения происходят от детства к подростковому возрасту. [8]
Миграция нейронов — это метод, с помощью которого нейроны перемещаются из места своего происхождения или рождения в свое конечное положение в мозге. Наиболее распространенными способами миграции являются радиальная и тангенциальная миграция.
Нейральные стволовые клетки размножаются в желудочковой зоне развивающегося неокортекса . Первые постмитотические клетки мигрируют из препластины, которым суждено стать клетками Кахаля-Ретциуса и нейронами субпластины . Эти клетки делают это путем сомальной транслокации. Нейроны, мигрирующие с помощью этого способа передвижения, являются биполярными и прикрепляют передний край отростка к мягкой мозговой оболочке . Затем сомовая оболочка транспортируется на поверхность мягкой мозговой оболочки с помощью нуклеокинеза, процесса, при котором микротрубочковая «клетка» вокруг ядра удлиняется и сокращается в ассоциации с центросомой , чтобы направить ядро к его конечному месту назначения. [12] Радиальные волокна (также известные как радиальная глия) могут транслоцироваться в кортикальную пластинку и дифференцироваться либо в астроциты , либо в нейроны . [13] Сомальная транслокация может происходить в любой момент развития. [14]
Последующие волны нейронов разделяют препластину, мигрируя вдоль радиальных глиальных волокон, чтобы сформировать кортикальную пластину. Каждая волна мигрирующих клеток проходит мимо своих предшественников, образуя слои изнутри наружу, что означает, что самые молодые нейроны находятся ближе всего к поверхности. [15] [16] По оценкам, глиальная направленная миграция составляет 80-90% мигрирующих нейронов. [17]
Многие нейроны, мигрирующие вдоль передне-задней оси тела, используют существующие аксонные тракты для миграции в процессе, называемом аксофильной миграцией. [18] Примером этого способа миграции являются нейроны, экспрессирующие ГнРГ , которые совершают долгое путешествие от места своего рождения в носу через передний мозг и в гипоталамус. [19] Многие механизмы этой миграции были разработаны, начиная с внеклеточных направляющих сигналов [20] , которые запускают внутриклеточную сигнализацию. Эти внутриклеточные сигналы, такие как кальциевая сигнализация , приводят к актиновой [21] и микротрубочковой [22] динамике цитоскелета, которые производят клеточные силы, которые взаимодействуют с внеклеточной средой через белки клеточной адгезии [23], вызывая движение этих клеток. Нейрофильная миграция относится к миграции нейронов вдоль аксона, принадлежащего другому нерву. Глиофильная миграция - это миграция глии вдоль глиальных волокон. [24]
Большинство интернейронов мигрируют тангенциально через несколько способов миграции, чтобы достичь своего соответствующего местоположения в коре. Примером тангенциальной миграции является перемещение клеток Кахаля-Ретциуса в пределах краевой зоны коркового нейроэпителия. [25]
Существует также метод миграции нейронов, называемый мультиполярной миграцией . [26] [27] Это наблюдается в мультиполярных клетках, которые в изобилии присутствуют в кортикальной промежуточной зоне . Они не похожи на клетки, мигрирующие путем локомоции или сомальной транслокации. Вместо этого эти мультиполярные клетки экспрессируют нейронные маркеры и расширяют множественные тонкие отростки в различных направлениях независимо от радиальных глиальных волокон. [26]
Нейротрофические факторы — это молекулы, которые способствуют и регулируют выживание нейронов в развивающейся нервной системе. Они отличаются от вездесущих метаболитов, необходимых для поддержания и роста клеток, своей специфичностью; каждый нейротрофический фактор способствует выживанию только определенных видов нейронов на определенной стадии их развития. Кроме того, утверждается, что нейротрофические факторы участвуют во многих других аспектах развития нейронов, начиная от аксонального руководства и заканчивая регуляцией синтеза нейротрансмиттеров. [28]
Нейроразвитие во взрослой нервной системе включает такие механизмы, как ремиелинизация , генерация новых нейронов , глии , аксонов , миелина или синапсов . Нейрорегенерация различается между периферической нервной системой (ПНС) и центральной нервной системой (ЦНС) по функциональным механизмам и особенно по степени и скорости.
Нервная система продолжает развиваться во взрослом возрасте до смерти мозга . [ необходимы дополнительные ссылки ] Например:
Исследования, методы лечения и политика часто различают «зрелый» мозг и «развивающийся» мозг, в то время как ученые отмечают, что «сложная природа самого нейроразвития создает проблемы для установления точки отсчета, которая указывала бы, когда мозг становится зрелым» и что различные структурные показатели мозга постоянно меняются на протяжении взрослой фазы жизни, [34] хотя уровни нейропластичности детства могут и не быть достигнуты снова [ необходима ссылка ] , и считается, что существуют различные критические и чувствительные периоды развития мозга. [35]
Обучение часто более эффективно у детей и занимает больше времени или становится более трудным с возрастом . Исследование с использованием нейровизуализации выявило быстрое усиление нейротрансмиттера ГАМК как основной потенциальный компонент объяснения того, почему это так. [36] [37]
Мозг ребенка содержит больше « тихих синапсов », которые неактивны до тех пор, пока не будут задействованы в качестве части нейропластичности и гибкого обучения или воспоминаний . [38] [39] Нейропластичность усиливается во время критических или чувствительных периодов развития мозга, в основном это касается развития мозга во время развития ребенка . [40]
То, чему люди учатся на ранних стадиях и чему они учатся применять, настраивает людей на жизненный путь или оказывает непропорциональное влияние. [41] Взрослые обычно обладают большей способностью выбирать, что они будут изучать, в какой степени и как. Например, дети могут изучать заданные предметы и темы школьной программы с помощью рукописного переписывания на доске в классе , вместо того, чтобы иметь возможность выбирать конкретные темы/навыки или работы для изучения и стили обучения. Например, дети могут не иметь развитых консолидированных интересов, этики, интереса к цели и значимым видам деятельности, знаний о требованиях и запросах реального мира и приоритетах.В раннем развитии (до рождения и в течение первых нескольких месяцев) мозг претерпевает больше изменений в размере, форме и структуре, чем в любое другое время жизни. Улучшение понимания развития мозга в этот критический период важно для картирования нормального роста и для исследования механизмов травм, связанных с факторами риска неправильного развития, такими как преждевременные роды. Следовательно, существует необходимость в плотном покрытии этого возрастного диапазона изменяющимся во времени, зависящим от возраста атласом. Такие пространственно-временные атласы могут точно отображать динамические изменения, происходящие во время раннего развития мозга, [9] и могут использоваться в качестве нормативного справочного пространства.
Кроме того, были проведены крупномасштабные исследования экспрессии генов в различных областях мозга от ранней беременности до старения. Такого рода данные дают уникальное представление об изменениях, которые происходят в мозге в течение этого длительного периода. Этот подход показал, что 86 процентов генов были экспрессированы, и что 90 процентов из них были дифференцированно отрегулированы на уровне всего транскрипта или экзона в разных областях мозга и/или во времени. Большинство этих пространственно-временных различий были обнаружены до рождения, с последующим увеличением сходства между региональными транскриптомами. Более того, межобластные различия демонстрируют временную модель песочных часов, разделяя развитие неокортекса человека на три основные фазы. Во время первой фазы, в первые шесть месяцев после зачатия, общая архитектура областей мозга в значительной степени формируется всплеском генетической активности, которая отличается для определенных областей неокортекса. За этим всплеском следует своего рода перерыв, начинающийся в третьем триместре беременности. В этот период большинство генов, которые активны в определенных областях мозга, затихают — за исключением генов, которые стимулируют связи между всеми областями неокортекса. Затем в позднем детстве и раннем подростковом возрасте генетический оркестр возобновляет работу и помогает тонко формировать области неокортекса, которые постепенно выполняют более специализированные задачи, процесс, который продолжается и во взрослой жизни. [42] [43] [44]
Подходы к исследованию органогенеза и раннего развития человеческого мозга или нервной системы включают:
Недоступность тканей человека препятствует молекулярному пониманию формирования когнитивных способностей. [45] Плацента также исследуется. [ 55] [56] [54]
Лучшее понимание развития может потенциально позволить проникнуть в суть заболеваний нервной системы, улучшить интеллект и улучшить защиту от вредного воздействия выявленных факторов развития плода (потенциально включая заболевания матери, различные события и ксенобиотики ). [53] [54] [ необходимы дополнительные ссылки ]
Благодаря неинвазивной визуализации удалось сделать новые открытия в отношении различных частей мозга.
В этой области у подростков отмечается большая активность, чем у взрослых, при выполнении тестов на ментализацию, а также коммуникативных и личных намерений. Снижение активности от подросткового возраста к взрослому. В ментализирующей задаче с использованием анимации dMPFC была более стимулирована у взрослых, в то время как вентральная MPFC была более стимулирована у детей. Их можно отнести к использованию объективной стратегии, связанной с dMPFC. Теории снижения активности от подросткового возраста к взрослому различаются. Одна теория заключается в том, что когнитивная стратегия становится более автоматической с возрастом, а другая заключается в том, что функциональные изменения происходят параллельно с нейроанатомическими изменениями, которые характеризуются синаптогенезом и обрезкой. [8]
MPFC — это пример одной конкретной области, которая стала лучше понята с использованием современных методов визуализации. Текущие исследования предоставляют гораздо больше подобных результатов.
Стресс в раннем возрасте определяется как воздействие обстоятельств в детстве, которые подавляют ресурсы совладания ребенка и приводят к длительным периодам стресса. [57] Результаты многочисленных исследований показывают, что влияние стресса в раннем возрасте на развивающийся мозг является значительным и включает, помимо прочего, следующее: увеличение объема миндалевидного тела, [58] [59] снижение активности в лобных корковых и лимбических структурах мозга, [60] и изменение структуры белого вещества. [61]
Считается, что стресс в раннем возрасте вызывает изменения в развитии мозга, вмешиваясь в нейрогенез, синаптическую продукцию и обрезку синапсов и рецепторов. [57] Вмешательство в эти процессы может привести к увеличению или уменьшению объемов областей мозга, что потенциально объясняет выводы о том, что стресс в раннем возрасте связан с увеличением объема миндалевидного тела и уменьшением объема передней поясной коры. [58] [62]
Из литературы было сделано несколько важных выводов. Области мозга, которые претерпевают значительное постнатальное развитие, такие как те, которые участвуют в памяти и эмоциях, более уязвимы к воздействию стресса в раннем возрасте. [57] [63] Например, гиппокамп продолжает развиваться после рождения и является структурой, на которую влияет жестокое обращение в детстве. [63] Стресс в раннем возрасте, по-видимому, мешает перепроизводству синапсов, что типично для детства, но не мешает синаптической обрезке в подростковом возрасте. Это приводит к меньшим объемам гиппокампа, что потенциально объясняет связь между стрессом в раннем возрасте и уменьшенным объемом гиппокампа. [62] Это уменьшение объема может быть связано с дефицитом регуляции эмоций, наблюдаемым у тех, кто подвергся стрессу в раннем возрасте.
Миндалевидное тело особенно уязвимо к стрессу в раннем возрасте. [57] Миндалевидное тело также претерпевает значительное развитие в детстве, структурно и функционально изменяется у людей, которые испытали стресс в раннем возрасте, и связано с социально-эмоциональными трудностями, связанными со стрессом в раннем возрасте.
Тип рецептора — еще один фактор, который следует учитывать при определении того, чувствительна ли область мозга к воздействию стресса в раннем возрасте. Области мозга с высокой плотностью глюкокортикоидных рецепторов особенно уязвимы к воздействию стресса в раннем возрасте, вероятно, потому, что глюкокортикоиды связываются с этими рецепторами во время воздействия стресса, способствуя развитию реакций выживания за счет других важных нервных путей. [63] Некоторые примеры областей мозга с высокой плотностью глюкокортикоидных рецепторов — гиппокамп и червь мозжечка. Стресс активирует ось HPA и приводит к выработке глюкокортикоидов. Повышенная выработка глюкокортикоидов приводит к повышенной активации этих областей мозга, способствуя развитию определенных нервных путей за счет других.
Аномалии в структуре и функционировании мозга часто связаны с дефицитами, которые могут сохраняться в течение многих лет после снятия стресса и могут быть фактором риска для будущей психопатологии. [57] Наиболее чувствительными к стрессу в раннем возрасте являются области мозга, которые подвергаются изменениям в развитии во время воздействия стресса. В результате стресс изменяет траекторию развития этой области мозга, вызывая долгосрочные изменения в структуре и функционировании.
Распространенные типы стресса в раннем возрасте, которые были задокументированы, включают в себя плохое обращение, пренебрежение и предыдущее пребывание в учреждении. Было также показано, что жизнь в бедности также влияет на функцию мозга. [64]