Рак поджелудочной железы возникает, когда клетки поджелудочной железы , железистого органа, расположенного за желудком , начинают бесконтрольно размножаться и образовывать массу . Эти раковые клетки способны проникать в другие части тела. [9] Известно несколько типов рака поджелудочной железы. [10]
Наиболее распространенная аденокарцинома поджелудочной железы составляет около 90% случаев [11] , и термин «рак поджелудочной железы» иногда используется для обозначения только этого типа. [10] Эти аденокарциномы возникают в той части поджелудочной железы, которая вырабатывает пищеварительные ферменты . [10] Некоторые другие типы рака, которые в совокупности представляют собой большинство неаденокарцином, также могут возникать из этих клеток. [10]
Около 1–2% случаев рака поджелудочной железы составляют нейроэндокринные опухоли , возникающие из гормонпродуцирующих клеток поджелудочной железы. [10] Они, как правило, менее агрессивны, чем аденокарцинома поджелудочной железы. [10]
Признаки и симптомы наиболее распространенной формы рака поджелудочной железы могут включать пожелтение кожи , боли в животе или спине , необъяснимую потерю веса , светлый стул , темную мочу и потерю аппетита . [1] Обычно на ранних стадиях заболевания симптомы не наблюдаются, а симптомы, которые достаточно специфичны , чтобы предположить рак поджелудочной железы, обычно не развиваются до тех пор, пока заболевание не достигнет поздней стадии. [1] [2] К моменту постановки диагноза рак поджелудочной железы часто распространяется на другие части тела. [10] [12]
Рак поджелудочной железы редко возникает в возрасте до 40 лет, и более половины случаев аденокарциномы поджелудочной железы встречается у людей старше 70 лет . [2] Факторы риска рака поджелудочной железы включают курение табака , ожирение , диабет и некоторые редкие генетические заболевания. [2] Около 25% случаев связаны с курением, [3] и 5–10% связаны с наследственными генами . [2]
Рак поджелудочной железы обычно диагностируется с помощью комбинации методов медицинской визуализации, таких как ультразвук или компьютерная томография , анализы крови и исследование образцов тканей ( биопсия ). [3] [4] Заболевание разделяют на стадии : от ранней (I стадия) до поздней (IV стадия). [12] Скрининг населения в целом не оказался эффективным. [13]
Риск развития рака поджелудочной железы ниже среди некурящих и людей, которые поддерживают здоровый вес и ограничивают потребление красного или обработанного мяса ; [5] однако риск выше для мужчин, особенно при очень высоком уровне потребления красного мяса. [14] Однако этот вопрос является предметом дискуссий, поскольку исследование, проведенное Международным журналом рака в 2013 году, не обнаружило какой-либо статистически значимой связи между потреблением красного мяса и раком поджелудочной железы, вместо этого не было обнаружено никакой мужской связи, а обнаружена только положительная связь с красным мясом. потребление с риском рака поджелудочной железы у женщин после ограничения микроскопически подтвержденными случаями. [15] Шансы курильщиков на развитие заболевания уменьшаются, если они бросают курить, и почти возвращаются к уровню остального населения через 20 лет. [10] Рак поджелудочной железы можно лечить хирургическим путем, лучевой терапией , химиотерапией , паллиативной помощью или их комбинацией. [1] Варианты лечения частично зависят от стадии рака. [1] Хирургическое вмешательство является единственным методом лечения, который может вылечить аденокарциному поджелудочной железы, [12] и может также применяться для улучшения качества жизни без возможности излечения. [1] [12] Иногда необходимы обезболивающие и лекарства для улучшения пищеварения. [12] Ранняя паллиативная помощь рекомендуется даже тем, кто получает лечение, направленное на излечение. [16]
Рак поджелудочной железы является одной из самых смертоносных форм рака в мире и имеет один из самых низких показателей выживаемости. В 2015 году рак поджелудочной железы всех типов стал причиной 411 600 смертей во всем мире. [8] Рак поджелудочной железы является пятой по распространенности причиной смерти от рака в Соединенном Королевстве [17] и третьей по распространенности в Соединенных Штатах. [18] Заболевание чаще всего встречается в развитых странах мира, где возникло около 70% новых случаев в 2012 году. [10] Аденокарцинома поджелудочной железы обычно имеет очень плохой прогноз; после постановки диагноза 25% людей выживают один год и 12% живут пять лет. [6] [10] При ранней диагностике рака пятилетняя выживаемость возрастает примерно до 20%. [19] Нейроэндокринный рак имеет лучшие результаты; через пять лет после постановки диагноза 65% пациентов с диагнозом живы, хотя выживаемость значительно варьируется в зависимости от типа опухоли. [10]


Многие типы рака поджелудочной железы можно разделить на две основные группы. Подавляющее большинство случаев (около 95%) возникает в той части поджелудочной железы, которая вырабатывает пищеварительные ферменты , известную как экзокринный компонент . Описано несколько подтипов экзокринного рака поджелудочной железы, но их диагностика и лечение имеют много общего.
Небольшое меньшинство видов рака, которые возникают в гормонпродуцирующей ( эндокринной ) ткани поджелудочной железы, имеют различные клинические характеристики и называются нейроэндокринными опухолями поджелудочной железы , иногда сокращенно «PanNET». Обе группы встречаются в основном (но не исключительно) у людей старше 40 лет и немного чаще встречаются у мужчин, но некоторые редкие подтипы встречаются преимущественно у женщин или детей. [21] [22]
В экзокринной группе преобладает аденокарцинома поджелудочной железы (варианты этого названия могут добавлять «инвазивный» и «протоковой»), которая на сегодняшний день является наиболее распространенным типом и составляет около 85% всех случаев рака поджелудочной железы. [2] Почти все они начинаются в протоках поджелудочной железы, образуя аденокарциному протоков поджелудочной железы (PDAC). [23] И это несмотря на то, что ткань, из которой он возникает – эпителий протоков поджелудочной железы – представляет менее 10% объема клеток поджелудочной железы, поскольку она представляет собой только протоки (обширная, но капилляроподобная система протоков, разветвляющаяся наружу) внутри поджелудочной железы. [24] Этот рак возникает в протоках, по которым секрет (например, ферменты и бикарбонат ) выводится из поджелудочной железы. Около 60–70% аденокарцином встречаются в головке поджелудочной железы . [2]
Следующий по распространенности тип — ацинарно-клеточная карцинома поджелудочной железы — возникает в скоплениях клеток , продуцирующих эти ферменты, и составляет 5% экзокринных раков поджелудочной железы. [25] Подобно «функционирующему» раку эндокринной системы, описанному ниже, ацинарно-клеточная карцинома может вызывать перепроизводство определенных молекул, в данном случае пищеварительных ферментов, что может вызывать такие симптомы, как кожная сыпь и боли в суставах.
Цистаденокарциномы составляют 1% случаев рака поджелудочной железы и имеют лучший прогноз, чем другие экзокринные типы. [25]
Панкреатобластома — редкая форма, чаще встречающаяся в детском возрасте и имеющая относительно хороший прогноз. Другие экзокринные виды рака включают аденосквамозный рак , перстнеклеточный рак , гепатоидный рак , коллоидный рак, недифференцированный рак и недифференцированный рак с остеокластоподобными гигантскими клетками . Солидная псевдопапиллярная опухоль — редкое новообразование низкой степени злокачественности, которое поражает преимущественно молодых женщин и обычно имеет очень хороший прогноз. [2] [26]
Муцинозно-кистозные новообразования поджелудочной железы представляют собой обширную группу опухолей поджелудочной железы с различным потенциалом злокачественности. Их выявляют значительно чаще, поскольку компьютерная томография становится все более мощной и распространенной, и продолжаются дискуссии о том, как лучше всего их оценивать и лечить, учитывая, что многие из них являются доброкачественными. [27]
Небольшое меньшинство опухолей, которые возникают в других частях поджелудочной железы, представляют собой в основном нейроэндокринные опухоли поджелудочной железы (PanNET). [28] Нейроэндокринные опухоли (НЭО) представляют собой разнообразную группу доброкачественных или злокачественных опухолей, которые возникают из нейроэндокринных клеток организма , которые отвечают за интеграцию нервной и эндокринной систем. НЭО могут возникать в большинстве органов тела, включая поджелудочную железу, где все различные типы злокачественных опухолей считаются редкими . PanNET подразделяются на «функционирующие» и «нефункционирующие» типы, в зависимости от степени выработки гормонов. Функционирующие типы выделяют в кровоток такие гормоны, как инсулин , гастрин и глюкагон , часто в больших количествах, вызывая серьезные симптомы, такие как низкий уровень сахара в крови , но также способствуют относительно раннему выявлению. Наиболее распространенными функционирующими PanNET являются инсулиномы и гастриномы , названные в честь гормонов, которые они секретируют. Нефункционирующие типы не секретируют гормоны в достаточном количестве, чтобы вызвать явные клинические симптомы, поэтому нефункционирующие PanNET часто диагностируются только после того, как рак распространился на другие части тела. [29]
Как и в случае с другими нейроэндокринными опухолями, история терминологии и классификации PanNET сложна. [28] PanNET иногда называют «раком островковых клеток», [30] хотя сейчас известно, что они на самом деле не возникают из островковых клеток , как считалось ранее. [29]

Поскольку рак поджелудочной железы обычно не вызывает заметных симптомов на ранних стадиях, заболевание обычно не диагностируется до тех пор, пока оно не распространится за пределы самой поджелудочной железы. [4] Это одна из основных причин низкой выживаемости. Исключением являются функционирующие сети PanNET, в которых перепроизводство различных активных гормонов может вызывать симптомы (которые зависят от типа гормона). [31]
Общие симптомы аденокарциномы поджелудочной железы включают:
Другие распространенные проявления заболевания включают слабость и быструю утомляемость, сухость во рту , проблемы со сном и пальпируемое образование в животе . [33]

Распространение рака поджелудочной железы на другие органы ( метастазирование ) также может вызывать симптомы. Обычно аденокарцинома поджелудочной железы сначала распространяется на близлежащие лимфатические узлы , а затем в печень или брюшную полость , толстую кишку или легкие. [3] В редких случаях он распространяется на кости или мозг. [35]
Рак поджелудочной железы также может быть вторичным раком , распространившимся из других частей тела. Это редкое явление, встречается только примерно в 2% случаев рака поджелудочной железы. Рак почки, безусловно, является наиболее распространенным раком, распространяющимся на поджелудочную железу, за ним следует колоректальный рак , а затем рак кожи , молочной железы и легких . В таких случаях может быть проведена операция на поджелудочной железе, либо в надежде на излечение, либо для облегчения симптомов. [36]
Факторы риска аденокарциномы поджелудочной железы включают: [2] [10] [12] [37] [38] [ чрезмерное цитирование ]
Чрезмерное употребление алкоголя является основной причиной хронического панкреатита , который, в свою очередь, предрасполагает к раку поджелудочной железы, но значительные исследования не смогли твердо установить, что употребление алкоголя является прямым фактором риска развития рака поджелудочной железы. В целом связь неизменно слаба, и большинство исследований не обнаружили никакой связи, при этом курение является сильным искажающим фактором. Доказательства более убедительны в отношении связи с злоупотреблением алкоголем (не менее шести порций в день). [3] [47]
_Case_01.jpg/440px-Pancreas_adenocarcinoma_(4)_Case_01.jpg)


Считается, что экзокринный рак возникает в результате нескольких типов предраковых поражений поджелудочной железы, но эти поражения не всегда перерастают в рак, и не все из них, выявляемые как побочный продукт увеличения использования компьютерной томографии по другим причинам, поддаются лечению. [3] Помимо серозных цистаденом поджелудочной железы , которые почти всегда доброкачественные, выделяют четыре типа предраковых поражений.
Первым из них является интраэпителиальная неоплазия поджелудочной железы (ПанИН). Эти поражения представляют собой микроскопические аномалии поджелудочной железы и часто обнаруживаются при аутопсии людей, у которых не диагностирован рак. Эти поражения могут прогрессировать от низкой до высокой степени , а затем и до опухоли. Более 90% случаев всех степеней несут дефектный ген KRAS , тогда как при 2 и 3 степени все чаще обнаруживаются повреждения еще трех генов — CDKN2A ( p16 ), p53 и SMAD4 . [2]
Второй тип — внутрипротоковое папиллярное муцинозное новообразование (ВПМН). Это макроскопические поражения, которые встречаются примерно у 2% всех взрослых. К 70 годам этот показатель возрастает примерно до 10%. Риск перерастания этих поражений в инвазивный рак составляет около 25%. У них могут быть мутации гена KRAS (40–65% случаев), а также альфа-субъединицы Gs GNAS и RNF43, влияющие на сигнальный путь Wnt . [2] Даже в случае хирургического удаления остается значительно повышенный риск развития рака поджелудочной железы в дальнейшем. [3]
Третий тип, муцинозно-кистозное новообразование поджелудочной железы (МКН), в основном встречается у женщин и может оставаться доброкачественным или прогрессировать в рак. [49] Если эти поражения становятся большими, вызывают симптомы или имеют подозрительные особенности, их обычно можно успешно удалить хирургическим путем. [3]
Четвертый тип рака, возникающий в поджелудочной железе, — это внутрипротоковая тубулопапиллярная опухоль. Этот тип был признан ВОЗ в 2010 г. и составляет около 1–3% всех новообразований поджелудочной железы. Средний возраст на момент постановки диагноза составляет 61 год (диапазон 35–78 лет). Около 50% этих поражений становятся инвазивными. Диагноз зависит от гистологии, поскольку эти поражения очень трудно отличить от других поражений ни по клиническим, ни по радиологическим признакам. [50]
Генетические события, обнаруженные при протоковой аденокарциноме, хорошо охарактеризованы, и для распространенных типов опухолей было проведено полное секвенирование экзома . В большинстве аденокарцином обнаружено мутации по четырем генам: KRAS (в 95% случаев), CDKN2A (также в 95%), TP53 (75%) и SMAD4 (55%). Последнее из них особенно связано с плохим прогнозом. [3] Мутации/ делеции SWI/SNF встречаются примерно в 10–15% аденокарцином. [2] Также были исследованы генетические изменения при некоторых других типах рака поджелудочной железы и предраковых поражениях. [3] Транскриптомический анализ и секвенирование мРНК распространенных форм рака поджелудочной железы показали, что 75% человеческих генов экспрессируются в опухолях, причем около 200 генов более специфически экспрессируются при раке поджелудочной железы по сравнению с другими типами опухолей. [51] [52]
Гены, часто обнаруживаемые мутировавшими в нейроэндокринных опухолях поджелудочной железы (PanNET), отличаются от генов при экзокринном раке поджелудочной железы. [53] Например, мутация KRAS обычно отсутствует. Вместо этого наследственные мутации гена MEN1 создают риск развития синдрома MEN1 , при котором первичные опухоли возникают в двух или более эндокринных железах . Около 40–70% людей, рожденных с мутацией MEN1 , в конечном итоге развивают PanNet. [54] Другие гены, которые часто мутируют, включают DAXX , mTOR и ATRX . [29]
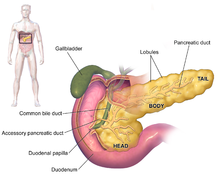


Симптомы аденокарциномы поджелудочной железы обычно не проявляются на ранних стадиях заболевания и не являются индивидуальными особенностями заболевания. [3] [12] [32] Симптомы при постановке диагноза различаются в зависимости от локализации рака поджелудочной железы, который анатомы делят (слева направо на большинстве диаграмм) на толстую головку, шею и сужающееся тело. заканчивающийся хвостом.
Независимо от локализации опухоли, наиболее частым симптомом является необъяснимая потеря веса, которая может быть значительной. У значительного меньшинства (от 35% до 47%) людей с диагнозом этого заболевания наблюдались тошнота, рвота или чувство слабости. Опухоли головки поджелудочной железы обычно также вызывают желтуху, боль, потерю аппетита , темную мочу и светлый стул. Опухоли тела и хвоста обычно также вызывают боль. [32]
У людей иногда наблюдается недавнее начало атипичного диабета 2 типа, который трудно контролировать, недавнее, но необъяснимое воспаление кровеносных сосудов, вызванное тромбами ( тромбофлебит ), известное как симптом Труссо , или предшествующий приступ панкреатита . [32] Врач может заподозрить рак поджелудочной железы, когда начало диабета у человека старше 50 лет сопровождается типичными симптомами, такими как необъяснимая потеря веса, постоянные боли в животе или спине, расстройство желудка, рвота или жирный кал. [12] Желтуха, сопровождающаяся безболезненным раздутием желчного пузыря (известная как симптом Курвуазье ), также может вызвать подозрения и помочь отличить рак поджелудочной железы от камней в желчном пузыре . [55]
Методы медицинской визуализации , такие как компьютерная томография (КТ) и эндоскопическое ультразвуковое исследование (ЭУЗИ), используются как для подтверждения диагноза, так и для принятия решения о том, можно ли удалить опухоль хирургическим путем (ее « резектабельность »). [12] При контрастной КТ рак поджелудочной железы обычно показывает постепенное увеличение поглощения рентгеноконтрастного вещества, а не быстрое вымывание, как это наблюдается в нормальной поджелудочной железе, или замедленное вымывание, как это наблюдается при хроническом панкреатите. [56] Также можно использовать магнитно-резонансную томографию и позитронно-эмиссионную томографию , [2] а в некоторых случаях может быть полезна магнитно-резонансная холангиопанкреатография . [32] УЗИ брюшной полости менее чувствительно и не пропускает небольшие опухоли, но может выявить рак, распространившийся на печень, и скопление жидкости в брюшной полости ( асцит ). [12] Его можно использовать для быстрого и дешевого первого обследования перед другими методами. [57]
.jpg/440px-Adenocarcinoma_of_Pancreas,_FNA_(5558060087).jpg)
Биопсия с помощью тонкоигольной аспирации , часто под контролем эндоскопического ультразвука, может использоваться в тех случаях, когда есть неопределенность в диагнозе, но гистологический диагноз обычно не требуется для дальнейшего удаления опухоли хирургическим путем. [12]
Функциональные тесты печени могут выявить комбинацию результатов, указывающих на обструкцию желчных протоков (повышение уровня конъюгированного билирубина , γ-глутамилтранспептидазы и щелочной фосфатазы ). CA19-9 (углеводный антиген 19.9) является опухолевым маркером , уровень которого часто повышается при раке поджелудочной железы. Однако ему недостает чувствительности и специфичности , не в последнюю очередь потому, что у 5% людей отсутствует антиген Льюиса (а) и они не могут производить CA19-9. Он имеет чувствительность 80% и специфичность 73% при обнаружении аденокарциномы поджелудочной железы и используется для отслеживания известных случаев, а не для диагностики. [2] [12]
Наиболее распространенная форма рака поджелудочной железы (аденокарцинома) обычно характеризуется умеренно или слабо дифференцированными железистыми структурами при микроскопическом исследовании. Обычно наблюдается значительная десмоплазия или образование плотной фиброзной стромы или структурной ткани, состоящей из ряда типов клеток (включая миофибробласты , макрофаги , лимфоциты и тучные клетки ) и отложенного материала (например, коллагена I типа и гиалуроновой кислоты ). Это создает микроокружение опухоли , в котором не хватает кровеносных сосудов (гиповаскуляризация) и, следовательно, кислорода ( гипоксия опухоли ). [2] Считается, что это предотвращает попадание многих химиотерапевтических препаратов в опухоль, поскольку это один из факторов, затрудняющих лечение рака. [2] [3]
Стадию рака поджелудочной железы обычно определяют после компьютерной томографии . [32] Наиболее широко используемой системой стадирования рака поджелудочной железы является система, разработанная Американским объединенным комитетом по раку (AJCC) совместно с Союзом международного контроля рака (UICC). Система стадирования AJCC-UICC определяет четыре основные общие стадии, от ранней до поздних стадий, на основе классификации TNM размера опухоли , распространения в лимфатические узлы и метастазов . [62]
Чтобы помочь определиться с лечением, опухоли также делятся на три более широкие категории в зависимости от того, возможно ли хирургическое удаление: таким образом, опухоли оцениваются как «операбельные», «пограничные резектабельные» или «неоперабельные». [63] Когда заболевание все еще находится на ранней стадии (стадии I и II AJCC-UICC), без распространения на крупные кровеносные сосуды или отдаленные органы, такие как печень или легкие, обычно можно выполнить хирургическую резекцию опухоли, если Пациент готов перенести эту серьезную операцию и считается достаточно здоровым. [12]
Система стадирования AJCC-UICC позволяет различать опухоли III стадии, которые считаются «пограничными резектабельными» (когда хирургическое вмешательство технически осуществимо, поскольку чревная ось и верхняя брыжеечная артерия все еще свободны), и теми, которые «неоперабельны» (из-за большего количества местно-распространенное заболевание); с точки зрения более детальной классификации TNM эти две группы соответствуют Т3 и Т4 соответственно. [3]

Местно-распространенная аденокарцинома распространяется на соседние органы, которыми может быть любой из следующих органов (примерно в порядке убывания частоты): двенадцатиперстная кишка , желудок , поперечная ободочная кишка , селезенка , надпочечники или почки . Очень часто они также распространяются на важные кровеносные или лимфатические сосуды и нервы, проходящие рядом с поджелудочной железой, что значительно затрудняет операцию. Типичными местами метастатического распространения (IV стадия заболевания) являются печень, брюшная полость и легкие , причем все они встречаются в 50% и более случаев полностью запущенных случаев. [64]
В классификации опухолей пищеварительной системы ВОЗ 2010 года все нейроэндокринные опухоли поджелудочной железы (PanNET) подразделяются на три категории в зависимости от степени их клеточной дифференциации (от «NET G1» до низкодифференцированных «NET G3»). [22] Национальная комплексная онкологическая сеть США рекомендует использовать ту же систему стадирования AJCC-UICC, что и аденокарциному поджелудочной железы. [65] : 52 При использовании этой схемы поэтапные результаты для PanNET отличаются от исходов экзокринного рака. [66] Другая система TNM для PanNET была предложена Европейским обществом нейроэндокринных опухолей. [22]
Помимо отказа от курения, Американское онкологическое общество рекомендует поддерживать здоровый вес и увеличивать потребление фруктов, овощей и цельнозерновых продуктов , одновременно снижая потребление красного и обработанного мяса , хотя нет убедительных доказательств того, что это предотвратит или уменьшит именно рак поджелудочной железы. . [67] Обзор исследований 2014 года пришел к выводу, что существуют доказательства того, что потребление цитрусовых и куркумина снижает риск рака поджелудочной железы, в то время как, возможно, существует положительный эффект от цельнозерновых продуктов, фолиевой кислоты , селена и нежареной рыбы. [47]
В общей популяции скрининг больших групп не считается эффективным и может быть вредным по состоянию на 2019 год, [68] , хотя в настоящее время оцениваются новые методы и скрининг узкоцелевых групп. [69] [70] Тем не менее, регулярный скрининг с помощью эндоскопического ультразвука и МРТ/КТ рекомендуется людям с высоким риском наследственной генетики. [4] [57] [70] [71]
Метаанализ 2019 года показал, что использование аспирина может быть отрицательно связано с риском заболеваемости раком поджелудочной железы, но не обнаружил существенной связи со смертностью от рака поджелудочной железы. [72]
Ключевая оценка, которая проводится после постановки диагноза, заключается в том, возможно ли хирургическое удаление опухоли (см. Стадирование), поскольку это единственное лекарство от этого рака. Можно ли предложить хирургическую резекцию или нет, зависит от того, насколько распространился рак. Точное расположение опухоли также является важным фактором, и КТ может показать, как она связана с основными кровеносными сосудами, проходящими вблизи поджелудочной железы. Также необходимо оценить общее состояние здоровья человека, хотя возраст сам по себе не является препятствием для операции. [3]
Большинству людей, вероятно, будут предложены химиотерапия и, в меньшей степени, лучевая терапия, независимо от того, возможна ли операция. Специалисты советуют, что лечение рака поджелудочной железы должно находиться в руках многопрофильной команды, включающей специалистов по нескольким аспектам онкологии , и, следовательно, лучше всего проводить его в более крупных центрах. [2] [3]

Хирургическое вмешательство с целью излечения возможно только примерно в одной пятой (20%) новых случаев. [12] Хотя компьютерная томография помогает, на практике может быть трудно определить, можно ли полностью удалить опухоль (ее «резектабельность»), и только во время операции может стать очевидным, что невозможно успешно удалить опухоль, не повредив ее. другие жизненно важные ткани. Возможность хирургической резекции может быть предложена или нет, зависит от различных факторов, включая точную степень местного анатомического прилегания или вовлечения венозных или артериальных кровеносных сосудов [2] , а также хирургического опыта и тщательного рассмотрения прогнозируемых последствий послеоперационного периода. оперативное восстановление. [73] [74] Возраст человека сам по себе не является причиной отказа от операции, но его общее состояние работоспособности должно быть достаточным для проведения серьезной операции. [12]
Одной из особенностей, которая оценивается, является обнадеживающее наличие или обескураживающее отсутствие прозрачного слоя или плоскости жира, создающего барьер между опухолью и сосудами. [3] Традиционно оценивают близость опухоли к крупным венозным или артериальным сосудам с точки зрения «прилегания» (определяемого как опухоль, касающаяся не более половины окружности кровеносного сосуда без разделяющего ее жира), «оболочки» (когда опухоль охватывает большую часть окружности сосуда) или полное поражение сосуда. [75] : 22 В некоторых случаях возможна резекция, включающая закрытые участки кровеносных сосудов, [76] [77] , особенно если возможна предварительная неоадъювантная терапия , [78] [79] [80] с использованием химиотерапии [74] [ 75] : 36 [81] и/или лучевая терапия. [75] : 29–30
Даже если операция кажется успешной, раковые клетки часто обнаруживаются по краям (« краям ») удаленной ткани, когда патологоанатом исследует их под микроскопом (это всегда будет сделано), что указывает на то, что рак не был полностью удален. . [2] Более того, раковые стволовые клетки обычно не обнаруживаются под микроскопом, и если они присутствуют, они могут продолжать развиваться и распространяться. [82] [83] Поэтому может быть выполнена исследовательская лапароскопия (небольшая хирургическая процедура под контролем камеры), чтобы получить более четкое представление о результате полноценной операции. [84]

При раке головки поджелудочной железы операция Уиппла является наиболее распространенным методом радикального хирургического лечения. Это серьезная операция, которая включает совместное удаление головки поджелудочной железы и изгиба двенадцатиперстной кишки («панкреатодуоденэктомия»), создание обходного пути для поступления пищи из желудка в тощую кишку («гастроеюностомия») и наложение петли тощей кишки. в пузырный проток для оттока желчи («холецисто-еюностомия»). Его можно выполнить только в том случае, если есть вероятность, что человек переживет серьезную операцию и если рак локализован, не прорастая в местные структуры и не метастазируя. Поэтому его можно выполнить лишь в меньшинстве случаев. Рак хвоста поджелудочной железы можно удалить с помощью процедуры, известной как дистальная панкреатэктомия , которая часто также влечет за собой удаление селезенки . [2] [3] В настоящее время это часто можно сделать с помощью минимально инвазивной хирургии . [2] [3]
Хотя лечебная хирургия больше не вызывает столь высоких показателей смертности, как это было до 1980-х годов, значительная часть людей (около 30–45%) по-прежнему нуждается в лечении от послеоперационных заболеваний, не вызванных самим раком. Наиболее частым осложнением операции является затруднение опорожнения желудка. [3] Для облегчения симптомов также можно использовать некоторые более ограниченные хирургические процедуры (см. Паллиативная помощь): например, если рак прорастает или сдавливает двенадцатиперстную или толстую кишку . В таких случаях шунтирование может преодолеть обструкцию и улучшить качество жизни, но не предназначено для лечения. [12]
После операции может быть предложена адъювантная химиотерапия гемцитабином или 5-ФУ, если человек достаточно здоров , после периода восстановления продолжительностью от одного до двух месяцев. [4] [57] У людей, которым не подходит хирургическое вмешательство, химиотерапия может использоваться для продления жизни или улучшения ее качества . [3] Перед операцией в случаях, которые считаются «пограничными резектабельными» (см. «Стадирование»), можно использовать неоадъювантную химиотерапию или химиолучевую терапию , чтобы снизить рак до уровня, при котором хирургическое вмешательство может оказаться полезным. В других случаях неоадъювантная терапия остается спорной, поскольку откладывает хирургическое вмешательство. [3] [4] [85]
Гемцитабин был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) в 1997 году после того, как клинические испытания показали улучшение качества жизни и пятинедельное улучшение средней продолжительности жизни у людей с распространенным раком поджелудочной железы. [86] Это был первый химиотерапевтический препарат, одобренный FDA в первую очередь для конечной точки клинического исследования, не связанной с выживанием. [87] Химиотерапия с использованием только гемцитабина была стандартом в течение примерно десяти лет, поскольку ряд испытаний, тестирующих его в сочетании с другими препаратами, не смогли продемонстрировать значительно лучшие результаты. Однако было обнаружено, что комбинация гемцитабина с эрлотинибом незначительно увеличивает выживаемость, и в 2005 году FDA лицензировало эрлотиниб для применения при раке поджелудочной железы [88].
Схема химиотерапии FOLFIRINOX с использованием четырех препаратов оказалась более эффективной, чем гемцитабин, но с существенными побочными эффектами и поэтому подходит только для людей с хорошим физическим состоянием. Это также относится к связанному с белками паклитакселу (наб-паклитакселу), который был лицензирован FDA в 2013 году для использования с гемцитабином при раке поджелудочной железы. [89] К концу 2013 года и FOLFIRINOX, и наб-паклитаксел с гемцитабином считались хорошим выбором для тех, кто способен переносить побочные эффекты, а гемцитабин оставался эффективным вариантом для тех, кто этого не делал. Ожидается прямое испытание двух новых вариантов, и испытания по изучению других вариантов продолжаются. Однако изменения последних нескольких лет увеличили время выживания лишь на несколько месяцев. [86] Часто проводятся клинические испытания новых адъювантных методов лечения. [4]
Роль лучевой терапии как вспомогательного (адъювантного) лечения после потенциально излечивающего хирургического вмешательства вызывает споры с 1980-х годов. [3] В начале 2000-х годов Европейская исследовательская группа по исследованию рака поджелудочной железы ( ESPAC ) продемонстрировала прогностическое превосходство адъювантной химиотерапии над химиолучевой терапией. [90] [91] [4] Европейское общество медицинской онкологии рекомендует использовать адъювантную лучевую терапию только для людей, участвующих в клинических исследованиях. [57] Тем не менее, сохраняется тенденция к тому, что врачи в США более готовы использовать адъювантную лучевую терапию, чем врачи в Европе. Многие клинические испытания, начиная с 1980-х годов, проверяли различные комбинации лечения, но не смогли окончательно решить этот вопрос. [3] [4]
Лучевая терапия может стать частью лечения, направленного на уменьшение опухоли до резектабельного состояния, но ее использование при неоперабельных опухолях остается спорным, поскольку существуют противоречивые результаты клинических испытаний. Предварительные результаты одного исследования, представленные в 2013 году, «заметно снизили энтузиазм» по поводу его использования при местно-распространенных опухолях. [2]
Лечение PanNET, включая менее распространенные злокачественные типы, может включать ряд подходов. [65] [92] [93] [94] Некоторые небольшие опухоли размером менее 1 см. которые идентифицируются случайно, например, при компьютерной томографии, выполненной для других целей, может сопровождаться бдительным ожиданием . [65] Это зависит от предполагаемого риска хирургического вмешательства, на который влияет расположение опухоли и наличие других медицинских проблем . [65] Опухоли только в поджелудочной железе (локализованные опухоли) или с ограниченными метастазами, например в печень, могут быть удалены хирургическим путем. Тип операции зависит от локализации опухоли и степени распространения на лимфатические узлы. [22]
Для локализованных опухолей хирургическая процедура может быть гораздо менее обширной, чем виды хирургического вмешательства, используемые для лечения аденокарциномы поджелудочной железы, описанные выше, но в остальном хирургические процедуры аналогичны таковым при экзокринных опухолях. Диапазон возможных результатов сильно различается; некоторые типы имеют очень высокую выживаемость после операции, в то время как другие имеют плохой прогноз. Поскольку все эти группы встречаются редко, в руководствах подчеркивается, что лечение должно проводиться в специализированном центре. [22] [29] В некоторых случаях метастазов в печень можно рассмотреть возможность трансплантации печени. [95]
При функционирующих опухолях препараты класса аналогов соматостатина , такие как октреотид , могут снизить чрезмерную выработку гормонов. [22] Ланреотид может замедлить рост опухоли. [96] Если опухоль не поддается хирургическому удалению и вызывает симптомы, таргетная терапия эверолимусом или сунитинибом может уменьшить симптомы и замедлить прогрессирование заболевания. [29] [97] [98] Стандартная цитотоксическая химиотерапия, как правило, не очень эффективна при PanNET, но может использоваться, когда другие медикаментозные методы лечения не могут предотвратить прогрессирование заболевания [29] или при низкодифференцированном раке PanNET. [99]
Лучевая терапия иногда используется, если возникает боль из-за анатомического расширения, например, метастазов в кости. Некоторые PanNET поглощают определенные пептиды или гормоны, и эти PanNET могут реагировать на терапию ядерной медициной с помощью радиоактивно меченных пептидов или гормонов, таких как иобенгуан (йод-131-MIBG). [100] [101] [102] [103] Также могут использоваться радиочастотная абляция (РЧА), криоабляция и эмболизация печеночной артерии . [104] [105]
Паллиативная помощь – это медицинская помощь, направленная на лечение симптомов серьезных заболеваний, таких как рак, и улучшение качества жизни. [106] Поскольку аденокарцинома поджелудочной железы обычно диагностируется после того, как она достигла поздней стадии, паллиативная помощь как лечение симптомов часто является единственным возможным лечением. [107]
Паллиативная помощь направлена не на лечение основного рака, а на лечение таких симптомов, как боль или тошнота, и может помочь в принятии решений, в том числе о том, когда и будет ли хосписная помощь полезной. [108] Боль можно контролировать с помощью лекарств, таких как опиоиды , или посредством процедурного вмешательства путем блокады нерва чревного сплетения (CPB). Это изменяет или, в зависимости от используемой техники, разрушает нервы, передающие боль из живота. CPB — безопасный и эффективный способ уменьшить боль, который обычно снижает необходимость использования опиоидных обезболивающих, которые имеют значительные негативные побочные эффекты. [3] [109]
Другими симптомами или осложнениями, которые можно лечить с помощью паллиативной хирургии, являются непроходимость опухолью кишечника или желчных протоков . В последнем случае, который встречается более чем в половине случаев, с помощью эндоскопа можно вставить небольшую металлическую трубку, называемую стентом , чтобы обеспечить дренирование протоков. [32] Паллиативная помощь также может помочь в лечении депрессии, которая часто сопровождается диагнозом рака поджелудочной железы. [3]
Как хирургическое вмешательство, так и распространенные неоперабельные опухоли часто приводят к расстройствам пищеварительной системы из-за недостатка экзокринных продуктов поджелудочной железы (экзокринная недостаточность). Их можно лечить, принимая панкреатин , который содержит произведенные ферменты поджелудочной железы, и его лучше всего принимать во время еды. [12] Затруднение опорожнения желудка (задержка опорожнения желудка) является распространенным явлением и может стать серьезной проблемой, требующей госпитализации. Лечение может включать в себя различные подходы, включая дренирование желудка путем назогастральной аспирации и применение препаратов, называемых ингибиторами протонной помпы или антагонистами H 2 , которые снижают выработку желудочной кислоты . [12] Для очистки содержимого желудка также можно использовать такие лекарства, как метоклопрамид .
Аденокарцинома поджелудочной железы и другие менее распространенные экзокринные виды рака имеют очень плохой прогноз , поскольку они обычно диагностируются на поздней стадии, когда рак уже локально распространен или распространился на другие части тела. [2] Результаты PanNET намного лучше: многие из них являются доброкачественными и полностью лишены клинических симптомов, и даже в тех случаях, которые не поддаются хирургическому лечению, средняя пятилетняя выживаемость составляет 16%, [63] хотя прогноз значительно варьируется в зависимости от тип. [31]
Для местно-распространенной и метастатической аденокарциномы поджелудочной железы, которые в совокупности составляют более 80% случаев, многочисленные исследования, сравнивающие режимы химиотерапии, показали увеличение времени выживаемости, но не более одного года. [2] [86] Общая пятилетняя выживаемость при раке поджелудочной железы в США улучшилась с 2% в случаях, диагностированных в 1975–1977 годах, и 4% в случаях диагнозов 1987–1989 годов, до 6% в 2003–2009 годах. [110] В менее чем 20% случаев аденокарциномы поджелудочной железы с диагнозом локализованного и небольшого ракового образования (менее 2 см на стадии Т1) около 20% американцев доживают до пяти лет. [19]
Около 1500 генов связаны с исходами аденокарциномы поджелудочной железы. К ним относятся как неблагоприятные гены, высокая экспрессия которых связана с плохим исходом, например C-Met и MUC-1 , так и благоприятные гены, высокая экспрессия которых связана с лучшей выживаемостью, например фактор транскрипции PELP1 . [51] [52]

В 2015 году рак поджелудочной железы всех типов стал причиной 411 600 смертей во всем мире. [8] Ожидается, что в 2014 году примерно у 46 000 человек в США будет диагностирован рак поджелудочной железы и 40 000 умрут от него. [2] Хотя рак поджелудочной железы составляет лишь 2,5% новых случаев, он является причиной 6% случаев смерти от рака каждый год. [111] Это седьмая по значимости причина смертности от рака в мире. [10] Рак поджелудочной железы является пятой по распространенности причиной смерти от рака в Соединенном Королевстве [17] и третьей по распространенности в Соединенных Штатах. [18]
В мировом масштабе рак поджелудочной железы занимает 11-е место среди наиболее распространенных видов рака у женщин и 12-е место среди мужчин. [10] Большинство зарегистрированных случаев приходится на развитые страны . [10] Жители США имеют средний риск развития заболевания в течение жизни примерно 1 из 67 (или 1,5%), [112] немного выше, чем в Великобритании. [113] Заболевание чаще встречается у мужчин, чем у женщин, [2] [10] хотя разница в показателях сократилась за последние десятилетия, что, вероятно, отражает более раннее увеличение числа курящих женщин. В Соединенных Штатах риск для афроамериканцев более чем на 50% выше, чем для белых , но показатели в Африке и Восточной Азии намного ниже, чем в Северной Америке или Европе. Высокие показатели наблюдаются в США, Центральной и Восточной Европе, а также в Аргентине и Уругвае . [10]
Ежегодная заболеваемость клинически распознаваемыми нейроэндокринными опухолями поджелудочной железы (ПанНЭО) невелика (около 5 на миллион человеко-лет) и преобладают нефункционирующие типы. [26] Считается, что где-то от 45% до 90% сетей PanNET относятся к нефункциональным типам. [22] [29] Исследования аутопсии довольно часто выявляли небольшие PanNET, что позволяет предположить, что распространенность опухолей , которые остаются инертными и бессимптомными , может быть относительно высокой. [29] Считается, что в целом PanNETs составляют от 1 до 2% всех опухолей поджелудочной железы. [26] Определение и классификация PanNET со временем изменились, что повлияло на то, что известно об их эпидемиологии и клинической значимости. [53]
Самое раннее признание рака поджелудочной железы приписывают итальянскому учёному XVIII века Джованни Баттисте Морганьи , историческому отцу современной анатомической патологии , который утверждал, что обнаружил несколько случаев рака поджелудочной железы. Многие врачи 18 и 19 веков скептически относились к существованию этого заболевания, учитывая схожесть панкреатита. Некоторые сообщения о случаях заболевания были опубликованы в 1820-х и 1830-х годах, а подлинный гистопатологический диагноз в конечном итоге был зафиксирован американским клиницистом Джейкобом Мендесом Да Костой , который также усомнился в достоверности интерпретаций Морганьи. К началу 20 века рак головки поджелудочной железы стал общепринятым диагнозом. [114]
Что касается распознавания PanNET, возможность рака островковых клеток была первоначально предложена в 1888 году. Первый случай гиперинсулинизма , вызванного опухолью этого типа, был зарегистрирован в 1927 году. Распознавание неинсулинсекретирующего типа PanNET обычно приписывается американским хирургам Р. М. Золлингеру и Э. Х. Эллисону, давшим свои имена синдрому Золлингера-Эллисона , после постулирования существования гастрин-секретирующей опухоли поджелудочной железы в сообщении о двух случаях необычайно тяжелых пептических язв, опубликованном в 1955 году . [114] ] В 2010 году ВОЗ рекомендовала называть PanNETs «нейроэндокринными», а не «эндокринными» опухолями. [28]
Небольшие предраковые новообразования при многих видах рака поджелудочной железы выявляются с гораздо большей частотой с помощью современной медицинской визуализации. Один тип, внутрипротоковое папиллярное муцинозное новообразование (ВПМН), был впервые описан японскими исследователями в 1982 году. В 2010 году было отмечено, что: «В течение следующего десятилетия этому сообщению уделялось мало внимания; однако в течение последующих 15 лет появились произошел настоящий взрыв в признании этой опухоли». [64]
Первая зарегистрированная частичная панкреатодуоденэктомия была выполнена итальянским хирургом Алессандро Кодивиллой в 1898 году, но пациент прожил всего 18 дней, прежде чем скончался от осложнений. Ранние операции были скомпрометированы отчасти из-за ошибочного убеждения, что люди умрут, если удалить двенадцатиперстную кишку, а также, поначалу, если прекратится отток панкреатического сока. Позже считалось (также ошибочно), что проток поджелудочной железы можно просто перевязать без серьезных побочных эффектов; на самом деле, позже он очень часто будет протекать. В 1907–1908 годах, после еще нескольких неудачных операций других хирургов, французские хирурги опробовали экспериментальные процедуры на трупах. [115]
В 1912 году немецкий хирург Вальтер Кауш первым удалил большие части двенадцатиперстной кишки и поджелудочной железы вместе ( en bloc ). Это было в Бреслау, ныне Вроцлаве , в Польше. В 1918 году при операциях на собаках было продемонстрировано, что можно выжить даже после полного удаления двенадцатиперстной кишки, но в хирургии человека о таком результате не сообщалось до 1935 года, когда американский хирург Аллен Олдфатер Уиппл опубликовал результаты серии исследований. трех операций в пресвитерианской больнице Колумбии в Нью-Йорке. Только одному из пациентов полностью удалили двенадцатиперстную кишку, но он прожил два года, прежде чем умер от метастазов в печень.
Первая операция была незапланированной, так как рак обнаружили только в операционной. Успех Уиппла указал путь в будущее, но операция оставалась сложной и опасной до последних десятилетий. Он опубликовал несколько усовершенствований своей процедуры, в том числе первое полное удаление двенадцатиперстной кишки в 1940 году, но всего он выполнил всего 37 операций. [115]
Открытие в конце 1930-х годов того, что витамин К предотвращает кровотечение при желтухе , а также развитие переливания крови как повседневного процесса улучшили послеоперационную выживаемость [115] , но около 25% людей никогда не покидали больницы живыми даже в 1970-х годах. . [116] В 1970-х годах группа американских хирургов написала письмо, в котором убеждала, что процедура слишком опасна и от нее следует отказаться. С тех пор результаты в более крупных центрах значительно улучшились, а смертность от операции часто составляет менее 4%. [24]
В 2006 году был опубликован отчет о серии из 1000 последовательных панкреатико-дуоденэктомий, выполненных одним хирургом из больницы Джонса Хопкинса в период с 1969 по 2003 год. Частота этих операций неуклонно росла за этот период, причем только три из них были выполнены до 1980 года, и среднее время работы сократилось с 8,8 часов в 1970-х годах до 5,5 часов в 2000-х, а смертность в течение 30 дней или в больнице составила всего 1%. [115] [116] Другая серия из 2050 операций в Массачусетской больнице общего профиля в период с 1941 по 2011 год показала аналогичную картину улучшения. [117]
Исследования на ранней стадии рака поджелудочной железы включают изучение генетики и раннего выявления, лечения на различных стадиях рака, хирургических стратегий и таргетной терапии , такой как ингибирование факторов роста , иммунная терапия и вакцины . [42] [118] [119] [120] [121] Желчные кислоты могут играть роль в канцерогенезе рака поджелудочной железы. [122]
Ключевым вопросом является время развития и прогрессирования заболевания, в частности, роль диабета [ 118] [34] и то, как и когда заболевание распространяется. [123] Знание того, что новое начало диабета может быть ранним признаком заболевания, может способствовать своевременной диагностике и профилактике , если будет разработана работоспособная стратегия скрининга. [118] [34] [124] Цель исследования Европейского регистра наследственного панкреатита и семейного рака поджелудочной железы (EUROPAC) – определить, подходит ли регулярный скрининг людям с семейным анамнезом этого заболевания. [125]
Оценивается хирургия замочной скважины ( лапароскопия ), а не процедура Уиппла , особенно с точки зрения времени восстановления. [126] Необратимая электропорация — относительно новый метод абляции , способный снизить стадию и продлить выживаемость у людей с местно-распространенным заболеванием, особенно для опухолей, расположенных вблизи перипанкреатических сосудов, без риска сосудистой травмы. [127] [128]
В настоящее время предпринимаются усилия по разработке новых лекарств, в том числе воздействующих на молекулярные механизмы возникновения рака, [ 129] [130] на стволовые клетки [83] и пролиферацию клеток . [130] [131] Дальнейший подход включает использование иммунотерапии , такой как онколитические вирусы . [132] Галектин -специфические механизмы микроокружения опухоли находятся в стадии изучения. [133]
Наночастицы способствуют устойчивому и целенаправленному высвобождению лекарственного препарата к участкам, специфичным для рака/опухоли, а не затрагивают здоровые клетки, что приводит к незначительной токсичности или ее отсутствию. [134]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ). Диаграмма Микаэля Хэггстрема, доктора медицинских наук.{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )(распространяется на условиях международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/)), название изображения и оптимизация: Микаэль Хэггстрем, доктор медицинских наук{{cite web}}: CS1 maint: несколько имен: список авторов ( ссылка )Последнее обновление автора: 4 марта 2022 г.{{cite journal}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )