
Местный анестетик ( МА ) — это лекарство , которое вызывает отсутствие всех ощущений (включая боль ) в определенной части тела без потери сознания, [1] обеспечивая местную анестезию , в отличие от общего анестетика , который устраняет все ощущения во всем теле и вызывает потерю сознания . [1] Местные анестетики чаще всего используются для устранения боли во время или после операции. [2] При его использовании на определенных нервных путях ( блокада нервов местной анестезией ) также может быть вызван паралич (потеря мышечной функции). [3]
ЛА бывают двух типов:
Синтетические местные антидепрессанты, полученные из кокаина, отличаются от кокаина тем, что обладают гораздо меньшим потенциалом злоупотребления и не вызывают гипертензивной вазоконстрикции (за редкими исключениями).
Суффикс «-каин» в конце названий этих лекарств произошел от слова « кокаин », поскольку раньше кокаин использовался в качестве местного анестетика.
Короткая продолжительность действия и низкая эффективность
Средняя продолжительность действия и средняя эффективность
Высокая продолжительность и высокая эффективность
Местные анестетики могут использоваться для профилактики и/или лечения острой боли, лечения хронической боли, а также в качестве дополнения к общей анестезии.
Они используются в различных методиках местной анестезии, таких как:
Несмотря на то, что острую боль можно контролировать с помощью анальгетиков , проводниковая анестезия может быть предпочтительнее из-за превосходного контроля боли и меньшего количества побочных эффектов. [ требуется цитата ] Для целей терапии боли препараты LA часто вводятся путем повторной инъекции или непрерывной инфузии через катетер. Препараты LA также часто сочетаются с другими средствами, такими как опиоиды, для синергического анальгетического действия. [5] Низкие дозы препаратов LA могут быть достаточными для того, чтобы не возникало мышечной слабости и пациенты могли быть мобилизованы. [ требуется цитата ]
Некоторые типичные применения проводниковой анестезии при острой боли:
Хроническая боль — это сложное и часто серьезное состояние, которое требует диагностики и лечения экспертом в области медицины боли. МА можно применять многократно или непрерывно в течение длительных периодов времени для облегчения хронической боли, обычно в сочетании с такими лекарствами, как опиоиды , НПВП и противосудорожные препараты . Хотя это можно легко выполнить, повторные местные анестезирующие блокады при хронических болевых состояниях не рекомендуются, поскольку нет никаких доказательств их долгосрочной пользы. [6]
Практически любая часть тела может быть обезболена с помощью проводниковой анестезии. Однако только ограниченное количество методов широко используется в клинической практике. Иногда проводниковая анестезия сочетается с общей анестезией или седацией для комфорта пациента и облегчения операции. Однако многие анестезиологи, хирурги, пациенты и медсестры считают, что безопаснее проводить крупные операции под местной анестезией, чем под общей анестезией. [7] Типичные операции, выполняемые под проводниковой анестезией, включают:
Диагностические тесты, такие как аспирация костного мозга, люмбальная пункция (спинномозговая пункция) и аспирация кист или других структур, становятся менее болезненными при введении местной анестезии перед введением более крупных игл. [8]
Местная анестезия также используется при введении внутривенных устройств, таких как кардиостимуляторы и имплантируемые дефибрилляторы, портов, используемых для введения химиотерапевтических препаратов, и катетеров для гемодиализа. [8]
Местная анестезия в виде лидокаина/прилокаина (ЭМЛА) чаще всего используется для обеспечения относительно безболезненной венепункции ( взятия крови ) и установки внутривенных канюль . Она также может быть пригодна для других видов пункций, таких как дренирование асцита и амниоцентез .
Поверхностная анестезия также облегчает проведение некоторых эндоскопических процедур, таких как бронхоскопия (визуализация нижних дыхательных путей) или цистоскопия (визуализация внутренней поверхности мочевого пузыря).
Отек языка, глотки и гортани может развиться как побочный эффект местной анестезии. Это может быть вызвано различными причинами, включая травму во время инъекции, инфекцию, аллергическую реакцию, гематому или инъекцию раздражающих растворов, таких как растворы для холодной стерилизации. Обычно в месте инъекции наблюдается отек тканей. Это происходит из-за прокола вены, что позволяет крови течь в рыхлые ткани в окружающей области. Побледнение тканей в области, где откладывается местный анестетик, также является обычным явлением. Это придает области белый вид, поскольку кровоток предотвращается из-за вазоконстрикции артерий в этой области. Стимул вазоконстрикции постепенно исчезает, и впоследствии ткань возвращается в нормальное состояние менее чем за два часа. [11]
Побочные эффекты блокады нижнего альвеолярного нерва включают чувство напряжения, сжимание кулаков и стоны. [12]
Продолжительность анестезии мягких тканей больше, чем анестезии пульпы, и часто связана с трудностями при приеме пищи, питье и речи. [12]
Риск временного или постоянного повреждения нервов варьируется в зависимости от местоположения и типа блокады нервов . [13]
Существует риск случайного повреждения местных кровеносных сосудов во время инъекции раствора местного анестетика. Это называется гематомой и может привести к боли, тризму , отеку и/или изменению цвета области. Плотность тканей, окружающих поврежденные сосуды, является важным фактором для гематомы. Наибольшая вероятность этого возникает при блокаде заднего верхнего альвеолярного нерва или при блокаде крыловидно-нижнечелюстного нерва. [ необходима цитата ]
Назначение местной анестезии пациентам с заболеваниями печени может иметь существенные последствия. Тщательная оценка заболевания должна быть проведена для оценки потенциального риска для пациента, так как при значительном нарушении функции печени период полувыведения амидных местных анестетиков может быть резко увеличен, что повышает риск передозировки.
Местные анестетики и вазоконстрикторы можно вводить беременным пациенткам, однако очень важно быть особенно осторожным при назначении беременной пациентке любого типа препарата. Лидокаин можно безопасно использовать, но бупивакаина и мепивакаина следует избегать. Консультация с акушером жизненно важна перед введением любого типа местного анестетика беременной пациентке. [11]
Постоянное повреждение нерва после периферической блокады нерва встречается редко. Симптомы, скорее всего, исчезнут в течение нескольких недель. Подавляющее большинство пострадавших (92–97%) выздоравливают в течение четырех-шести недель; 99% из этих людей выздоравливают в течение года. По оценкам, один из 5000–30000 случаев блокады нерва приводит к некоторой степени постоянного стойкого повреждения нерва. [13]
Симптомы могут продолжать улучшаться в течение 18 месяцев после травмы.
Общие системные побочные эффекты обусловлены фармакологическими эффектами используемых анестетиков. Проведение электрических импульсов происходит по схожему механизму в периферических нервах , центральной нервной системе и сердце . Поэтому эффекты местных анестетиков неспецифичны для проведения сигнала в периферических нервах. Побочные эффекты на центральную нервную систему и сердце могут быть серьезными и потенциально фатальными. Однако токсичность обычно возникает только на уровнях в плазме, которые редко достигаются при соблюдении надлежащих методов анестезии. Высокие уровни в плазме могут возникать, например, когда дозы, предназначенные для эпидурального или интраопорного введения тканей, случайно вводятся в виде внутрисосудистой инъекции. [ необходима цитата ]
Когда пациенты эмоционально затронуты в форме нервозности или страха, это может привести к вазовагальному коллапсу. Это ожидание боли во время введения, которое активирует парасимпатическую нервную систему , одновременно подавляя ортосимпатическую нервную систему. [14] Результатом является расширение артерий в мышцах, что может привести к уменьшению объема циркулирующей крови, вызывая временную нехватку притока крови к мозгу. Известные симптомы включают беспокойство, видимую бледность, потливость и возможную потерю сознания. В тяжелых случаях могут возникнуть клонические судороги, напоминающие эпилептический инсульт. [14]
С другой стороны, страх перед введением может также привести к ускоренному, поверхностному дыханию или гипервентиляции . Пациент может чувствовать покалывание в руках и ногах или чувство головокружения и повышенное давление в груди. [ необходима цитата ]
Поэтому для медицинского работника, проводящего местную анестезию, особенно в форме инъекции, крайне важно обеспечить пациенту комфортную обстановку и устранить все возможные страхи, чтобы избежать возможных осложнений.
В зависимости от концентрации местных анестетиков в тканях может возникнуть возбуждающее или угнетающее действие на центральную нервную систему.
Первоначальные симптомы системной токсичности включают звон в ушах ( тиннитус ), металлический привкус во рту, покалывание или онемение во рту, головокружение и/или дезориентацию.
При более высоких концентрациях относительно селективная депрессия тормозных нейронов приводит к церебральному возбуждению, что может привести к более серьезным симптомам, включая двигательные подергивания на периферии с последующими большими эпилептическими припадками . Сообщается, что припадки чаще возникают при использовании бупивакаина, особенно в сочетании с хлоропрокаином. [15]
Глубокое угнетение функций мозга может возникнуть при еще более высоких концентрациях, что может привести к коме , остановке дыхания и смерти. [16] Такие концентрации в тканях могут быть обусловлены очень высокими уровнями в плазме после внутривенной инъекции большой дозы.
Другой возможностью является прямое воздействие на центральную нервную систему через спинномозговую жидкость , т. е. передозировка при спинномозговой анестезии или случайная инъекция в субарахноидальное пространство при эпидуральной анестезии.
Кардиотоксичность может возникнуть в результате неправильного введения агента в сосуд. Даже при правильном введении неизбежна некоторая диффузия агента в организм из места применения из-за непредвиденных анатомических особенностей пациента. [15] Это может повлиять на нервную систему или привести к попаданию агента в общий кровоток. Однако инфекции передаются очень редко.
Кардиотоксичность, связанная с передозировкой внутрисосудистой инъекции местного анестетика, характеризуется гипотензией , задержкой атриовентрикулярной проводимости, идиовентрикулярными ритмами и возможным сердечно-сосудистым коллапсом. Хотя все местные анестетики потенциально сокращают рефрактерный период миокарда, бупивакаин блокирует сердечные натриевые каналы, тем самым делая его наиболее вероятным для ускорения злокачественных аритмий . Даже левобупивакаин и ропивакаин (производные одного энантиомера), разработанные для смягчения сердечно-сосудистых побочных эффектов, по-прежнему несут в себе потенциал для нарушения сердечной функции. [17] Токсичность от комбинаций анестетиков является аддитивной. [15]
Эндокринная и метаболическая системы имеют лишь незначительные неблагоприятные эффекты, и в большинстве случаев клинические последствия отсутствуют. [15]
Побочные реакции на местные анестетики (особенно эфиры) не являются редкостью, но легитимные аллергии очень редки. Аллергические реакции на эфиры обычно обусловлены чувствительностью к их метаболиту, парааминобензойной кислоте , и не приводят к перекрестной аллергии на амиды. [18] [19] Поэтому амиды могут использоваться в качестве альтернативы у этих пациентов. Неаллергические реакции могут напоминать аллергию по своим проявлениям. В некоторых случаях для установления диагноза аллергии могут потребоваться кожные пробы и провокационная проба. Также встречаются случаи аллергии на производные парабенов , которые часто добавляют в качестве консервантов в растворы местных анестетиков.
Метгемоглобинемия — это процесс, при котором изменяется содержание железа в гемоглобине, что снижает его способность переносить кислород, что вызывает цианоз и симптомы гипоксии . Воздействие химических веществ группы анилина, таких как бензокаин , лидокаин и прилокаин, может вызывать этот эффект, особенно бензокаин. [18] [19] Системная токсичность прилокаина сравнительно низкая, но известно, что его метаболит, о-толуидин, вызывает метгемоглобинемию .
Применение местных анестетиков во время извлечения ооцитов во время экстракорпорального оплодотворения стало предметом дискуссий. Фармакологические концентрации анестетиков были обнаружены в фолликулярной жидкости. [15] Клинические испытания не пришли к выводу о каком-либо влиянии на беременных женщин. Однако есть некоторые опасения относительно поведенческих эффектов лидокаина на потомство у крыс. [15]
Во время беременности местные анестетики нечасто оказывают какое-либо неблагоприятное воздействие на плод. Несмотря на это, риски токсичности могут быть выше во время беременности из-за увеличения несвязанной фракции местного анестетика, а физиологические изменения увеличивают передачу местного анестетика в центральную нервную систему. [15] Следовательно, беременным женщинам рекомендуется использовать более низкую дозу местного анестетика, чтобы снизить возможные осложнения.
Терапия липидной эмульсией или липидное спасение — это метод лечения токсичности, изобретенный доктором Гаем Вайнбергом в 1998 году и не использовавшийся широко до первой публикации успешного спасения в 2006 году. Имеющиеся данные указывают на то, что Интралипид , общедоступная внутривенная липидная эмульсия, может быть эффективна при лечении тяжелой кардиотоксичности, вызванной передозировкой местных анестетиков, включая сообщения о случаях заболевания людей. [20] [21] [22] [23] [24] Однако на данный момент доказательств все еще недостаточно. [25]
Хотя в большинстве отчетов о случаях на сегодняшний день зафиксировано наиболее распространенное применение Интралипида, другие эмульсии, такие как Липозин и Медиалипид, также продемонстрировали свою эффективность. [ необходима цитата ]
Множество подтверждающих данных о животных [20] [21] и отчетов о случаях заболевания людей показывают успешное использование липидного спасения таким образом. [23] [24] В Великобритании были предприняты усилия по более широкому распространению липидного спасения. [22] В 2010 году липидное спасение было официально представлено Ассоциацией анестезиологов Великобритании и Ирландии в качестве метода лечения токсичности местных анестетиков . [26] Сообщалось об одном опубликованном случае успешного лечения рефрактерной остановки сердца при передозировке бупропиона и ламотриджина с использованием липидной эмульсии. [27]
Была описана конструкция «домашнего» набора для спасения липидов. [28]
Хотя механизм действия липидного спасения не полностью понят, добавленный липид в кровоток может действовать как сток, позволяя удалять липофильные токсины из пораженных тканей. Эта теория согласуется с двумя исследованиями по липидному спасению при токсичности кломипрамина у кроликов [29] [30] и с клиническим отчетом об использовании липидного спасения в ветеринарии для лечения щенка с токсикозом моксидектина . [31]
Все LA являются мембраностабилизирующими препаратами; они обратимо снижают скорость деполяризации и реполяризации возбудимых мембран (например, ноцицепторов ). Хотя многие другие препараты также обладают мембраностабилизирующими свойствами, не все они используются в качестве LA ( например, пропранолол , хотя он и обладает свойствами LA). Препараты LA действуют в основном путем ингибирования притока натрия через натрий-специфические ионные каналы в мембране нейрональных клеток , в частности, так называемые потенциалзависимые натриевые каналы. Когда приток натрия прерывается, потенциал действия не может возникнуть, и проведение сигнала ингибируется. Считается, что рецепторный участок расположен в цитоплазматической (внутренней) части натриевого канала. Местные анестетики легче связываются с натриевыми каналами в активированном состоянии, поэтому начало нейрональной блокады происходит быстрее в быстро активирующихся нейронах. Это называется блокадой, зависящей от состояния.
LA являются слабыми основаниями и обычно формулируются в виде гидрохлоридной соли, чтобы сделать их водорастворимыми. При pH, равном pKa протонированного основания, протонированная (ионизированная) и непротонированная (неионизированная) формы молекулы существуют в эквимолярных количествах, но только непротонированное основание легко диффундирует через клеточные мембраны. Попав внутрь клетки, местный анестетик будет находиться в равновесии с образованием протонированной (ионизированной) формы, которая нелегко выходит обратно из клетки. Это называется «ионным захватом». В протонированной форме молекула связывается с сайтом связывания LA на внутренней стороне ионного канала вблизи цитоплазматического конца. Большинство LA работают на внутренней поверхности мембраны — лекарство должно проникнуть через клеточную мембрану, что лучше всего достигается в неионизированной форме. Примером этого является постоянно ионизированный LA RAC 421-II , который не может диффундировать через клеточную мембрану, но при введении в цитозоль нервного волокна может вызывать блокаду NaKATPase и анестезирующий эффект.
Ацидоз, вызванный воспалением раны, частично снижает действие местных анестетиков. Это отчасти связано с тем, что большая часть анестетика ионизирована и, следовательно, неспособна пересекать клеточную мембрану, чтобы достичь своего цитоплазматического участка действия на натриевом канале.
У большинства пациентов введение местных анестетиков вызывает первую потерю ощущения боли, затем температуры, прикосновения, глубокого давления и, наконец, двигательной функции. [32] Чувствительность нервных волокон к блокаде зависит от комбинации диаметра и миелинизации. Их различная чувствительность к блокаде LA называется дифференциальной блокадой. Миелинизированные волокна более чувствительны к блокаде, поскольку они прерываются перехватами Ранвье , таким образом, прерывание только последовательных перехватов Ранвье предотвратит распространение потенциала действия. В свою очередь, в немиелинизированных нервах необходимо блокировать всю длину. [33] Что касается диаметра, общепринятый принцип заключается в том, что восприимчивость к местной анестезии обратно пропорциональна диаметру волокна. [34]
В целом, автономные волокна типа B , небольшие немиелинизированные волокна типа C (болевые ощущения) и небольшие миелинизированные волокна Aδ (болевые и температурные ощущения) блокируются раньше, чем более крупные миелинизированные волокна Aγ, Aβ и Aα (передающие постуральную, тактильную, давящую и двигательную информацию). [32]
Местные анестетики могут блокировать практически каждый нерв между периферическими нервными окончаниями и центральной нервной системой. Наиболее периферической методикой является местная анестезия кожи или другой поверхности тела. Мелкие и крупные периферические нервы могут быть анестезированы по отдельности (периферическая нервная блокада) или в анатомических нервных пучках (плексусная анестезия). Спинальная анестезия и эпидуральная анестезия сливаются в центральную нервную систему.
Инъекция местных анестетиков часто болезненна. Для уменьшения этой боли можно использовать ряд методов, включая буферизацию раствора бикарбонатом и согревание. [35]
Клинические методы включают:
Специфические стоматологические методы включают в себя:
Метод Вазирани–Акиноси также известен как блокада нижнечелюстного нерва с закрытым ртом. Он в основном используется у пациентов с ограниченным открытием нижней челюсти или у тех, у кого тризм; спазм жевательных мышц. Нервы, которые анестезируются при этом методе, — это нижнеальвеолярный, резцовый, подбородочный, язычный и челюстно-подъязычный нервы.
Стоматологические иглы доступны в двух длинах, короткие и длинные. Поскольку Вазирани–Акиноси является методом местной анестезии, который требует проникновения в значительную толщу мягких тканей, используется длинная игла. Игла вводится в мягкую ткань, которая покрывает медиальный край ветви нижней челюсти, в области нижнего альвеолярного, язычного и челюстно-подъязычного нервов. Расположение скоса иглы очень важно, поскольку он должен быть расположен вдали от кости ветви нижней челюсти и вместо этого по направлению к средней линии. [37]
Интралигаментарная инфильтрация, также известная как инъекция в периодонтальную связку или интралигаментарная инъекция (ILI), известна как «самая универсальная из дополнительных инъекций». ILI обычно вводятся, когда методы блокады нижнего альвеолярного нерва неадекватны или неэффективны. [38] ILI предназначены для:
Ожидается, что использование ВЛЗ увеличится, поскольку пациенты стоматологических клиник предпочитают меньше анестезии мягких тканей, а стоматологи стремятся сократить применение традиционной блокады нижнего альвеолярного нерва (ИНАБ) при рутинных восстановительных процедурах. [40]
Методология инъекции: пространство периодонтальной связки обеспечивает доступный путь к губчатой альвеолярной кости, а анестетик достигает пульпарного нерва через естественную перфорацию внутриротовой костной ткани. [41] [42]
Преимущества ILI перед INAB: быстрое начало действия (в течение 30 секунд), требуется небольшая доза (0,2–1,0 мл), ограниченная область онемения, [43] [44] более низкие внутренние риски, такие как невропатия, гематома, тризм/растяжение челюсти [45] [46] и самоповреждение тканей пародонта, [47] [48], а также снижение сердечно-сосудистых нарушений. [49] Его использование в качестве вторичной или дополнительной анестезии на нижней челюсти показало высокий уровень успеха — более 90%. [50] [51]
Недостатки: риск временного повреждения тканей пародонта, вероятность бактериемии и эндокардита у групп риска, [52] правильное давление и правильное размещение иглы являются обязательными для успешного обезболивания, короткая продолжительность анестезии пульпы ограничивает использование ВЛИ для нескольких восстановительных процедур, которые требуют большей продолжительности, [52] послеоперационный дискомфорт и травмы непрорезавшихся зубов, такие как гипоплазия эмали и дефекты.
Описание техники:
Шприцы:
На что следует обратить внимание:
Техника Гоу-Гейтса используется для анестезии нижней челюсти рта пациента. С помощью внеротовых и внутриротовых ориентиров игла вводится в интраоральную латеро-переднюю поверхность мыщелка, не доходя ниже места прикрепления латеральной крыловидной мышцы. [61] Внеротовыми ориентирами, используемыми для этой техники, являются нижняя граница козелка уха, углы рта и угол козелка на боковой стороне лица. [61]
Биофизические силы (пульсация верхнечелюстной артерии, мышечная функция движения челюсти) и гравитация будут способствовать диффузии анестетика для заполнения всего крыловидно-нижнечелюстного пространства. Все три оральные сенсорные части нижнечелюстной ветви тройничного нерва и другие сенсорные нервы в этой области будут контактировать с анестетиком, и это уменьшит необходимость анестезировать дополнительную иннервацию. [61]
По сравнению с другими региональными методами анестезии нижней челюсти, метод Гоу-Гейтса имеет более высокий уровень успеха в полной анестезии нижней челюсти. Одно исследование показало, что из 1200 пациентов, которым были сделаны инъекции с помощью метода Гоу-Гейтса, только 2 из них не получили полной анестезии. [61]

Растворы местных анестетиков для инъекций обычно состоят из: [62]
Эфиры склонны вызывать аллергические реакции, что может потребовать использования амида . Названия каждого местного клинического анестетика имеют суффикс «-каин». Большинство эфирных МА метаболизируются псевдохолинэстеразой , в то время как амидные МА метаболизируются в печени. Это может быть фактором при выборе агента для пациентов с печеночной недостаточностью, [63] хотя, поскольку холинэстеразы вырабатываются в печени, физиологически (например, очень молодой или очень старый человек) или патологически (например, цирроз ) нарушенный печеночный метаболизм также является фактором при использовании эфиров.
Иногда LA объединяются, например:
Растворы местных анестетиков для инъекций иногда смешивают с вазоконстрикторами ( комбинированный препарат ) для увеличения продолжительности местной анестезии путем сужения кровеносных сосудов, тем самым безопасно концентрируя анестетик в течение длительного времени, а также уменьшая кровотечение . [64] Поскольку вазоконстриктор временно снижает скорость, с которой системный кровоток удаляет местный анестетик из области инъекции, максимальные дозы местных анестетиков при сочетании с вазоконстриктором выше по сравнению с тем же местным анестетиком без какого-либо вазоконстриктора. Иногда для этой цели вводят кокаин. Вот некоторые примеры:
Одним из комбинированных препаратов такого типа является ТАС (5–12% тетракаина , 1/2000 (0,05%, 500 ppm , 1 ⁄ 2 промилле) адреналина, 4 или 10% кокаина), который используется местно для поверхностной анестезии.
Использование местного анестетика с вазоконстриктором безопасно в областях, снабжаемых конечными артериями . Распространенное мнение, что местный анестетик с вазоконстриктором может вызвать некроз конечностей, таких как нос, уши, пальцы рук и ног (из-за сужения конечных артерий), несостоятельно, поскольку ни одного случая некроза не было зарегистрировано с момента появления коммерческого лидокаина с адреналином в 1948 году. [65]
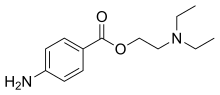

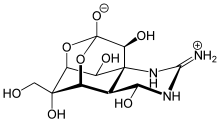
Большинство местных анестетиков природного происхождения, за исключением ментола, эвгенола и кокаина, являются нейротоксинами и имеют в своих названиях суффикс -токсин. Кокаин связывается с внутриклеточной стороной каналов, тогда как сакситоксин, неосакситоксин и тетродотоксин связываются с внеклеточной стороной натриевых каналов.
В Перу древние инки , как полагают, использовали листья растения коки в качестве местного анестетика в дополнение к его стимулирующим свойствам. [66] Он также использовался для оплаты труда рабов и, как полагают, сыграл свою роль в последующем уничтожении культуры инков , когда испанцы осознали последствия жевания листьев коки и воспользовались этим. [66] Кокаин впервые был использован в качестве местного анестетика в 1884 году. Поиск менее токсичной и менее вызывающей привыкание замены привел к разработке аминоэфирных местных анестетиков стоваина в 1903 году и прокаина в 1904 году. С тех пор было разработано и введено в клиническую практику несколько синтетических местных анестетиков, в частности лидокаин в 1943 году, бупивакаин в 1957 году и прилокаин в 1959 году.
Изобретение клинического использования местной анестезии приписывают Венской школе, в которую входили Зигмунд Фрейд (1856-1939), Карл Коллер (1857-1944) и Леопольд Кенигштейн (1850-1942). Они ввели местную анестезию, используя кокаин, посредством «самостоятельных экспериментов» на слизистой оболочке полости рта, прежде чем ввести его в эксперименты на животных или людях. Венская школа впервые начала использовать кокаин в качестве местной анестезии в офтальмологии, и позже он был включен в офтальмологическую практику. Доктор Халстед и доктор Холл в Соединенных Штатах в 1885 году описали метод внутриротовой анестезии, заключающийся в блокировании нижнего альвеолярного нерва и передневерхнего зубного нерва с использованием 4% кокаина.{ [67]
Вскоре после первого использования кокаина для местной анестезии были описаны блокады периферических нервов. Анестезия плечевого сплетения путем чрескожной инъекции через подмышечные и надключичные доступы была разработана в начале 20 века. Поиск наиболее эффективного и наименее травматичного подхода к анестезии сплетения и блокадам периферических нервов продолжается и по сей день. В последние десятилетия непрерывная регионарная анестезия с использованием катетеров и автоматических насосов развилась как метод терапии боли.
Внутривенная регионарная анестезия была впервые описана Августом Биром в 1908 году. Эта методика используется до сих пор и является исключительно безопасной при использовании препаратов с низкой системной токсичностью, таких как прилокаин.
Спинальная анестезия была впервые использована в 1885 году, но не была введена в клиническую практику до 1899 года, когда Август Бир подверг себя клиническому эксперименту, в котором он наблюдал анестезирующий эффект, а также типичный побочный эффект в виде постпункционной головной боли. В течение нескольких лет спинальная анестезия стала широко использоваться для хирургической анестезии и была принята как безопасный и эффективный метод. Хотя сегодня используются атравматические (нережущие кончики) канюли и современные препараты, в остальном эта техника мало изменилась за многие десятилетия.
Эпидуральная анестезия с каудальным подходом была известна еще в начале 20-го века, но четко определенная техника с использованием поясничной инъекции не была разработана до 1921 года, когда Фидель Пажес опубликовал свою статью «Anestesia Metamérica». Эта техника была популяризирована в 1930-х и 1940-х годах Ахиле Марио Дольотти. С появлением тонких, гибких катетеров стали возможны непрерывная инфузия и повторные инъекции, что делает эпидуральную анестезию по-прежнему весьма успешной техникой. Помимо ее многочисленных применений в хирургии, эпидуральная анестезия особенно популярна в акушерстве для лечения родовой боли.
{{cite book}}: |work=проигнорировано ( помощь ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )