Химиотерапия (часто сокращенно химиотерапия , а иногда и CTX или CTx ) — это тип лечения рака , при котором используется один или несколько противораковых препаратов ( химиотерапевтических агентов или алкилирующих агентов ) как часть стандартизированного режима химиотерапии . Химиотерапия может проводиться с лечебной целью (которая почти всегда включает в себя комбинацию препаратов) или может быть направлена на продление жизни или уменьшение симптомов ( паллиативная химиотерапия). Химиотерапия — одна из основных категорий медицинской дисциплины, специально посвященной фармакотерапии рака , которая называется медицинской онкологией . [1] [2]
Термин «химиотерапия» стал означать неспецифическое использование внутриклеточных ядов для ингибирования митоза (деление клеток) или индукции повреждения ДНК , поэтому ингибирование восстановления ДНК может усиливать химиотерапию. [3] Значение слова «химиотерапия» исключает более селективные агенты, которые блокируют внеклеточные сигналы ( передача сигнала ). Разработка методов лечения со специфическими молекулярными или генетическими мишенями, которые подавляют стимулирующие рост сигналы классических эндокринных гормонов (в первую очередь эстрогенов при раке молочной железы и андрогенов при раке простаты), теперь называется гормональной терапией . Напротив, другие ингибиции сигналов роста, например, связанные с рецепторными тирозинкиназами, называются таргетной терапией .
Важно отметить, что использование лекарств (будь то химиотерапия, гормональная терапия или таргетная терапия) представляет собой системную терапию рака, поскольку они вводятся в кровоток и, следовательно, в принципе способны воздействовать на рак в любой анатомической области тела. Системная терапия часто используется в сочетании с другими методами, составляющими местную терапию (т.е. лечением, эффективность которых ограничена анатомической областью, где они применяются) при раке, такими как лучевая терапия , хирургическое вмешательство или гипертермическая терапия .
Традиционные химиотерапевтические агенты цитотоксичны , поскольку препятствуют делению клеток (митозу), но чувствительность раковых клеток к этим агентам сильно различается. В значительной степени химиотерапию можно рассматривать как способ повреждения или стресса клеток, что может затем привести к гибели клеток, если инициируется апоптоз . Многие из побочных эффектов химиотерапии можно объяснить повреждением нормальных клеток, которые быстро делятся и поэтому чувствительны к антимитотическим препаратам: клеток костного мозга , пищеварительного тракта и волосяных фолликулов . Это приводит к наиболее частым побочным эффектам химиотерапии: миелосупрессии (снижению выработки клеток крови, а следовательно, и иммуносупрессии ), мукозиту (воспалению слизистой оболочки пищеварительного тракта) и алопеции (выпадению волос). Из-за воздействия на иммунные клетки (особенно на лимфоциты) химиотерапевтические препараты часто находят применение при множестве заболеваний, возникающих в результате вредной чрезмерной активности иммунной системы против себя (так называемый аутоиммунитет ). К ним относятся ревматоидный артрит , системная красная волчанка , рассеянный склероз , васкулит и многие другие.
Сегодня существует ряд стратегий применения химиотерапевтических препаратов. Химиотерапия может проводиться с лечебной целью или может быть направлена на продление жизни или облегчение симптомов .
Все схемы химиотерапии требуют, чтобы реципиент был способен пройти лечение. Статус работоспособности часто используется в качестве меры для определения того, может ли человек получать химиотерапию или требуется ли снижение дозы. Поскольку только часть клеток опухоли погибает при каждом лечении ( фракционное уничтожение ), необходимо вводить повторные дозы, чтобы продолжать уменьшать размер опухоли. [10] В современных схемах химиотерапии медикаментозное лечение проводится циклами, при этом частота и продолжительность лечения ограничены токсичностью. [11]
Эффективность химиотерапии зависит от типа рака и стадии. Общая эффективность варьируется от излечения при некоторых видах рака, таких как некоторые лейкемии , [12] [13] до неэффективности, например, при некоторых опухолях головного мозга , [14] до бесполезности при других видах рака, например, при большинстве немеланомных видов рака кожи . [15]

Дозировка химиотерапии может быть затруднена: если доза слишком мала, она будет неэффективна против опухоли, тогда как при чрезмерных дозах токсичность ( побочные эффекты ) будет непереносима для человека, получающего ее. [4] Стандартный метод определения дозировки химиотерапии основан на расчете площади поверхности тела (ППТ). BSA обычно рассчитывается с помощью математической формулы или номограммы с использованием веса и роста получателя, а не путем прямого измерения площади тела. Эта формула была первоначально выведена в исследовании 1916 года и представляла попытку перевести лекарственные дозы, установленные для лабораторных животных, в эквивалентные дозы для людей. [16] В исследовании участвовало только девять человек. [17] Когда в 1950-х годах была введена химиотерапия, формула БСА была принята в качестве официального стандарта дозирования химиотерапии из-за отсутствия лучшего варианта. [18] [19]
Достоверность этого метода при расчете единых доз подвергается сомнению, поскольку формула учитывает только вес и рост человека. На абсорбцию и клиренс лекарства влияют множество факторов, включая возраст, пол, обмен веществ, болезненное состояние, функцию органов, взаимодействие лекарств, генетику и ожирение, которые оказывают серьезное влияние на фактическую концентрацию лекарства в кровотоке человека. . [18] [20] [21] В результате наблюдается высокая вариабельность концентрации системных химиотерапевтических препаратов у людей, получающих БСА, и, как было продемонстрировано, эта вариабельность для многих препаратов превышает десять раз. [17] [22] Другими словами, если два человека получают одинаковую дозу данного препарата на основе БСА, концентрация этого препарата в кровотоке одного человека может быть в 10 раз выше или ниже по сравнению с концентрацией этого препарата у другого человека. . [22] Эта вариабельность типична для многих химиотерапевтических препаратов, дозируемых БСА, и, как показано ниже, была продемонстрирована в исследовании 14 распространенных химиотерапевтических препаратов. [17]

Результатом этой фармакокинетической вариабельности среди людей является то, что многие люди не получают правильную дозу, необходимую для достижения оптимальной эффективности лечения с минимизацией токсических побочных эффектов. Некоторые люди получают передозировку, а другие – недостаточную. [18] [20] [21] [23] [24] [25] [26] Например, в рандомизированном клиническом исследовании исследователи обнаружили, что 85% пациентов с метастатическим колоректальным раком, получавших 5-фторурацил (5-ФУ), не не получили оптимальную терапевтическую дозу при дозировке по стандарту BSA — 68% получили недостаточную дозу и 17% — передозировку. [23]
Были разногласия по поводу использования BSA для расчета доз химиотерапии для людей, страдающих ожирением . [27] Из-за более высокого содержания BSA врачи часто произвольно снижают дозу, предписанную по формуле BSA, опасаясь передозировки . [27] Во многих случаях это может привести к неоптимальному лечению. [27]
Несколько клинических исследований показали, что когда дозировка химиотерапии подбирается индивидуально для достижения оптимального системного воздействия препарата, результаты лечения улучшаются, а токсические побочные эффекты уменьшаются. [23] [25] В клиническом исследовании 5-ФУ, упомянутом выше, люди, чья доза была скорректирована для достижения заранее определенного целевого воздействия, отметили улучшение на 84% уровня ответа на лечение и шестимесячное улучшение общей выживаемости (ОВ). по сравнению с теми, кто получал БСА. [23]
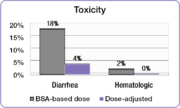
В том же исследовании исследователи сравнили частоту частых проявлений токсичности 3/4 степени, связанной с 5-ФУ, между людьми с корректированной дозой и людьми, получавшими дозы BSA. [23] Частота диареи тяжелой степени снизилась с 18% в группе, принимавшей БСА, до 4% в группе с корректированной дозой, а серьезные гематологические побочные эффекты были устранены. [23] Из-за снижения токсичности пациенты с корректированной дозой могли лечиться в течение более длительных периодов времени. [23] Люди, принимавшие БСА, получали лечение в общей сложности 680 месяцев, тогда как люди в группе с корректированной дозой получали лечение в общей сложности 791 месяц. [23] Завершение курса лечения является важным фактором в достижении лучших результатов лечения.
Аналогичные результаты были получены в исследовании с участием людей с колоректальным раком, которые лечились популярной схемой FOLFOX . [25] Частота возникновения серьезной диареи снизилась с 12% в группе пациентов, принимавших БСА, до 1,7% в группе с корректированной дозой, а частота развития тяжелого мукозита снизилась с 15% до 0,8%. [25]
Исследование FOLFOX также продемонстрировало улучшение результатов лечения. [25] Положительный ответ увеличился с 46% в группе, принимавшей БСА, до 70% в группе с корректированной дозой. Медиана выживаемости без прогрессирования (ВБП) и общая выживаемость (ОВ) улучшились на шесть месяцев в группе с корректированной дозой. [25]
Один из подходов, который может помочь клиницистам индивидуализировать дозировку химиотерапии, заключается в измерении уровней препарата в плазме крови с течением времени и корректировке дозы в соответствии с формулой или алгоритмом для достижения оптимального воздействия. При установленном целевом воздействии для оптимизации эффективности лечения и минимизации токсичности дозировку можно персонализировать для достижения целевого воздействия и оптимальных результатов для каждого человека. Такой алгоритм использовался в упомянутых выше клинических исследованиях и привел к значительному улучшению результатов лечения. [28]
Онкологи уже индивидуализируют дозировку некоторых противораковых препаратов в зависимости от воздействия. Дозирование карбоплатина [29] : 4 и бусульфана [30] [31] зависит от результатов анализов крови для расчета оптимальной дозы для каждого человека. Простые анализы крови также доступны для оптимизации дозы метотрексата , [32] 5-ФУ, паклитаксела и доцетаксела . [33] [34]
Уровень сывороточного альбумина непосредственно перед назначением химиотерапии является независимым прогностическим предиктором выживаемости при различных типах рака. [35]

Алкилирующие агенты являются старейшей группой химиотерапевтических средств, используемых сегодня. Первоначально полученный из горчичного газа, использовавшегося во время Первой мировой войны , в настоящее время используется множество типов алкилирующих агентов. [4] Они названы так из-за своей способности алкилировать многие молекулы, включая белки , РНК и ДНК . Эта способность ковалентно связываться с ДНК через алкильную группу является основной причиной их противоракового действия. [37] ДНК состоит из двух цепей, и молекулы могут либо дважды связываться с одной цепью ДНК (внутрицепочечная сшивка), либо могут связываться один раз с обеими цепями (межцепочечная сшивка). Если клетка пытается реплицировать сшитую ДНК во время деления клетки или пытается ее восстановить, нити ДНК могут порваться. Это приводит к форме запрограммированной гибели клеток, называемой апоптозом . [36] [38] Алкилирующие агенты действуют в любой точке клеточного цикла и поэтому известны как препараты, независимые от клеточного цикла. По этой причине воздействие на клетку зависит от дозы; доля погибающих клеток прямо пропорциональна дозе препарата. [39]
Подтипами алкилирующих агентов являются азотистые иприты , нитрозомочевины , тетразины , азиридины , [40] цисплатины и их производные, а также неклассические алкилирующие агенты. Азотистые иприты включают мехлоретамин , циклофосфамид , мелфалан , хлорамбуцил , ифосфамид и бусульфан . Нитрозомочевины включают N-нитрозо-N-метилмочевину (MNU), кармустин (BCNU), ломустин (CCNU) и семустин (MeCCNU), фотемустин и стрептозотоцин . К тетразинам относятся дакарбазин , митозоломид и темозоломид . К азиридинам относятся тиотепа , митомицин и диазиквон (AZQ). Цисплатин и производные включают цисплатин , карбоплатин и оксалиплатин . [37] [38] Они нарушают функцию клеток, образуя ковалентные связи с амино , карбоксильными , сульфгидрильными и фосфатными группами в биологически важных молекулах. [41] Неклассические алкилирующие агенты включают прокарбазин и гексаметилмеламин. [37] [38]

Антиметаболиты — это группа молекул, которые препятствуют синтезу ДНК и РНК. Многие из них имеют структуру, аналогичную строительным блокам ДНК и РНК. Строительными блоками являются нуклеотиды ; молекула, содержащая азотистое основание , сахар и фосфатную группу . Нуклеиновые основания делятся на пурины ( гуанин и аденин ) и пиримидины ( цитозин , тимин и урацил ). Антиметаболиты напоминают либо азотистые основания, либо нуклеозиды (нуклеотиды без фосфатной группы), но имеют измененные химические группы . [42] Эти препараты оказывают свое действие либо блокируя ферменты, необходимые для синтеза ДНК, либо встраиваясь в ДНК или РНК. Ингибируя ферменты, участвующие в синтезе ДНК, они предотвращают митоз, поскольку ДНК не может дублировать себя. Кроме того, после неправильного включения молекул в ДНК может произойти повреждение ДНК и индуцироваться запрограммированная гибель клеток ( апоптоз ). В отличие от алкилирующих агентов, антиметаболиты зависят от клеточного цикла. Это означает, что они работают только во время определенной части клеточного цикла, в данном случае S-фазы (фазы синтеза ДНК). По этой причине при определенной дозе эффект выходит на плато, и при увеличении дозы гибель клеток пропорционально прекращается. Подтипами антиметаболитов являются антифолаты , фторпиримидины, аналоги дезоксинуклеозидов и тиопурины . [37] [42]
К антифолатам относятся метотрексат и пеметрексед . Метотрексат ингибирует дигидрофолатредуктазу (ДГФР), фермент, который регенерирует тетрагидрофолат из дигидрофолата . Когда фермент ингибируется метотрексатом, клеточные уровни фолат-коэнзимов снижаются. Они необходимы для производства тимидилата и пурина, которые необходимы для синтеза ДНК и деления клеток. [6] : 55–59 [7] : 11 Пеметрексед – еще один антиметаболит, влияющий на выработку пуринов и пиримидинов и, следовательно, также ингибирующий синтез ДНК. Он в первую очередь ингибирует фермент тимидилатсинтазу , но также оказывает воздействие на DHFR, аминоимидазолкарбоксамидрибонуклеотидформилтрансферазу и глицинамидрибонуклеотидформилтрансферазу . [43] Фторпиримидины включают фторурацил и капецитабин . Фторурацил представляет собой аналог нуклеиновых оснований, который метаболизируется в клетках с образованием как минимум двух активных продуктов; 5-фторуридинмонофосфат (FUMP) и 5-фтор-2'-дезоксиуридин-5'-фосфат (fdUMP). FUMP включается в РНК, а fdUMP ингибирует фермент тимидилатсинтазу; оба из которых приводят к гибели клеток. [7] : 11 Капецитабин представляет собой пролекарство 5-фторурацила, которое расщепляется в клетках с образованием активного препарата. [44] Аналоги дезоксинуклеозидов включают цитарабин , гемцитабин , децитабин , азацитидин , флударабин , неларабин , кладрибин , клофарабин и пентостатин . К тиопуринам относятся тиогуанин и меркаптопурин . [37] [42]

Антимикротрубочковые агенты — это химические вещества растительного происхождения, которые блокируют деление клеток, препятствуя функционированию микротрубочек . Микротрубочки представляют собой важную клеточную структуру, состоящую из двух белков: α-тубулина и β-тубулина . Это полые структуры в форме стержней, которые, помимо других клеточных функций, необходимы для деления клеток. [45] Микротрубочки представляют собой динамические структуры, а это означает, что они постоянно находятся в состоянии сборки и разборки. Алкалоиды барвинка и таксаны представляют собой две основные группы антимикротрубочковых агентов, и хотя обе эти группы препаратов вызывают дисфункцию микротрубочек, механизмы их действия совершенно противоположны: алкалоиды барвинка предотвращают сборку микротрубочек, тогда как таксаны предотвращают их разборку. Поступая таким образом, они могут вызвать митотическую катастрофу в раковых клетках. [46] После этого происходит остановка клеточного цикла, что вызывает запрограммированную гибель клеток ( апоптоз ). [37] [47] Эти препараты также могут влиять на рост кровеносных сосудов — важный процесс, который опухоли используют для роста и метастазирования. [47]
Алкалоиды барвинка получают из мадагаскарского барвинка Catharanthus Roseus , [48] [49], ранее известного как Vinca rosea . Они связываются со специфическими участками тубулина, ингибируя сборку тубулина в микротрубочки. Оригинальные алкалоиды барвинка представляют собой натуральные продукты , в состав которых входят винкристин и винбластин . [50] [51] [52] [53] После успеха этих препаратов были произведены полусинтетические алкалоиды барвинка : винорелбин (используется при лечении немелкоклеточного рака легких [52] [54] [55] ), виндезин и винфлунин . [47] Эти препараты специфичны для клеточного цикла . Они связываются с молекулами тубулина в S-фазе и предотвращают правильное образование микротрубочек, необходимое для М-фазы . [39]
Таксаны – природные и полусинтетические препараты. Первый препарат этого класса, паклитаксел , первоначально был извлечен из Taxus brevifolia , тиса тихоокеанского. Теперь этот препарат и еще один препарат этого класса, доцетаксел , производятся полусинтетически из химического вещества, обнаруженного в коре другого тиса, Taxus baccata . [56]
Подофиллотоксин представляет собой противоопухолевый лигнан , полученный в основном из американского майского яблока ( Podophyllum peltatum ) и гималайского майского яблока ( Sinopodophyllum hexandrum ). Он обладает антимикротрубочковой активностью, и его механизм аналогичен механизму действия алкалоидов барвинка в том смысле, что они связываются с тубулином, ингибируя образование микротрубочек. Подофиллотоксин используется для производства двух других препаратов с разными механизмами действия: этопозида и тенипозида . [57] [58]

Ингибиторы топоизомеразы — препараты, влияющие на активность двух ферментов: топоизомеразы I и топоизомеразы II . Когда двухцепочечная спираль ДНК раскручивается, например, во время репликации или транскрипции ДНК , соседняя нераскрытая ДНК скручивается туже (суперспирали), как размыкание середины витой веревки. Стрессу, вызванному этим эффектом, частично способствуют ферменты топоизомеразы. Они производят одно- или двухцепочечные разрывы ДНК, уменьшая напряжение в цепи ДНК. Это позволяет нормальному раскручиванию ДНК происходить во время репликации или транскрипции. Ингибирование топоизомеразы I или II препятствует обоим этим процессам. [59] [60]
Два ингибитора топоизомеразы I, иринотекан и топотекан , полусинтетически получены из камптотецина , который получают из китайского декоративного дерева Camptotheca acuminata . [39] Препараты, нацеленные на топоизомеразу II, можно разделить на две группы. Яды топоизомеразы II вызывают повышение уровня ферментов, связанных с ДНК. Это предотвращает репликацию и транскрипцию ДНК, вызывает разрывы цепей ДНК и приводит к запрограммированной гибели клеток ( апоптозу ). Эти агенты включают этопозид , доксорубицин , митоксантрон и тенипозид . Вторая группа, каталитические ингибиторы, представляет собой препараты, которые блокируют активность топоизомеразы II и, следовательно, предотвращают синтез и трансляцию ДНК, поскольку ДНК не может раскручиваться должным образом. В эту группу входят новобиоцин , мербарон и акларубицин , которые также обладают другими важными механизмами действия. [61]
Цитотоксические антибиотики представляют собой разнообразную группу препаратов, имеющих различные механизмы действия. Общая тема, которую они разделяют в своих показаниях к химиотерапии, заключается в том, что они прерывают деление клеток . Наиболее важной подгруппой являются антрациклины и блеомицины ; другие известные примеры включают митомицин С и актиномицин . [62]
Среди антрациклинов первыми были доксорубицин и даунорубицин , полученные из бактерии Streptomyces peucetius . [63] Производные этих соединений включают эпирубицин и идарубицин . Другими клинически используемыми препаратами из группы антрациклинов являются пирарубицин , акларубицин и митоксантрон . [64] Механизмы действия антрациклинов включают интеркаляцию ДНК (молекулы вставляются между двумя нитями ДНК), генерацию высокореактивных свободных радикалов , которые повреждают межклеточные молекулы и ингибирование топоизомеразы. [65]
Актиномицин представляет собой сложную молекулу, которая интеркалирует ДНК и предотвращает синтез РНК . [66]
Блеомицин, гликопептид , выделенный из Streptomyces verticillus , также интеркалирует ДНК, но производит свободные радикалы , которые повреждают ДНК. Это происходит, когда блеомицин связывается с ионом металла , химически восстанавливается и реагирует с кислородом . [67] [6] : 87
Митомицин — цитотоксический антибиотик, способный алкилировать ДНК. [68]

Большая часть химиотерапии проводится внутривенно , хотя ряд препаратов можно назначать перорально (например, мелфалан , бусульфан , капецитабин ). Согласно недавнему (2016 г.) систематическому обзору, пероральная терапия создает дополнительные проблемы для пациентов и медицинских работников, связанные с поддержанием и поддержкой соблюдения планов лечения. [69]
Существует множество внутривенных методов доставки лекарств, известных как устройства сосудистого доступа. К ним относятся крылатое инфузионное устройство , периферический венозный катетер , срединный катетер, периферически вводимый центральный катетер (PICC), центральный венозный катетер и имплантируемый порт . Устройства имеют различное применение в зависимости от продолжительности химиотерапевтического лечения, способа доставки и типов химиотерапевтического агента. [7] : 94–95
В зависимости от человека, рака, стадии рака, типа химиотерапии и дозировки внутривенная химиотерапия может проводиться как в стационаре, так и амбулаторно . Для непрерывного, частого или длительного внутривенного введения химиотерапии в сосудистую сеть можно хирургическим путем вводить различные системы для поддержания доступа. [7] : 113–118 Обычно используемые системы — линия Хикмана , линия Port-a-Cath и линия PICC . Они имеют меньший риск заражения, гораздо менее склонны к флебиту или экстравазации и устраняют необходимость повторного введения периферических канюль. [70]
Изолированная перфузия конечностей (часто используемая при меланоме ) [71] или изолированная инфузия химиопрепаратов в печень [72] или легкие использовались для лечения некоторых опухолей. Основная цель этих подходов — доставить очень высокую дозу химиотерапии к опухолевым участкам, не вызывая при этом подавляющего системного повреждения. [73] Эти подходы могут помочь контролировать одиночные или ограниченные метастазы, но они по определению не являются системными и, следовательно, не лечат распределенные метастазы или микрометастазы . [ нужна цитата ]
Местная химиотерапия, такая как 5-фторурацил , используется для лечения некоторых случаев немеланомного рака кожи . [74]
Если рак поражает центральную нервную систему или сопровождается поражением мозговых оболочек, можно назначить интратекальную химиотерапию. [4]
Химиотерапевтические методы имеют ряд побочных эффектов, которые зависят от типа используемых лекарств. Наиболее распространенные лекарства воздействуют главным образом на быстро делящиеся клетки организма, такие как клетки крови и клетки, выстилающие ротовую полость, желудок и кишечник. Токсичность, связанная с химиотерапией, может возникать остро после введения, в течение нескольких часов или дней, или хронически, от недель до лет. [6] : 265
Практически все химиотерапевтические схемы могут вызвать депрессию иммунной системы , часто парализуя костный мозг и приводя к уменьшению количества лейкоцитов , эритроцитов и тромбоцитов .Анемия и тромбоцитопения могут потребовать переливания крови . Нейтропению (снижение количества нейтрофильных гранулоцитов ниже 0,5 х 10 9 / л ) можно уменьшить с помощью синтетического Г-КСФ ( гранулоцитарно -колониестимулирующего фактора, например, филграстима , ленограстима , эфбемаленограстима альфа ). [75]
При очень тяжелой миелосупрессии , которая возникает при некоторых схемах лечения, почти все стволовые клетки костного мозга (клетки, продуцирующие белые и красные кровяные тельца ) разрушаются, что означает необходимость трансплантации аллогенных или аутологичных клеток костного мозга . (При аутологичной ТКМ клетки удаляются у человека перед лечением, размножаются, а затем вводятся повторно; при аллогенной ТКМ источником является донор.) Однако у некоторых людей по-прежнему развиваются заболевания из-за такого воздействия на костный мозг. [76]
Хотя людям, получающим химиотерапию, рекомендуется мыть руки, избегать больных людей и предпринимать другие меры по снижению инфекций, около 85% инфекций вызваны естественными микроорганизмами в собственном желудочно-кишечном тракте человека (включая полость рта ) и на коже. [77] : 130 Это может проявляться как системные инфекции, такие как сепсис , или как локализованные вспышки, такие как простой герпес , опоясывающий лишай или другие представители Herpesviridea . [78] Риск заболевания и смерти можно снизить, принимая обычные антибиотики, такие как хинолоны или триметоприм/сульфаметоксазол, до появления лихорадки или признаков инфекции. [79] Хинолоны показывают эффективную профилактику главным образом гематологического рака. [79] Однако в целом из каждых пяти человек с иммуносупрессией после химиотерапии, принимающих антибиотики, можно предотвратить одну лихорадку; из каждых 34 человек, принимающих антибиотики, можно предотвратить одну смерть. [79] Иногда химиотерапию откладывают, поскольку иммунная система подавлена до критически низкого уровня. [ нужна цитата ]
В Японии правительство одобрило использование некоторых лекарственных грибов, таких как Trametes versicolor , для противодействия депрессии иммунной системы у людей, проходящих химиотерапию. [80]
Трилациклиб — ингибитор циклинзависимой киназы 4/6, одобренный для профилактики миелосупрессии, вызванной химиотерапией. Препарат назначают перед химиотерапией для защиты функции костного мозга. [81]
Из-за подавления иммунной системы нейтропенический энтероколит (тифлит) является «опасным для жизни желудочно-кишечным осложнением химиотерапии». [82] Тифлит — это кишечная инфекция, которая может проявляться такими симптомами, как тошнота , рвота , диарея , вздутие живота , лихорадка , озноб или боль и болезненность в животе. [83]
Тифлит требует неотложной медицинской помощи . Оно имеет очень плохой прогноз и часто приводит к летальному исходу, если его не своевременно распознать и не начать агрессивное лечение. [84] Успешное лечение зависит от ранней диагностики, обеспечиваемой высоким индексом подозрительности и использования компьютерной томографии, консервативного лечения в неосложненных случаях и иногда плановой правосторонней гемиколэктомии для предотвращения рецидива. [84]
Тошнота , рвота , анорексия , диарея , спазмы в животе и запор являются частыми побочными эффектами химиотерапевтических препаратов, которые убивают быстроделящиеся клетки. [85] Недоедание и обезвоживание могут возникнуть, когда получатель не ест и не пьет достаточно, или когда человека часто рвет из-за желудочно-кишечного повреждения. Это может привести к быстрой потере веса, а иногда и к его увеличению, если человек ест слишком много, пытаясь облегчить тошноту или изжогу. Увеличение веса также может быть вызвано приемом некоторых стероидных препаратов. Эти побочные эффекты часто можно уменьшить или устранить с помощью противорвотных препаратов. Доказательства низкой определенности также позволяют предположить, что пробиотики могут оказывать профилактическое и лечебное действие при диарее, связанной с применением только химиотерапии и лучевой терапии. [86] Тем не менее, высокий индекс подозрений уместен, поскольку диарея и вздутие живота также являются симптомами тифлита , очень серьезного и потенциально опасного для жизни состояния , требующего немедленного лечения. [87]
Анемия может быть комбинированным исходом, вызванным миелосупрессивной химиотерапией и возможными причинами, связанными с раком, такими как кровотечение , разрушение клеток крови ( гемолиз ), наследственное заболевание, дисфункция почек, дефицит питательных веществ или анемия хронических заболеваний . Лечение анемии включает гормоны для повышения выработки крови ( эритропоэтин ), препараты железа и переливание крови . [88] [89] [90] Миелосупрессивная терапия может вызвать склонность к кровотечениям, что приводит к анемии. Лекарства, которые убивают быстро делящиеся клетки или клетки крови, могут уменьшить количество тромбоцитов в крови, что может привести к синякам и кровотечениям . Чрезвычайно низкое количество тромбоцитов можно временно повысить с помощью переливания тромбоцитов , и разрабатываются новые препараты для увеличения количества тромбоцитов во время химиотерапии. [91] [92] [93] [94] Иногда химиотерапию откладывают, чтобы дать возможность восстановиться количеству тромбоцитов.
Усталость может быть следствием рака или его лечения и может сохраняться от месяцев до лет после лечения. Одной из физиологических причин усталости является анемия, которая может быть вызвана химиотерапией, хирургическим вмешательством , лучевой терапией , первичными и метастатическими заболеваниями или истощением питательных веществ. [95] [96] Было обнаружено, что аэробные упражнения полезны для снижения утомляемости у людей с солидными опухолями . [97]
Тошнота и рвота являются двумя наиболее опасными побочными эффектами, связанными с лечением рака, для людей, больных раком, и их семей. В 1983 году Коутс и др. обнаружили, что люди, получающие химиотерапию, считали тошноту и рвоту первым и вторым наиболее серьезными побочными эффектами соответственно. [98] До 20% людей, получавших в то время высокоэметогенные препараты, откладывали или даже отказывались от потенциально радикального лечения. [99] Тошнота и рвота, вызванные химиотерапией (CINV), часто встречаются при многих методах лечения и некоторых формах рака. С 1990-х годов было разработано и коммерциализировано несколько новых классов противорвотных средств , которые стали почти универсальным стандартом в схемах химиотерапии и помогли успешно справиться с этими симптомами у многих людей. Эффективное устранение этих неприятных, а иногда и изнурительных симптомов приводит к повышению качества жизни реципиента и более эффективным циклам лечения благодаря меньшему количеству перерывов в лечении из-за лучшей переносимости и улучшения общего состояния здоровья. [100]

Выпадение волос (алопеция) может быть вызвано химиотерапией, которая убивает быстро делящиеся клетки; другие лекарства могут привести к истончению волос. Чаще всего это временные эффекты: волосы обычно начинают расти через несколько недель после последней процедуры, но иногда с изменением цвета, текстуры, толщины или стиля. Иногда волосы имеют тенденцию скручиваться после отрастания, что приводит к «химическим завиткам». Сильная потеря волос чаще всего возникает при приеме таких препаратов, как доксорубицин , даунорубицин , паклитаксел , доцетаксел , циклофосфамид , ифосфамид и этопозид . Некоторые стандартные схемы химиотерапии могут привести к необратимому истончению или выпадению волос. [101]
Выпадение волос, вызванное химиотерапией, происходит по неандрогенному механизму и может проявляться в виде тотальной алопеции , телогеновой алопеции или, реже, очаговой алопеции . [102] Обычно оно связано с системным лечением из-за высокой скорости митоза волосяных фолликулов и более обратимо, чем андрогенное выпадение волос, [103] [104] , хотя могут встречаться и необратимые случаи. [105] Химиотерапия вызывает выпадение волос у женщин чаще, чем у мужчин. [106]
Охлаждение кожи головы позволяет предотвратить как постоянное, так и временное выпадение волос; однако были высказаны опасения по поводу этого метода. [107] [108]
Возможно развитие вторичной неоплазии после успешного лечения химиотерапией или лучевой терапией. Наиболее частым вторичным новообразованием является вторичный острый миелолейкоз, развивающийся преимущественно после лечения алкилирующими средствами или ингибиторами топоизомеразы. [109] Вероятность развития вторичного новообразования в течение 30 лет после лечения у людей, перенесших детский рак, более чем в 13 раз выше , чем у населения в целом. [110] Не все это увеличение можно объяснить химиотерапией.
Некоторые виды химиотерапии гонадотоксичны и могут вызвать бесплодие . [111] Химиотерапия с высоким риском включает прокарбазин и другие алкилирующие препараты, такие как циклофосфамид, ифосфамид, бусульфан, мелфалан, хлорамбуцил и хлорметин. [111] К препаратам среднего риска относятся доксорубицин и аналоги платины, такие как цисплатин и карбоплатин. [111] С другой стороны, методы лечения с низким риском гонадотоксичности включают производные растений, такие как винкристин и винбластин, антибиотики , такие как блеомицин и дактиномицин, и антиметаболиты, такие как метотрексат, меркаптопурин и 5-фторурацил. [111]
Женское бесплодие вследствие химиотерапии, по-видимому, является вторичным по отношению к преждевременной недостаточности яичников из-за потери примордиальных фолликулов . [112] Эта потеря не обязательно является прямым эффектом химиотерапевтических агентов, но может быть связана с увеличением скорости начала роста для замены поврежденных развивающихся фолликулов. [112]
Люди могут выбирать между несколькими методами сохранения фертильности перед химиотерапией, включая криоконсервацию спермы, ткани яичников, ооцитов или эмбрионов. [113] Поскольку более половины больных раком — пожилые люди, этот побочный эффект актуален только для меньшинства пациентов. Исследование, проведенное во Франции в период с 1999 по 2011 год, показало, что замораживание эмбрионов перед введением гонадотоксических агентов самкам вызывало задержку лечения в 34% случаев, а рождение живого ребенка - в 27% выживших случаев, которые хотели забеременеть, при этом продолжительность наблюдения варьируется от 1 до 13 лет. [114]
Потенциальные защитные или ослабляющие агенты включают аналоги ГнРГ , некоторые исследования показали защитный эффект in vivo на людях, но некоторые исследования не показывают такого эффекта. Сфингозин-1-фосфат (S1P) продемонстрировал аналогичный эффект, но его механизм ингибирования пути апоптоза сфингомиелина может также влиять на апоптозное действие химиотерапевтических препаратов. [115]
В ходе исследования химиотерапии в качестве режима кондиционирования при трансплантации гемопоэтических стволовых клеток исследование людей, получавших только циклофосфамид по поводу тяжелой апластической анемии, показало, что восстановление яичников произошло у всех женщин моложе 26 лет на момент трансплантации, но только у пяти из 16. женщины старше 26 лет. [116]
Химиотерапия тератогенна во время беременности , особенно в первом триместре , до такой степени, что обычно рекомендуется аборт , если беременность в этот период обнаруживается во время химиотерапии. [117] Воздействие во втором и третьем триместре обычно не увеличивает тератогенный риск и неблагоприятное воздействие на когнитивное развитие, но может увеличить риск различных осложнений беременности и миелосупрессии плода. [117]
У мужчин, ранее проходивших химиотерапию или лучевую терапию, у их детей, зачатых после терапии, не наблюдается увеличения генетических дефектов или врожденных пороков развития. [117] Использование вспомогательных репродуктивных технологий и методов микроманипуляции может увеличить этот риск. [117] У женщин, ранее прошедших химиотерапию, частота выкидышей и врожденных пороков развития не увеличивается при последующих зачатиях. [117] Однако, когда экстракорпоральное оплодотворение и криоконсервация эмбрионов практикуются между лечением или вскоре после него, существуют возможные генетические риски для растущих ооцитов, и поэтому рекомендуется проводить скрининг младенцев. [117]
От 30 до 40 процентов людей, проходящих химиотерапию, страдают периферической невропатией, вызванной химиотерапией (CIPN), прогрессирующим, стойким и часто необратимым состоянием, вызывающим боль, покалывание, онемение и чувствительность к холоду, начиная с рук и ног и иногда прогрессируя до руки и ноги. [118] Химиотерапевтические препараты, связанные с CIPN, включают талидомид , эпотилоны , алкалоиды барвинка , таксаны, ингибиторы протеасом и препараты на основе платины. [118] [119] Возникает ли CIPN и в какой степени определяется выбором препарата, длительностью применения, общим потребляемым количеством и наличием у человека уже периферической невропатии . Хотя симптомы в основном сенсорные, в некоторых случаях поражаются двигательные нервы и вегетативная нервная система . [120] CIPN часто следует за первой дозой химиотерапии и усиливается по мере продолжения лечения, но это прогрессирование обычно выравнивается по завершении лечения. Препараты на основе платины являются исключением; при применении этих препаратов чувствительность может продолжать ухудшаться в течение нескольких месяцев после окончания лечения. [121] Некоторые CIPN кажутся необратимыми. [121] Боль часто можно контролировать с помощью лекарств или других методов лечения, но онемение обычно не поддается лечению. [122]
Некоторые люди, получающие химиотерапию, сообщают об усталости или неспецифических нейрокогнитивных проблемах, таких как неспособность сосредоточиться; это иногда называют когнитивным нарушением после химиотерапии , которое в популярных и социальных сетях называют «химиомозгом». [123]
При особенно крупных опухолях и раковых заболеваниях с высоким количеством лейкоцитов , таких как лимфомы , тератомы и некоторые лейкозы , у некоторых людей развивается синдром лизиса опухоли . Быстрое разрушение раковых клеток приводит к высвобождению химических веществ изнутри клеток. После этого в крови обнаруживается высокий уровень мочевой кислоты , калия и фосфатов . Высокие уровни фосфатов вызывают вторичный гипопаратиреоз, что приводит к снижению уровня кальция в крови. [124] Это вызывает повреждение почек, а высокий уровень калия может вызвать сердечную аритмию . Хотя профилактика доступна и ее часто начинают у людей с большими опухолями, это опасный побочный эффект, который может привести к смерти, если его не лечить. [7] : 202
Кардиотоксичность (поражение сердца) особенно выражена при применении антрациклиновых препаратов ( доксорубицин , эпирубицин , идарубицин и липосомальный доксорубицин ). Причина этого, скорее всего, связана с выработкой свободных радикалов в клетке и последующим повреждением ДНК . Другими химиотерапевтическими агентами, которые вызывают кардиотоксичность, но с меньшей частотой, являются циклофосфамид , доцетаксел и клофарабин . [125]
Гепатотоксичность (поражение печени) могут вызывать многие цитотоксические препараты. Восприимчивость человека к повреждению печени может быть изменена другими факторами, такими как сам рак, вирусный гепатит , иммуносупрессия и дефицит питания . Поражение печени может включать повреждение клеток печени, печеночный синусоидальный синдром (обструкция вен печени), холестаз (когда желчь не течет из печени в кишечник) и фиброз печени . [126] [127]
Нефротоксичность (поражение почек) может быть вызвана синдромом лизиса опухоли , а также прямым эффектом клиренса препарата почками. Различные препараты поражают разные части почек, и токсичность может протекать бессимптомно (выявляться только при анализах крови или мочи) или может вызвать острое повреждение почек . [128] [129]
Ототоксичность (повреждение внутреннего уха) — распространенный побочный эффект препаратов на основе платины, который может вызывать такие симптомы, как головокружение и головокружение . [130] [131] Было обнаружено, что дети, получавшие аналоги платины, подвергаются риску развития потери слуха. [132] [133] [134]
Менее распространенные побочные эффекты включают покраснение кожи ( эритема ), сухость кожи, повреждение ногтей, сухость во рту ( ксеростомия ), задержку жидкости и половое бессилие . Некоторые лекарства могут вызывать аллергические или псевдоаллергические реакции.
Специфические химиотерапевтические агенты связаны с органоспецифической токсичностью, включая сердечно-сосудистые заболевания (например, доксорубицин ), интерстициальные заболевания легких (например, блеомицин ) и иногда вторичные новообразования (например, терапия MOPP при болезни Ходжкина). [135]
Синдром «ладонь-нога» — еще один побочный эффект цитотоксической химиотерапии. [136]
Проблемы с питанием также часто наблюдаются у онкологических больных при постановке диагноза и во время химиотерапии. Исследования показывают, что у детей и молодых людей, проходящих лечение рака, парентеральное питание может помочь в этом, что приводит к увеличению веса и увеличению потребления калорий и белка по сравнению с энтеральным питанием. [137]
Химиотерапия не всегда эффективна, и даже если она полезна, она не может полностью уничтожить рак. Люди часто не понимают его ограничений. В одном исследовании людей, у которых недавно был диагностирован неизлечимый рак четвертой стадии , более двух третей людей с раком легких и более четырех пятых людей с колоректальным раком все еще считали, что химиотерапия может вылечить их рак. [138]
Гематоэнцефалический барьер препятствует доставке химиотерапии в мозг . Это связано с тем, что в мозге имеется обширная система защиты от вредных химических веществ. Транспортеры лекарств могут выкачивать лекарства из мозга и клеток кровеносных сосудов головного мозга в спинномозговую жидкость и кровообращение. Эти транспортеры выкачивают большинство химиотерапевтических препаратов, что снижает их эффективность при лечении опухолей головного мозга. Только небольшие липофильные алкилирующие агенты , такие как ломустин или темозоломид , способны преодолевать этот гематоэнцефалический барьер. [139] [140] [141]
Кровеносные сосуды в опухолях сильно отличаются от сосудов в нормальных тканях. По мере роста опухоли опухолевые клетки, наиболее удаленные от кровеносных сосудов, теряют кислород ( гипоксия ). Чтобы противодействовать этому, они сигнализируют о росте новых кровеносных сосудов. Новообразованная сосудистая сеть опухоли сформирована плохо и не обеспечивает адекватного кровоснабжения всех участков опухоли. Это приводит к проблемам с доставкой лекарств, поскольку многие лекарства будут доставляться в опухоль через систему кровообращения . [142]
Резистентность является основной причиной неудач лечения химиотерапевтическими препаратами. Существует несколько возможных причин резистентности рака, одна из которых — наличие небольших насосов на поверхности раковых клеток, которые активно перемещают химиотерапию изнутри клетки наружу. Раковые клетки производят большое количество этих насосов, известных как p-гликопротеин , чтобы защитить себя от химиотерапии. В настоящее время продолжаются исследования p-гликопротеина и других подобных химиотерапевтических насосов. Лекарства, ингибирующие функцию р-гликопротеина, находятся в стадии исследования, но из-за токсичности и взаимодействия с противораковыми препаратами их разработка затруднена. [143] [144] Другим механизмом устойчивости является амплификация гена , процесс, при котором раковые клетки продуцируют несколько копий гена. Это преодолевает эффект препаратов, снижающих экспрессию генов, участвующих в репликации. При наличии большего количества копий гена препарат не может предотвратить всю экспрессию гена, и, следовательно, клетка может восстановить свою пролиферативную способность. Раковые клетки также могут вызывать дефекты клеточных путей апоптоза (запрограммированной гибели клеток). Поскольку большинство химиотерапевтических препаратов убивают раковые клетки таким образом, дефектный апоптоз позволяет этим клеткам выжить, делая их устойчивыми. Многие химиотерапевтические препараты также вызывают повреждения ДНК, которые могут быть устранены ферментами в клетке, осуществляющими восстановление ДНК . Повышение регуляции этих генов может преодолеть повреждение ДНК и предотвратить индукцию апоптоза. Могут возникнуть мутации в генах, которые производят белки-мишени для лекарств, такие как тубулин , которые препятствуют связыванию лекарств с белком, что приводит к устойчивости к этим типам лекарств. [145] Лекарства, используемые в химиотерапии, могут вызывать клеточный стресс, который может убить раковую клетку; однако при определенных условиях стресс клеток может вызвать изменения в экспрессии генов, что обеспечивает устойчивость к нескольким типам лекарств. [146] Считается, что при раке легких транскрипционный фактор NFκB играет роль в устойчивости к химиотерапии через воспалительные пути. [147] [148] [149]
Таргетная терапия — это относительно новый класс лекарств от рака, который может решить многие проблемы, возникающие при использовании цитотоксических препаратов. Их разделяют на две группы: малые молекулы и антитела. Массивная токсичность, наблюдаемая при использовании цитотоксических препаратов, обусловлена отсутствием клеточной специфичности препаратов. Они убьют любую быстро делящуюся клетку, опухолевую или нормальную. Таргетная терапия предназначена для воздействия на клеточные белки или процессы, которые используются раковыми клетками. [150] Это позволяет воздействовать высокой дозой на раковые ткани при относительно низкой дозе на другие ткани. Хотя побочные эффекты часто менее серьезные, чем у цитотоксических химиотерапевтических препаратов, могут возникнуть опасные для жизни последствия. Первоначально предполагалось, что таргетная терапия будет селективной только в отношении одного белка. Теперь ясно, что зачастую существует целый ряд белковых мишеней, с которыми может связываться лекарство. Примером мишени для таргетной терапии является белок BCR-ABL1, продуцируемый филадельфийской хромосомой , генетическое повреждение, обычно встречающееся при хроническом миелогенном лейкозе и у некоторых пациентов с острым лимфобластным лейкозом . Этот слитый белок обладает ферментной активностью, которую можно ингибировать иматинибом , низкомолекулярным препаратом . [151] [152] [153] [154]

Рак – это неконтролируемый рост клеток в сочетании со злокачественным поведением: инвазией и метастазированием (среди других особенностей). [155] Это вызвано взаимодействием генетической предрасположенности и факторов окружающей среды. [156] [157] Эти факторы приводят к накоплению генетических мутаций в онкогенах (генах, которые контролируют скорость роста клеток) и генах-супрессорах опухолей (генах, которые помогают предотвратить рак), что придает раковым клеткам их злокачественные характеристики, такие как неконтролируемая рост. [158] : 93–94
В широком смысле большинство химиотерапевтических препаратов действуют, нарушая митоз ( деление клеток ), эффективно воздействуя на быстро делящиеся клетки . Поскольку эти препараты повреждают клетки, их называют цитотоксическими . Они предотвращают митоз с помощью различных механизмов, включая повреждение ДНК и ингибирование клеточного механизма, участвующего в делении клеток. [39] [159] Одна из теорий, почему эти препараты убивают раковые клетки, заключается в том, что они вызывают запрограммированную форму гибели клеток, известную как апоптоз . [160]
Поскольку химиотерапия влияет на деление клеток, опухоли с высокими темпами роста (такие как острый миелогенный лейкоз и агрессивные лимфомы , включая болезнь Ходжкина ) более чувствительны к химиотерапии, поскольку большая часть клеток-мишеней подвергается клеточному делению в любое время. Злокачественные новообразования с более медленными темпами роста, такие как индолентные лимфомы, как правило, реагируют на химиотерапию гораздо скромнее. [4] Гетерогенные опухоли также могут проявлять различную чувствительность к химиотерапевтическим агентам, в зависимости от субклональных популяций внутри опухоли. [161]
Клетки иммунной системы также вносят решающий вклад в противоопухолевый эффект химиотерапии. [162] Например, химиотерапевтические препараты оксалиплатин и циклофосфамид могут вызывать гибель опухолевых клеток способом, который обнаруживается иммунной системой (так называемая иммуногенная смерть клеток ), которая мобилизует иммунные клетки с противоопухолевыми функциями. [163] Химиотерапевтические препараты, вызывающие иммуногенную гибель раковых опухолевых клеток, могут сделать невосприимчивые опухоли чувствительными к терапии иммунных контрольных точек . [164]
Некоторые химиотерапевтические препараты используются при заболеваниях, отличных от рака, например, при аутоиммунных заболеваниях [165] и нераковой дискразии плазматических клеток . В некоторых случаях их часто используют в более низких дозах, что означает, что побочные эффекты сведены к минимуму, [165] тогда как в других случаях используются дозы, аналогичные тем, которые используются для лечения рака. Метотрексат используется при лечении ревматоидного артрита (РА), [166] псориаза , [167] анкилозирующего спондилита [168] и рассеянного склероза . [169] [170] Считается, что противовоспалительный ответ, наблюдаемый при РА, обусловлен увеличением уровня аденозина , который вызывает иммуносупрессию ; воздействие на иммунорегуляторные пути фермента циклооксигеназы -2; снижение провоспалительных цитокинов ; и антипролиферативные свойства. [166] Хотя метотрексат используется для лечения как рассеянного склероза, так и анкилозирующего спондилита, его эффективность при этих заболеваниях до сих пор не определена. [168] [169] [170] Циклофосфамид иногда используется для лечения волчаночного нефрита , распространенного симптома системной красной волчанки . [171] Дексаметазон вместе с бортезомибом или мелфаланом обычно используется для лечения AL-амилоидоза . Недавно бортезомид в сочетании с циклофосфамидом и дексаметазоном также оказался перспективным для лечения AL-амилоидоза. Другие препараты, используемые для лечения миеломы , такие как леналидомид, показали многообещающую эффективность в лечении AL-амилоидоза. [172]
Химиотерапевтические препараты также используются в схемах кондиционирования перед трансплантацией костного мозга ( трансплантация гемопоэтических стволовых клеток ). Схемы кондиционирования используются для подавления иммунной системы реципиента, чтобы обеспечить приживление трансплантата. Циклофосфамид является распространенным цитотоксическим препаратом, используемым таким образом, и его часто применяют в сочетании с общим облучением тела . Химиотерапевтические препараты могут использоваться в высоких дозах для окончательного удаления клеток костного мозга реципиента (миелоаблативное кондиционирование) или в более низких дозах, чтобы предотвратить необратимую потерю костного мозга (немиелоаблативное кондиционирование и кондиционирование пониженной интенсивности). [173] При использовании в нераковых условиях лечение по-прежнему называется «химиотерапией» и часто проводится в тех же лечебных центрах, которые используются для людей, больных раком.
В 1970-х годах противоопухолевые (химиотерапевтические) препараты были признаны опасными, и с тех пор Американское общество фармацевтов системы здравоохранения (ASHP) ввело концепцию опасных лекарств после публикации в 1983 году рекомендации относительно обращения с опасными лекарствами. Адаптация федеральных правил произошла, когда Управление по охране труда США (OSHA) впервые опубликовало свои рекомендации в 1986 году, а затем обновило их в 1996, 1999 годах и, совсем недавно, в 2006 году. [174]
С тех пор Национальный институт безопасности и гигиены труда (NIOSH) проводит оценку на рабочем месте в отношении этих препаратов. Профессиональное воздействие противоопухолевых препаратов связано с многочисленными последствиями для здоровья, включая бесплодие и возможные канцерогенные эффекты. В отчете NIOSH сообщалось о нескольких случаях, например, о случае, когда у женщины-фармацевта был диагностирован папиллярный переходно-клеточный рак. За двенадцать лет до того, как у фармацевта диагностировали это заболевание, она проработала 20 месяцев в больнице, где отвечала за приготовление нескольких противоопухолевых препаратов. [175] У фармацевта не было других факторов риска развития рака, и поэтому ее рак был связан с воздействием противоопухолевых препаратов, хотя причинно-следственная связь в литературе не установлена. Другой случай произошел, когда неисправность в шкафах биобезопасности, как полагают, привела к воздействию противоопухолевых препаратов на медперсонал. Расследования выявили наличие генотоксичных биомаркеров через два и девять месяцев после воздействия.
Противоопухолевые препараты обычно вводятся внутривенно , внутримышечно , интратекально или подкожно . В большинстве случаев, прежде чем лекарство будет введено пациенту, его необходимо подготовить и обработать несколькими работниками. Любой работник, который занимается обращением, приготовлением или введением лекарств, а также чисткой предметов, контактировавших с противоопухолевыми препаратами, потенциально подвергается воздействию опасных лекарств. Медицинские работники подвергаются воздействию лекарств при различных обстоятельствах, например, когда фармацевты и фармацевты готовят и обрабатывают противоопухолевые препараты, а также когда медсестры и врачи вводят лекарства пациентам. Кроме того, риску заражения подвергаются и те, кто отвечает за утилизацию противоопухолевых препаратов в медицинских учреждениях. [176]
Считается, что основным путем воздействия является кожное воздействие, поскольку значительные количества противоопухолевых агентов были обнаружены в перчатках, которые носят медицинские работники, которые готовят, обрабатывают и вводят эти агенты. Еще один заслуживающий внимания путь воздействия – вдыхание паров наркотиков. В многочисленных исследованиях ингаляционный путь изучался как путь воздействия, и хотя пробы воздуха не выявили каких-либо опасных уровней, это все еще потенциальный путь воздействия. Проглатывание через руки в рот представляет собой путь заражения, который менее вероятен по сравнению с другими из-за жестких гигиенических стандартов в медицинских учреждениях. Тем не менее, это все еще потенциальный путь, особенно на рабочем месте, за пределами медицинского учреждения. Человек также может подвергнуться воздействию этих опасных наркотиков при инъекции иглой . Исследования, проведенные в этой области, установили, что профессиональное воздействие происходит путем изучения доказательств в многочисленных пробах мочи медицинских работников. [177]
Опасные лекарства подвергают медицинских работников серьезному риску для здоровья. Многие исследования показывают, что противоопухолевые препараты могут иметь множество побочных эффектов на репродуктивную систему, такие как потеря плода, врожденные пороки развития и бесплодие. Работники здравоохранения, которые во многих случаях подвергаются воздействию противоопухолевых препаратов, имеют неблагоприятные репродуктивные последствия, такие как самопроизвольные аборты, мертворождения и врожденные пороки развития. Более того, исследования показали, что воздействие этих препаратов приводит к нарушениям менструального цикла. Противоопухолевые препараты также могут увеличить риск нарушений обучаемости среди детей работников здравоохранения, которые подвергаются воздействию этих опасных веществ. [178]
Более того, эти препараты обладают канцерогенным действием. За последние пять десятилетий многочисленные исследования показали канцерогенные эффекты воздействия противоопухолевых препаратов. Аналогичным образом, были проведены исследования, которые связали алкилирующие агенты с развитием у людей лейкемии. Исследования показали повышенный риск развития рака молочной железы, немеланомного рака кожи и рака прямой кишки среди медсестер, подвергающихся воздействию этих препаратов. Другие исследования показали, что существует потенциальный генотоксический эффект противоопухолевых препаратов для работников медицинских учреждений. [175]
По состоянию на 2018 год не было установлено никаких пределов профессионального воздействия для противоопухолевых препаратов, то есть OSHA или Американская конференция правительственных специалистов по промышленной гигиене (ACGIH) не установили руководящие принципы безопасности на рабочем месте. [179]
NIOSH рекомендует использовать вентилируемый шкаф , предназначенный для снижения воздействия на работников. Кроме того, он рекомендует провести обучение всего персонала, использовать шкафы, провести первоначальную оценку техники программы безопасности и носить защитные перчатки и халаты при открытии упаковки лекарств, обращении с флаконами или маркировке. При ношении средств индивидуальной защиты перед использованием следует проверять перчатки на наличие физических дефектов и всегда надевать двойные перчатки и защитные халаты. Медицинские работники также обязаны мыть руки с водой и мылом до и после работы с противоопухолевыми препаратами, менять перчатки каждые 30 минут или при каждом проколе и немедленно выбрасывать их в контейнер для химиотерапевтических отходов. [180]
Используемые халаты должны быть одноразовыми, изготовленными из полипропилена с полиэтиленовым покрытием. Нося халаты, люди должны убедиться, что они закрыты и имеют длинные рукава. Когда подготовка завершена, конечный продукт следует полностью запечатать в полиэтиленовый пакет. [181]
Медицинский работник также должен протирать все контейнеры для отходов внутри вентилируемого шкафа, прежде чем вынимать их из шкафа. Наконец, работникам следует снять всю защитную одежду и положить ее в мешок для утилизации внутри вентилируемого шкафа. [176]
Лекарственные препараты следует вводить только с использованием защитных медицинских устройств, таких как списки игл и закрытых систем, а также таких методов, как заполнение внутривенных трубок персоналом аптеки внутри вентилируемого шкафа. Работники всегда должны носить средства индивидуальной защиты, такие как двойные перчатки, очки и защитные халаты, при открытии внешней сумки и сборке системы доставки для доставки препарата пациенту, а также при утилизации всех материалов, использованных при введении лекарств. [179]
Работникам больницы никогда не следует вынимать трубки из капельного мешка, содержащего противоопухолевый препарат, а при отсоединении трубок системы они должны убедиться, что трубки тщательно промыты. После извлечения пакета для внутривенного введения работники должны поместить его вместе с другими одноразовыми предметами непосредственно в желтый контейнер для отходов химиотерапии с закрытой крышкой. Защитные средства следует снять и положить в одноразовый контейнер для химиотерапевтических отходов. После этого следует собрать отходы химиотерапии в двойной пакет до или после снятия внутренних перчаток. Кроме того, перед тем как покинуть место введения препарата, необходимо всегда мыть руки с мылом. [182]
Все сотрудники, чья работа в медицинских учреждениях подвергает их воздействию опасных наркотиков, должны пройти обучение. Обучение должно охватывать персонал, занимающийся транспортировкой и приемкой, домработниц, фармацевтов, помощников и всех лиц, участвующих в транспортировке и хранении противоопухолевых препаратов. Эти люди должны получить информацию и пройти обучение, чтобы информировать их об опасностях наркотиков, присутствующих в их сферах работы. Они должны быть проинформированы и обучены операциям и процедурам на своих рабочих местах, где они могут столкнуться с опасностями, различным методам, используемым для обнаружения присутствия опасных наркотиков и тому, как высвобождаются опасности, а также физическим опасностям и опасностям для здоровья, связанным с наркотиками, включая их репродуктивную функцию. и потенциал канцерогенной опасности. Кроме того, их следует проинформировать и обучить мерам, которые им следует принять, чтобы избежать этих опасностей и защитить себя от них. Эту информацию необходимо предоставлять при контакте медицинских работников с лекарственными средствами, то есть при выполнении первоначального задания на рабочем месте с опасными лекарственными средствами. Кроме того, обучение должно проводиться при появлении новых опасностей, а также при внедрении новых лекарств, процедур или оборудования. [179]
При проведении уборки и обеззараживания рабочей зоны, где применяются противоопухолевые препараты, следует обеспечить достаточную вентиляцию для предотвращения накопления концентраций передающихся по воздуху препаратов. При очистке рабочей поверхности работники больницы должны использовать деактивирующие и чистящие средства до и после каждого вида деятельности, а также в конце смены. Уборку всегда следует производить в двойных защитных перчатках и одноразовых халатах. После того, как сотрудники закончат уборку, им следует выбросить использованные при этом предметы в желтый контейнер для отходов химиотерапии, сохраняя при этом защитные перчатки. После снятия перчаток следует тщательно вымыть руки с мылом. Все, что контактировало с противоопухолевыми препаратами или имело их следы, например иглы, пустые флаконы, шприцы, халаты и перчатки, следует поместить в контейнер для отходов химиотерапии. [183]
Необходимо иметь письменную политику на случай разлива противоопухолевых препаратов. Политика должна учитывать возможность разливов разного размера, а также процедуры и средства индивидуальной защиты, необходимые для каждого размера. Обученный работник должен справиться с большой утечкой и всегда выбрасывать все чистящие материалы в контейнер для химических отходов в соответствии с правилами EPA, а не в желтый контейнер для отходов химиотерапии. [184]
Необходимо разработать программу медицинского наблюдения . В случае воздействия специалисты по гигиене труда должны запросить подробный анамнез и провести тщательный медицинский осмотр. Им следует проверить мочу потенциально подвергшегося воздействию работника с помощью щупа или микроскопического исследования, в основном на наличие крови, поскольку известно, что некоторые противоопухолевые препараты вызывают повреждение мочевого пузыря. [175]
Мутагенность мочи является маркером воздействия противоопухолевых препаратов, который впервые был использован Фальком и его коллегами в 1979 году с использованием анализов бактериальной мутагенности. Помимо того, что тест неспецифичен, на него могут влиять посторонние факторы, такие как рацион питания и курение, поэтому его используют с осторожностью. Однако испытание сыграло значительную роль в изменении использования боксов с горизонтальным потоком на боксы биологической безопасности с вертикальным потоком при приготовлении противоопухолевых препаратов, поскольку первые подвергали медицинских работников воздействию высоких доз лекарств. Это изменило обращение с лекарствами и эффективно снизило воздействие противоопухолевых препаратов на рабочих. [175]
Биомаркеры воздействия противоопухолевых препаратов обычно включают платину в моче , метотрексат , циклофосфамид и ифосфамид в моче , а также метаболит 5-фторурацила в моче . Помимо этого, существуют и другие препараты, позволяющие измерять содержание лекарств непосредственно в моче, хотя они используются редко. Измерение содержания этих препаратов непосредственно в моче является признаком высоких уровней воздействия и того, что попадание наркотиков происходит либо через дыхательные пути, либо через кожу. [175]
Существует обширный список противоопухолевых средств . Для разделения лекарств, применяемых против рака, на несколько различных типов использовалось несколько классификационных схем. [185] [186]


Впервые низкомолекулярные препараты для лечения рака были использованы в начале 20-го века, хотя конкретные химические вещества изначально не предназначались для этой цели. Горчичный газ использовался в качестве боевого отравляющего вещества во время Первой мировой войны , и было обнаружено, что он является мощным подавителем кроветворения ( производства крови). [187] Подобное семейство соединений, известное как азотистые иприты , дополнительно изучалось во время Второй мировой войны в Йельской медицинской школе . [188] Было высказано предположение, что агент, повреждающий быстро растущие лейкоциты, может оказывать аналогичный эффект на рак. [188] Поэтому в декабре 1942 года нескольким людям с запущенными лимфомами (раком лимфатической системы и лимфатических узлов) препарат вводили внутривенно, а не вдыхая раздражающий газ. [188] Их улучшение, хотя и временное, было замечательным. [189] Одновременно во время военной операции во время Второй мировой войны, после налета немецкой авиации на итальянскую гавань Бари , несколько сотен человек случайно подверглись воздействию горчичного газа, который был доставлен туда союзными войсками для подготовки к возможному возмездию. в случае применения Германией химического оружия. Позже выяснилось, что у выживших было очень низкое количество лейкоцитов. [190] После того, как Вторая мировая война закончилась и отчеты были рассекречены, опыты совпали и побудили исследователей искать другие вещества, которые могли бы оказывать аналогичное воздействие на рак. Первым химиотерапевтическим препаратом, разработанным в рамках этого направления исследований, был мустин . С тех пор было разработано множество других лекарств для лечения рака, и разработка лекарств превратилась в многомиллиардную индустрию, хотя принципы и ограничения химиотерапии, открытые ранними исследователями, все еще применимы. [191]
Слово «химиотерапия без модификатора» обычно относится к лечению рака, но его историческое значение было более широким. Этот термин был придуман в начале 1900-х годов Паулем Эрлихом и означал любое использование химических веществ для лечения любого заболевания ( химио- + -терапия ), например, использование антибиотиков ( антибактериальная химиотерапия ). [192] Эрлих не верил в то, что будут найдены эффективные химиотерапевтические препараты для лечения рака. [192] Первым современным химиотерапевтическим агентом был арсфенамин , соединение мышьяка, открытое в 1907 году и используемое для лечения сифилиса . [193] Позже за этим последовали сульфаниламиды (сульфамидные препараты) и пенициллин . В сегодняшнем использовании смысл « любое лечение заболеваний лекарственными средствами» часто выражается словом «фармакотерапия» . С точки зрения метафорического языка, «химиотерапию» можно сравнить с идеей «шторма», поскольку и то, и другое может вызвать страдания, но впоследствии может иметь лечебный/очищающий эффект.
Топ-10 самых продаваемых (с точки зрения доходов) лекарств от рака 2013 года: [194]

Специально направленные средства доставки направлены на повышение эффективных уровней химиотерапии для опухолевых клеток при одновременном снижении эффективных уровней для других клеток. Это должно привести к увеличению гибели опухоли или снижению токсичности, или к тому и другому. [195]
Конъюгаты антитело-лекарственное средство (ADC) содержат антитело , лекарственное средство и линкер между ними. Антитело будет нацелено на белок, преимущественно экспрессируемый в опухолевых клетках (известный как опухолевый антиген ) или на клетки, которые опухоль может использовать, например, эндотелиальные клетки кровеносных сосудов . Они связываются с опухолевым антигеном и интернализуются, при этом линкер высвобождает лекарство в клетку. Эти специально нацеленные средства доставки различаются по своей стабильности, селективности и выбору мишени, но, по сути, все они направлены на увеличение максимальной эффективной дозы, которая может быть доставлена в опухолевые клетки. [196] Снижение системной токсичности означает, что их также можно использовать у более больных людей и что они могут нести новые химиотерапевтические агенты, которые были бы слишком токсичными для доставки с помощью традиционных системных подходов. [197]
Первым одобренным препаратом этого типа был гемтузумаб озогамицин (Милотарг), выпущенный компанией Wyeth (ныне Pfizer ). Препарат одобрен для лечения острого миелолейкоза . [198] Два других препарата, трастузумаб эмтанзин и брентуксимаб ведотин , находятся на поздних клинических испытаниях, а последний получил ускоренное одобрение для лечения рефрактерной лимфомы Ходжкина и системной анапластической крупноклеточной лимфомы . [196]
Наночастицы — это частицы размером от 1 до 1000 нанометров (нм), которые могут способствовать селективности опухоли и способствовать доставке малорастворимых лекарств . Наночастицы могут быть нацелены пассивно или активно. Пассивное нацеливание использует разницу между кровеносными сосудами опухоли и нормальными кровеносными сосудами. Кровеносные сосуды в опухолях являются «дырявыми», поскольку имеют щели размером от 200 до 2000 нм, которые позволяют наночастицам выходить в опухоль. Активное нацеливание использует биологические молекулы ( антитела , белки , ДНК и лиганды рецепторов ) для преимущественного нацеливания наночастиц на опухолевые клетки. Существует много типов систем доставки наночастиц, таких как диоксид кремния , полимеры , липосомы [199] и магнитные частицы. Наночастицы из магнитного материала также можно использовать для концентрации агентов в местах опухоли с помощью внешнего магнитного поля. [195] Они стали полезным средством магнитной доставки лекарств для плохо растворимых агентов, таких как паклитаксел . [200]
Электрохимиотерапия — это комбинированное лечение, при котором за инъекцией химиотерапевтического препарата следует локальное воздействие высоковольтных электрических импульсов на опухоль. Лечение позволяет химиотерапевтическим препаратам, которые в противном случае не могут или с трудом проходят через мембрану клеток (таким как блеомицин и цисплатин), проникнуть в раковые клетки. Следовательно, достигается большая эффективность противоопухолевого лечения. [201]
Клиническая электрохимиотерапия успешно применяется для лечения опухолей кожи и подкожной клетчатки независимо от их гистологического происхождения. [202] [203] Во всех отчетах о клиническом использовании электрохимиотерапии этот метод был отмечен как безопасный, простой и высокоэффективный. По проекту ESOPE (Европейские стандартные операционные процедуры электрохимиотерапии) были подготовлены Стандартные операционные процедуры (СОП) электрохимиотерапии, основанные на опыте ведущих европейских онкологических центров по электрохимиотерапии. [204] [205] Недавно были разработаны новые методы электрохимиотерапии для лечения внутренних опухолей с использованием хирургических процедур, эндоскопических методов или чрескожных подходов для получения доступа к области лечения. [206] [207]
Гипертермическая терапия — это тепловая обработка рака, которая может быть мощным инструментом в сочетании с химиотерапией (термохимиотерапией) или лучевой терапией для борьбы с различными видами рака. Тепло можно приложить локально к месту опухоли, что расширит кровеносные сосуды опухоли, позволяя большему количеству химиотерапевтических препаратов проникнуть в опухоль. Кроме того, мембрана опухолевой клетки станет более пористой, что позволит большему количеству химиотерапевтического лекарства проникнуть в опухолевую клетку.
Также было показано, что гипертермия помогает предотвратить или обратить вспять «химиорезистентность». Устойчивость к химиотерапии иногда развивается с течением времени, поскольку опухоли адаптируются и могут преодолеть токсичность химиопрепаратов. «Преодоление химиорезистентности широко изучалось в прошлом, особенно с использованием клеток, устойчивых к CDDP. Что касается потенциальной выгоды, заключающейся в том, что устойчивые к лекарствам клетки могут быть задействованы для эффективной терапии путем сочетания химиотерапии с гипертермией, было важно показать, что химиорезистентность против нескольких противораковые препараты (например, митомицин С, антрациклины, BCNU, мелфалан), включая CDDP, можно, по крайней мере частично, обратить вспять путем добавления тепла [208] .
Химиотерапия используется в ветеринарии так же, как и в медицине человека. [209]
Тошнота и рвота являются двумя наиболее опасными побочными эффектами, связанными с лечением рака, для больных раком и их семей.