В качестве лекарственного средства инсулин представляет собой любой фармацевтический препарат белкового гормона инсулина , который используется для лечения повышенного уровня глюкозы в крови . [6] К таким состояниям относятся диабет 1 типа , диабет 2 типа , гестационный диабет и осложнения диабета , такие как диабетический кетоацидоз и гиперосмолярные гипергликемические состояния . [6] Инсулин также используется вместе с глюкозой для лечения гиперкалиемии (высокого уровня калия в крови). [7] Обычно его вводят путем инъекции под кожу , но некоторые формы также можно использовать путем инъекции в вену или мышцу . [6] Существуют различные типы инсулина, подходящие для разных периодов времени. Все эти типы часто называют инсулином в широком смысле , хотя в более точном смысле инсулин идентичен природной молекуле, тогда как аналоги инсулина имеют немного разные молекулы, что позволяет изменить время действия. Он включен в Список основных лекарственных средств Всемирной организации здравоохранения . [8] [9] В 2020 году обычный человеческий инсулин занял 307-е место среди наиболее часто назначаемых лекарств в США: на него было выписано более 1 миллиона рецептов. [10] [11]
Инсулин можно производить из поджелудочной железы свиней или коров. [12] Человеческие версии могут быть созданы либо путем модификации свиных версий, либо с помощью рекомбинантной технологии [12] с использованием в основном E. coli или Saccharomyces cerevisiae . [13] Он бывает трех основных типов: короткого действия (например, обычный инсулин ), промежуточного действия (например, нейтральный протамин инсулин Хагедорна (НПХ)) и длительного действия (например, инсулин гларгин ). [12]
Инсулин впервые был использован в качестве лекарства в Канаде Чарльзом Бестом и Фредериком Бантингом в 1922 году. [14] [15]
Это хронология ключевых вех в истории медицинского использования инсулина. Более подробную информацию об открытии, экстракции, очистке, клиническом использовании и синтезе инсулина см. в разделе Инсулин .



Инсулин используется для лечения ряда заболеваний, включая диабет и его острые осложнения, такие как диабетический кетоацидоз и гиперосмолярные гипергликемические состояния . Он также используется вместе с глюкозой для лечения повышенного уровня калия в крови . Использование во время беременности относительно безопасно для ребенка. [6] Инсулин ранее использовался в психиатрическом лечении, называемом инсулиновой шоковой терапией . [23]
Некоторые побочные эффекты включают гипогликемию (низкий уровень сахара в крови), гипокалиемию (низкий уровень калия в крови) и аллергические реакции . [6] Аллергия на инсулин затрагивает около 2% людей, из которых большинство реакций вызвано не самим инсулином, а консервантами, добавленными к инсулину, такими как цинк, протамин и метакрезол . Большинство реакций относятся к реакциям гиперчувствительности I типа и редко вызывают анафилаксию . Подозрение на аллергию на инсулин может быть подтверждено прик-тестами , пластырями и иногда биопсией кожи . Терапия первой линии при реакциях гиперчувствительности к инсулину включает симптоматическую терапию антигистаминными препаратами. Затем пострадавших переводят на препарат, который не содержит конкретного агента, на который они реагируют, или подвергают десенсибилизации . [24]
Кожные побочные эффекты
Другие побочные эффекты могут включать боль или изменения кожи в местах инъекции. Повторная подкожная инъекция без ротации места может привести к липогипертрофии и амилоидомам, которые проявляются в виде плотных пальпируемых узелков под кожей. [25]
Раннее начало инсулинотерапии для долгосрочного лечения таких состояний, как диабет 2 типа, предполагает, что использование инсулина имеет уникальные преимущества, однако при инсулинотерапии существует необходимость постепенного повышения дозы и усложнения режима. , а также вероятность развития тяжелой гипогликемии, поэтому многие люди и их врачи не решаются начинать инсулинотерапию на ранней стадии лечения заболевания. [26] Многие препятствия, связанные с поведением в отношении здоровья, также мешают людям с сахарным диабетом 2 типа начать или усилить лечение инсулином, включая отсутствие мотивации, отсутствие знаний или опыта лечения, а также ограничения во времени, из-за которых у людей возникают высокие гликемические нагрузки в течение длительного времени. длительные периоды времени до начала инсулинотерапии. Вот почему управление побочными эффектами, связанными с длительным ранним рутинным применением инсулина при сахарном диабете 2 типа, может оказаться трудной терапевтической и поведенческой проблемой. [27]
Инсулин – эндогенный гормон , который вырабатывается поджелудочной железой . [30] Белок инсулина оказался высококонсервативным на протяжении эволюции и присутствует как у млекопитающих , так и у беспозвоночных . Сигнальный путь инсулина/ инсулиноподобного фактора роста (IIS) тщательно изучался у таких видов, как нематоды (например, C. elegans ), мухи ( Drosophila melanogaster ) и мыши ( Mus musculus ). Механизмы его действия очень схожи у разных видов. [31]
Как диабет 1-го типа , так и диабет 2-го типа характеризуются потерей функции поджелудочной железы, хотя и в разной степени. [30] Людей, страдающих диабетом, называют диабетиками. Многим диабетикам требуется экзогенный источник инсулина, чтобы поддерживать уровень сахара в крови в безопасном целевом диапазоне. [32] [33] [34]
В 1916 году Николае Паулеску (1869–1931) удалось разработать водный экстракт поджелудочной железы, который нормализовал состояние собаки, страдающей диабетом. В 1921 году он опубликовал 4 статьи в Биологическом обществе в Париже, посвященные успешному воздействию экстракта поджелудочной железы на собак с диабетом. Исследование Паулеску о роли поджелудочной железы в усвоении пищи было опубликовано в августе 1921 года в Archives Internationales de Physiologie, Льеж, Бельгия. Первоначально единственным способом получить инсулин для клинического использования было его извлечение из поджелудочной железы другого существа. Железы животных можно было получить как отходы мясоперерабатывающей промышленности. Инсулин получали в основном от коров ( Eli Lilly and Company ) и свиней ( Nordisk Insulinlaboratorium ). Для изготовления восьми унций очищенного инсулина может потребоваться до двух тонн частей свиньи. [35] [36] [37] Инсулин из этих источников эффективен для людей, поскольку он очень похож на человеческий инсулин (разница в три аминокислоты у бычьего инсулина, разница в одну аминокислоту у свиньи). [37] Первоначально более низкая чистота препарата приводила к аллергическим реакциям на присутствие неинсулиновых веществ. Чистота неуклонно улучшалась с 1920-х годов, в конечном итоге достигнув чистоты 99% к середине 1970-х годов благодаря методам жидкостной хроматографии высокого давления (ВЭЖХ). Незначительные аллергические реакции все еще иногда возникают, даже на синтетические «человеческие» разновидности инсулина. [37]
Начиная с 1982 года биосинтетический «человеческий» инсулин производится для клинического использования с помощью методов генной инженерии с использованием технологии рекомбинантной ДНК . Компания Genentech разработала технологию, используемую для производства первого такого инсулина, Хумулина, но сама не продавала этот продукт на коммерческом рынке. Компания Eli Lilly выпустила на рынок Хумулин в 1982 году. [38] Хумулин был первым лекарством, произведенным с использованием современных методов генной инженерии, при которых настоящая человеческая ДНК вставляется в клетку-хозяина ( в данном случае E. coli ). Затем клеткам-хозяевам позволяют нормально расти и размножаться, и благодаря вставленной человеческой ДНК они производят синтетическую версию человеческого инсулина. Производители утверждают, что это уменьшает присутствие многих примесей. Однако клинические препараты, приготовленные из таких инсулинов, отличаются от эндогенного человеческого инсулина в нескольких важных отношениях; примером является отсутствие C-пептида , который, как было показано в последние годы, сам по себе оказывает системное воздействие. Ново Нордиск также независимо разработала генно-инженерный инсулин, используя дрожжевой процесс. [39] [40]
Согласно исследованию, проведенному Международной диабетической федерацией в 2002 году по вопросам доступа и наличия инсулина в странах-членах, примерно 70% инсулина, который в настоящее время продается в мире, представляет собой рекомбинантный биосинтетический «человеческий» инсулин. [41] Большая часть инсулина, используемого сегодня в клинической практике, производится таким способом, хотя клинический опыт предоставил противоречивые данные о том, что эти инсулины с меньшей вероятностью вызывают аллергическую реакцию. Сообщалось о побочных реакциях; к ним относятся потеря предупредительных признаков того, что пациенты могут впасть в кому из-за гипогликемии , судорог, провалов в памяти и потери концентрации. [42] Однако в заявлении Международной диабетической федерации от 2005 года очень четко сказано, что «нет НИКАКИХ неопровержимых доказательств предпочтения одного вида инсулина другому» и «[современные, высокоочищенные] животные инсулины остаются вполне приемлемой альтернативой. " [43]
С января 2006 года все инсулины, распространяемые в США и некоторых других странах, являются синтетическими «человеческими» инсулинами или их аналогами. Требуется специальный процесс импорта FDA для получения бычьего или свиного инсулина для использования в США, хотя могут оставаться некоторые запасы свиного инсулина, произведенного Lilly в 2005 году или ранее, а свиной инсулин ленте также продается и продается под торговой маркой название Ветсулин (СМ) в США для использования в ветеринарии при лечении домашних животных с диабетом. [44]
При диабете 1 типа выработка инсулина чрезвычайно низка, поэтому организму требуется экзогенный инсулин. Некоторым людям с диабетом 2 типа, особенно с очень высокими показателями гемоглобина A1c , также может потребоваться базовая доза инсулина, поскольку их организм понижен чувствительности к уровню вырабатываемого инсулина. Базальный инсулин регулирует уровень глюкозы в крови между приемами пищи, а также в ночное время. Такая базальная скорость действия инсулина обычно достигается за счет использования инсулина промежуточного действия (например, НПХ) или аналога инсулина длительного действия. У больных сахарным диабетом 1 типа этого также можно добиться путем непрерывной инфузии инсулина быстрого действия с помощью инсулиновой помпы . Примерно половина суточной потребности человека в инсулине вводится в виде базального инсулина, обычно вводимого один раз в день на ночь. [45]
Когда человек ест пищу, содержащую углеводы и глюкозу, инсулин помогает регулировать метаболизм пищи в организме. Прандиальный инсулин, также называемый инсулином во время еды или болюсным инсулином, разработан в виде болюсной дозы инсулина перед едой для регулирования скачка уровня глюкозы в крови, который происходит после еды. Доза прандиального инсулина может быть статической или может быть рассчитана пациентом с использованием текущего уровня сахара в крови, запланированного потребления углеводов или того и другого. Этот расчет также может быть выполнен с помощью инсулиновой помпы у пациентов, использующих помпу. Режимы введения инсулина, состоящие из доз, рассчитанных таким образом, считаются интенсивными режимами введения инсулина . [46] Прандиальный инсулин обычно вводят не более чем за 15–30 минут до еды, используя инсулин быстрого действия или обычный инсулин. У некоторых пациентов можно использовать комбинированный инсулин, который содержит как инсулин НПХ (длительного действия), так и инсулин быстрого/регулярного действия, чтобы обеспечить как базальный инсулин, так и прандиальный инсулин. [45]
Существует несколько проблем, связанных с использованием инсулина в качестве клинического лечения диабета: [47]
Медицинские препараты инсулина никогда не представляют собой просто инсулин в воде (ничего больше). Клинические инсулины представляют собой смеси инсулина и других веществ, включая консерванты. Они предотвращают слишком быструю порчу или денатурацию белка , задерживают всасывание инсулина, регулируют pH раствора для уменьшения реакций в месте инъекции и так далее. [48]
Незначительные вариации молекулы человеческого инсулина называются аналогами инсулина (технически « лиганды инсулиновых рецепторов »), названными так потому, что технически они не являются инсулином, а являются аналогами, которые сохраняют функции гормона по управлению глюкозой. Они обладают характеристиками абсорбции и активности, которые в настоящее время недоступны при собственно подкожном введении инсулина. Они либо быстро всасываются, пытаясь имитировать настоящий бета-клеточный инсулин (как в случае с инсулином лизпро , инсулином аспарт и инсулином глулизином ), либо стабильно всасываются после инъекции вместо «пика», за которым следует более или менее быстрое снижение уровня инсулина. действия (как и инсулин детемир и инсулин гларгин ), при этом сохраняя сахароснижающее действие инсулина в организме человека. Тем не менее, ряд метаанализов , в том числе проведенных Кокрейновским сотрудничеством в 2005 году, [49] Немецким институтом качества и экономической эффективности в секторе здравоохранения [IQWiG], опубликованным в 2007 году, [50] и Канадским агентством по лекарственным средствам и «Технологии в здравоохранении» (CADTH) [51] , также выпущенные в 2007 году, не показали однозначных преимуществ в клиническом использовании аналогов инсулина по сравнению с более традиционными типами инсулина. [50] [51]
Обычно используемые типы инсулина следующие. [30]
Включает аналоги инсулина аспарт , лизпро и глулизин . Они начинают действовать через 5–15 минут и активны в течение 3–4 часов. Большинство инсулинов образуют гексамеры , которые задерживают поступление в кровь в активной форме; эти аналоговые инсулины не обладают нормальной инсулиновой активностью. В настоящее время ожидают одобрения регулирующих органов в США новые разновидности, которые созданы для быстрого действия, но сохраняют ту же генетическую структуру, что и обычный человеческий инсулин . [52] [53]
Включает обычный инсулин , который начинает действовать через 30 минут и активен примерно от 5 до 8 часов. [54]
Включает инсулин НПХ , который начинает действовать через 1–3 часа и активен в течение 16–24 часов. [55]
Включает аналоги гларгин U100 и детемир , каждый из которых начинает действовать через 1–2 часа и продолжает действовать без резких пиков или спадов в течение примерно 24 часов, хотя у многих людей это варьируется. [56] [57]
Включает аналоги инсулина гларгин U300 и деглудек , которые начинают действовать через 30–90 минут и продолжают действовать более 24 часов. [29]
Включает комбинацию инсулина быстрого или короткого действия с инсулином длительного действия, обычно инсулином НПХ . Комбинированные препараты начинают действовать вместе с инсулином короткого действия (5–15 минут для инсулина быстрого действия и 30 минут для короткого действия) и остаются активными в течение 16–24 часов. Существует несколько вариантов с разными пропорциями смешанных инсулинов (например, Novolog Mix 70/30 содержит 70% протамина аспарт [сродни НПХ] и 30% аспарт) [58]

В отличие от многих лекарств, инсулин в настоящее время нельзя принимать перорально. Как и почти все другие белки, попадающие в желудочно-кишечный тракт , он восстанавливается до фрагментов (компонентов из отдельных аминокислот), после чего теряется всякая активность. Были проведены некоторые исследования способов защиты инсулина от пищеварительного тракта, чтобы его можно было вводить в таблетках. Пока это полностью экспериментальный вариант. [59]
Инсулин обычно вводят подкожно с помощью одноразовых шприцов с иглами , инсулиновой помпы или инсулиновых шприц-ручек с иглами многократного использования . Люди, которые хотят уменьшить количество повторных проколов кожи при инъекциях инсулина, часто используют инъекционный порт в сочетании со шприцами. [60]
Использование подкожных инъекций инсулина предназначено для имитации естественного физиологического цикла секреции инсулина с учетом различных свойств используемых препаратов, таких как период полувыведения, начало действия и продолжительность действия. У многих людей для уменьшения количества инъекций в день используются инсулиновые препараты как быстрого или короткого действия, так и продукты среднего или длительного действия. В некоторых случаях инъекции инсулина можно комбинировать с другими инъекционными методами лечения, такими как агонисты рецептора GLP-1 . Очистка места инъекции и техника инъекции необходимы для обеспечения эффективной инсулинотерапии. [45]
Для некоторых инсулиновые помпы являются разумным решением. Преимуществами для человека являются лучший контроль над фоновой или базальной дозой инсулина, болюсные дозы, рассчитанные с точностью до долей единицы, и калькуляторы в помпе, которые могут помочь в определении доз болюсной инфузии. Ограничениями являются стоимость, возможность эпизодов гипогликемии и гипергликемии, проблемы с катетером и отсутствие средств «замкнутого цикла» контроля доставки инсулина на основе текущего уровня глюкозы в крови. [ нужна цитата ]
Инсулиновые помпы могут быть похожи на «электрические инъекторы», прикрепленные к временно имплантированному катетеру или канюле . Некоторые из тех, кто не может добиться адекватного контроля уровня глюкозы с помощью обычной (или струйной) инъекции, могут сделать это с помощью подходящей помпы. [61]
Постоянные катетеры создают риск заражения и образования язв, а у некоторых людей из-за инфузионных наборов может развиться липодистрофия . Эти риски часто можно свести к минимуму, поддерживая чистоту мест инфузии. Инсулиновые помпы требуют осторожности и усилий при правильном использовании. [61]
Одна международная единица инсулина (1 МЕ) определяется как «биологический эквивалент» 34,7 мкг чистого кристаллического инсулина.
Первым определением единицы инсулина было количество, необходимое для того, чтобы вызвать гипогликемию у кролика. Это было установлено Джеймсом Коллипом из Университета Торонто в 1922 году. Конечно, это зависело от размера и рациона кроликов. Единица инсулина была установлена инсулиновым комитетом Университета Торонто. [62] В конечном итоге эта единица превратилась в старую инсулиновую единицу USP , где одна единица (ЕД) инсулина устанавливалась равной количеству инсулина, необходимому для снижения концентрации глюкозы в крови у голодного кролика до 45 мкг / д л ( 2,5 м моль / л ). Как только химическая структура и масса инсулина были известны, единица инсулина определялась массой чистого кристаллического инсулина, необходимой для получения единицы USP.
Единица измерения, используемая в инсулинотерапии, не является частью Международной системы единиц (сокращенно СИ), которая является современной формой метрической системы . Вместо этого фармакологическая международная единица (МЕ) определяется Комитетом экспертов ВОЗ по биологической стандартизации . [63]
Центральной проблемой для тех, кто нуждается в наружном инсулине, является выбор правильной дозы инсулина и правильного времени введения.
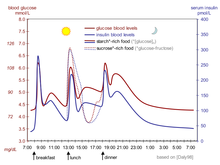
Физиологическая регуляция уровня глюкозы в крови, как у людей, не страдающих диабетом, была бы наилучшей. Повышение уровня глюкозы в крови после еды является стимулом для быстрого выброса инсулина из поджелудочной железы. Повышенный уровень инсулина вызывает поглощение и хранение глюкозы в клетках, снижает преобразование гликогена в глюкозу, снижая уровень глюкозы в крови и, таким образом, уменьшая высвобождение инсулина. В результате уровень глюкозы в крови несколько повышается после еды и в течение часа или около того возвращается к нормальному уровню «натощак». Даже самое лучшее лечение диабета синтетическим человеческим инсулином или даже аналогами инсулина, как бы оно ни проводилось, далеко не обеспечивает нормального контроля уровня глюкозы у людей, не страдающих диабетом. [64]
Ситуация усложняется тем, что состав съеденной пищи (см. гликемический индекс ) влияет на скорость всасывания в кишечнике. Глюкоза из некоторых продуктов усваивается быстрее (или медленнее), чем такое же количество глюкозы из других продуктов. Кроме того, жиры и белки вызывают задержку всасывания глюкозы из съеденных одновременно углеводов. Кроме того, физические упражнения снижают потребность в инсулине, даже если все остальные факторы остаются прежними, поскольку работающие мышцы обладают некоторой способностью поглощать глюкозу без помощи инсулина. [65]
Из-за сложных и взаимодействующих факторов в принципе невозможно точно знать, сколько инсулина (и какого типа) необходимо для «покрытия» конкретного приема пищи и достижения разумного уровня глюкозы в крови в течение часа или двух после еды. . Бета-клетки недиабетиков регулярно и автоматически справляются с этим путем постоянного мониторинга уровня глюкозы и высвобождения инсулина. Все подобные решения диабетика должны быть основаны на опыте и обучении (т. е. по указанию врача, специалиста по диабету или, в некоторых местах, специалиста по диабету) и, кроме того, конкретно на индивидуальном опыте человека. Но это непросто, и никогда не следует делать это по привычке или по рутине. Однако при некоторой осторожности это можно сделать достаточно хорошо в клинической практике. Например, некоторым людям с диабетом требуется больше инсулина после употребления обезжиренного молока , чем после приема эквивалентного количества жиров, белков, углеводов и жидкости в какой-либо другой форме. Их особая реакция на обезжиренное молоко отличается от реакции других людей с диабетом, но такое же количество цельного молока может вызвать еще иную реакцию даже у этого человека. Цельное молоко содержит значительное количество жира, а обезжиренное — гораздо меньше. Это постоянное балансирующее действие для всех людей с диабетом, особенно для тех, кто принимает инсулин.
Людям с инсулинозависимым диабетом обычно требуется некоторый базовый уровень инсулина (базальный инсулин), а также инсулин короткого действия для покрытия еды (болюс, также известный как инсулин во время еды или прандиальный инсулин). Поддержание базальной и болюсной дозы — это непрерывный процесс балансирования, который люди с инсулинозависимым диабетом должны выполнять каждый день. Обычно это достигается с помощью регулярных анализов крови, хотя в настоящее время становится доступным оборудование для непрерывного измерения уровня сахара в крови ( мониторы непрерывного измерения уровня глюкозы или CGM), которые могут помочь усовершенствовать этот балансирующий процесс, как только его широкое использование станет обычным явлением.
Инсулин длительного действия используется для приближения базальной секреции инсулина поджелудочной железой, которая меняется в течение дня. [66] Для этой цели можно использовать НПХ/изофан, ленте, ультраленте, гларгин и детемир. Преимуществом НПХ является его низкая стоимость, возможность смешивания его с формами инсулина короткого действия, тем самым сводя к минимуму количество инъекций, которые необходимо вводить, а также то, что активность НПХ достигает пика через 4–6 часов после введения. позволяя дозе перед сном сбалансировать тенденцию повышения уровня глюкозы с рассветом , наряду с меньшей утренней дозой, чтобы сбалансировать более низкую базальную потребность во второй половине дня, и, возможно, дневной дозой, чтобы покрыть вечернюю потребность. Недостаток НПХ перед сном заключается в том, что, если его не принять достаточно поздно (около полуночи), чтобы достичь пика незадолго до рассвета, он может вызвать гипогликемию. Одним из теоретических преимуществ гларгина и детемира является то, что их нужно принимать только один раз в день, хотя на практике многие люди обнаруживают, что ни один из них не действует в течение полных 24 часов. Их также можно принимать в любое время в течение дня при условии, что они принимаются в одно и то же время каждый день. Еще одним преимуществом инсулинов длительного действия является то, что базальный компонент режима инсулинотерапии (обеспечивающий минимальный уровень инсулина в течение дня) может быть отделен от прандиального или болюсного компонента (обеспечивающего покрытие времени приема пищи инсулинами ультракороткого действия), в то время как Схемы с использованием НПХ и обычного инсулина имеют тот недостаток, что любая корректировка дозы влияет как на базальный, так и на прандиальный охват. Гларгин и детемир существенно дороже НПХ, ленте и ультраленте, и их нельзя смешивать с другими формами инсулина. [ нужна цитата ]
Инсулин короткого действия используется для имитации выброса эндогенного инсулина, возникающего в ожидании еды. Для этой цели можно использовать обычный инсулин, лизпро, аспарт и глулизин. Регулярный инсулин следует вводить примерно за 30 минут до еды, чтобы обеспечить максимальную эффективность и свести к минимуму возможность гипогликемии. Лиспро, аспарт и глулизин разрешены для приема при первом укусе еды и могут быть даже эффективны, если принимать их после завершения еды. Инсулин короткого действия также используется для коррекции гипергликемии. [67]
Впервые описанный в 1934 году [68] , то, что врачи обычно называют инсулином скользящей шкалы (SSI), представляет собой только инсулин быстрого или быстрого действия, вводимый подкожно, обычно во время еды, а иногда и перед сном, [69] , но только тогда, когда уровень глюкозы в крови превышает пороговое значение (например, 10 ммоль/л, 180 мг/дл). [70] Так называемый метод «скользящей шкалы» широко преподается, хотя и подвергается резкой критике. [71] [72] [73] [74] Инсулин по скользящей шкале (SSI) не является эффективным способом лечения долгосрочного диабета у лиц, проживающих в домах престарелых. [69] [75] Скользящая шкала инсулина приводит к большему дискомфорту и увеличению времени кормления грудью. [75]
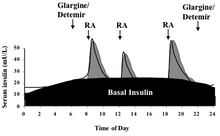
Пример схемы применения инсулина гларгин и инсулина лизпро:
Во время беременности может развиться спонтанная гипергликемия, которая может привести к гестационному сахарному диабету (ГСД) — частому осложнению беременности. Гестационный сахарный диабет (ГСД) распространен среди беременных женщин во всем мире в 6–20% и определяется как непереносимость глюкозы любой степени, развивающаяся или первоначально выявленная во время беременности. [76] Нейтральный протамин- инсулин Хагедорна (НПХ) был краеугольным камнем инсулинотерапии во время беременности, вводимый два-четыре раза в день. Женщины с ГСД и беременные женщины с сахарным диабетом I типа, которые часто проверяют уровень глюкозы в крови и используют для этого оборудование для мониторинга уровня глюкозы, используют непрерывную инфузию инсулина аналога инсулина быстрого действия, такого как лизпро и аспарт. Однако при выборе режима введения инсулина пациентам необходимо учитывать ряд соображений. При лечении ГСД у беременных эти рекомендации имеют решающее значение и могут варьироваться в зависимости от определенной физиологической и, что интересно, социокультурной среды. Действующие перинатальные рекомендации рекомендуют низкую суточную дозу инсулина с учетом физиологических особенностей женщины и частоты самоконтроля. Подчеркивается важность использования специализированного планирования инсулинотерапии на основе параметров, подобных указанным выше, а не широкого подхода. [77]
Женщины с ранее существовавшим диабетом имеют самый высокий уровень чувствительности к инсулину на ранних этапах беременности. Тщательный мониторинг уровня глюкозы необходим для предотвращения гипогликемии, которая потенциально может привести к изменению сознания, судорогам и вреду для матери. [78] Новорожденные с низкой массой тела при рождении также могут быть результатом гипогликемии, особенно у пациентов с диабетом 1 типа, поскольку они часто более чувствительны к инсулину, чем люди с диабетом 2 типа, и с большей вероятностью не осознают своего гипогликемического состояния. Тщательный мониторинг уровня глюкозы имеет важное значение, поскольку после 16 недель беременности женщины с ранее существовавшим диабетом становятся более резистентными к инсулину, и их потребности в инсулине могут колебаться еженедельно. Потребность в инсулине может возрастать от одной беременности к другой. Таким образом, вполне реально ожидать более высоких потребностей в контроле уровня глюкозы при последующих беременностях у повторнородящих женщин. [78]
Возможность использования инсулина в попытке улучшить спортивные результаты была предложена еще на зимних Олимпийских играх 1998 года в Нагано, Япония , как сообщил Питер Сёнксен в июльском выпуске журнала эндокринологии за 2001 год . Вопрос о том, могут ли спортсмены, не страдающие диабетом, легально использовать инсулин, был поднят российским медиком. [79] [80] Неясно, действительно ли инсулин улучшит спортивные результаты, но опасения по поводу его использования привели к тому, что Международный олимпийский комитет запретил использование гормона спортсменами, не страдающими диабетом, в 1998 году. [81]
В книге «Игра теней» (2001), написанной репортерами Марком Файнару-Вада и Лэнсом Уильямсом, содержались утверждения о том, что бейсболист Барри Бондс использовал инсулин (а также другие лекарства), очевидно полагая, что это повысит эффективность гормона роста, который он использовал. якобы брал. [82] Бондс в конечном итоге дал показания перед федеральным большим жюри в рамках правительственного расследования BALCO . [83]
В частности, утверждается, что бодибилдеры используют экзогенный инсулин и другие препараты, полагая, что они увеличат мышечную массу. Описано, что бодибилдеры вводят до 10 МЕ обычного синтетического инсулина перед употреблением сладкой пищи. [81] В отчете 2008 года высказывалось предположение, что инсулин иногда используется в сочетании с анаболическими стероидами и гормоном роста (ГР), и что «спортсмены подвергают себя потенциальному вреду, самостоятельно вводя большие дозы ГР, ИФР-I и инсулина». [84] [85] Злоупотребление инсулином упоминалось как возможный фактор смерти бодибилдеров Гента Уэйкфилда и Рича Пианы . [86]
Инсулин, гормон роста человека (HGH) и инсулиноподобный фактор роста 1 (IGF-1) назначаются самостоятельно теми, кто хочет увеличить мышечную массу за пределами возможностей, предлагаемых только анаболическими стероидами. Их обоснование заключается в том, что, поскольку инсулин и гормон роста действуют синергически, стимулируя рост, и поскольку IGF-1 является основным медиатором скелетно-мышечного роста, «наложение» инсулина, гормона роста и IGF-1 должно оказывать синергетический эффект роста на скелетные мышцы. Эту теорию в последние годы поддержали бодибилдеры высшего уровня, чей соревновательный вес превышает 50 фунтов (23 кг) мышц, что больше, чем у конкурентов в прошлом, и с еще более низким уровнем жира в организме. [ нужна цитата ]
Экзогенный инсулин значительно повышает скорость метаболизма глюкозы у тренирующихся спортсменов наряду со значительным увеличением пика V-02 . [87] Считается, что инсулин повышает работоспособность за счет увеличения синтеза белка, снижения катаболизма белка и облегчения переноса определенных аминокислот в скелетные мышцы человека. Считается, что спортсмены, получающие инсулин, имеют нежирную массу тела, поскольку физиологическая гиперинсулинемия в скелетных мышцах человека улучшает активность транспорта аминокислот, что, в свою очередь, способствует синтезу белка. [87] Инсулин стимулирует транспорт аминокислот в клетки, а также контролирует метаболизм глюкозы. Он уменьшает липолиз и увеличивает липогенез, поэтому бодибилдеры и спортсмены используют рчГР в сочетании с ним, чтобы компенсировать этот негативный эффект и одновременно максимизировать синтез белка. Спортсмены экстраполировали физиологию больных диабетом на спортивную арену, поскольку были заинтересованы в подавлении протеолиза. Установлено, что введение инсулина является белковым анаболиком при инсулинорезистентном состоянии хронической почечной недостаточности. [88] Он ингибирует протеолиз и при введении вместе с аминокислотами усиливает чистый синтез белка. Экзогенная инъекция инсулина создает гиперинсулинемический зажим in vivo, повышая уровень мышечного гликогена до и во время фаз восстановления после интенсивных упражнений. Ожидается, что в результате увеличится мощность, сила и выносливость, а также это может ускорить процесс заживления после интенсивной физической активности. Во-вторых, ожидается, что инсулин увеличит мышечную массу, предотвращая распад мышечного белка при его употреблении вместе с диетой с высоким содержанием углеводов. Хотя ограниченное количество исследований действительно предполагает, что инсулином можно злоупотреблять в качестве фармакологического лечения для повышения силы и работоспособности у молодых, здоровых людей или спортсменов, недавняя оценка исследования показывает, что это применимо только к небольшой группе «лекарственных препаратов». -наивные» личности. [87]
Злоупотребление экзогенным инсулином сопряжено с сопутствующим риском гипогликемической комы и смерти, когда используемое количество превышает необходимое для обработки принятых углеводов. Острые риски включают повреждение головного мозга , паралич и смерть . Симптомы могут включать головокружение, слабость, дрожь, сердцебиение , судороги, спутанность сознания, головную боль, сонливость, кому, потливость и тошноту . Все лица с передозировкой должны быть направлены на медицинское обследование и лечение, которое может длиться несколько часов или дней. [89]
Данные Национальной системы данных о отравлениях США (2013 г.) показывают, что 89,3% случаев применения инсулина, зарегистрированных в токсикологических центрах, являются непреднамеренными и являются результатом терапевтических ошибок. Еще 10% случаев являются преднамеренными и могут отражать попытку самоубийства, жестокое обращение, преступные намерения, вторичную выгоду или другие неизвестные причины. [89] Гипогликемия, вызванная экзогенным инсулином, может быть обнаружена химически путем изучения соотношения инсулина и С-пептида в периферическом кровообращении. [90] Было высказано предположение, что этот тип подхода можно использовать для выявления экзогенного злоупотребления инсулином у спортсменов. [91]
Инсулин часто измеряют в сыворотке, плазме или крови, чтобы контролировать терапию людей, страдающих диабетом, подтвердить диагноз отравления у госпитализированных лиц или помочь в судебно-медицинском расследовании подозрительной смерти. Интерпретация полученных концентраций инсулина сложна, учитывая многочисленные доступные типы инсулина, различные пути введения, наличие антиинсулиновых антител у инсулинозависимых диабетиков и нестабильность препарата ex vivo . Другие потенциальные мешающие факторы включают широкую перекрестную реактивность коммерческих иммуноанализов инсулина на биосинтетические аналоги инсулина, использование высоких доз внутривенного инсулина в качестве антидота к передозировке антигипертензивных препаратов и посмертное перераспределение инсулина в организме. В некоторых обстоятельствах использование хроматографического метода для анализа инсулина может быть предпочтительнее иммуноанализа, чтобы избежать проблемы перекрестной реактивности, влияющей на количественный результат, а также для помощи в идентификации конкретного типа инсулина в образце. [92]
Комбинированная терапия инсулином и другими противодиабетическими препаратами, по-видимому, наиболее полезна для людей, страдающих диабетом, у которых все еще сохраняется остаточная способность к секреции инсулина. [93] Комбинация инсулинотерапии и сульфонилмочевины более эффективна, чем один инсулин, при лечении людей с диабетом 2 типа после вторичной неэффективности пероральных препаратов, что приводит к улучшению профилей глюкозы и/или снижению потребности в инсулине. [93]
В Соединенных Штатах цена за единицу инсулина неуклонно росла с 1991 по 2019 год. [94] [95] С 2002 по 2013 год она выросла в три раза. [96] Затраты могут достигать 900 долларов США в месяц. [96] В 2016 году были высказаны опасения по поводу того, что фармацевтические компании совместно работают над повышением цен. [96] В январе 2019 года законодатели Палаты представителей США направили письма производителям инсулина Eli Lilly and Co. , Sanofi и Novo Nordisk с просьбой объяснить быстрый рост цен на инсулин. Ежегодная стоимость инсулина для людей с диабетом 1 типа в США за период с 2012 по 2016 год выросла почти вдвое — с 2900 до 5700 долларов США. [97]
По данным Международной федерации планов медицинского страхования, люди в США платят в два-шесть раз больше, чем в остальном мире, включая Канаду, за фирменные лекарства, отпускаемые по рецепту. В Канаде, как и во многих других промышленно развитых странах, действует контроль над стоимостью фармацевтических препаратов. [98]
Калифорния в июле 2022 года утвердила бюджет, согласно которому штату будет выделено 100 миллионов долларов на создание собственного инсулина по цене, близкой к себестоимости. [99]
Инсулин и все другие лекарства предоставляются бесплатно людям, которые используют его для лечения диабета, Национальными службами здравоохранения стран Соединенного Королевства. [100]
В марте 2020 года FDA изменило правила одобрения новых препаратов инсулина. [101] Инсулин регулируется как биологический препарат, а не как лекарство. [101] Измененный статус дает FDA больше гибкости в вопросах одобрения и маркировки. [102] В июле 2021 года FDA одобрило инсулин гларгин-yfgn (Semglee), биоподобный продукт, содержащий аналог инсулина гларгин длительного действия. [103] Инсулин гларгин-yfgn является взаимозаменяемым и менее дорогим, чем эталонный препарат инсулин гларгин (Лантус), который был одобрен в 2000 году. [104] FDA требует, чтобы новые инсулиновые препараты не уступали существующим инсулиновым препаратам в отношении снижение гемоглобина А1с. [105]
В 2006 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило использование Эксуберы , первого ингаляционного инсулина. [106] Он был отозван с рынка его производителем в третьем квартале 2007 года из-за отсутствия признания.
Утверждается, что ингаляционный инсулин имеет такую же эффективность, как и инъекционный инсулин, как с точки зрения контроля уровня глюкозы, так и с точки зрения периода полувыведения из крови. В настоящее время ингаляционный инсулин имеет короткое действие и обычно принимается перед едой; часто по-прежнему требуется инъекция инсулина длительного действия на ночь. [107] Когда людей перевели с инъекционного инсулина на ингаляционный, не наблюдалось существенной разницы в уровнях Hb A1c в течение трех месяцев. Особой проблемой было точное дозирование, хотя у людей не наблюдалось значительного увеличения веса или снижения функции легких на протяжении всего исследования по сравнению с исходным уровнем. [108]
После его коммерческого запуска в 2005 году в Соединенном Королевстве он не был (по состоянию на июль 2006 года) рекомендован Национальным институтом здравоохранения и клинического мастерства для повседневного использования, за исключением случаев, когда существует «доказанная фобия инъекций, диагностированная психиатром или психологом». . [107]
В январе 2008 года крупнейший в мире производитель инсулина Novo Nordisk также объявил, что компания прекращает дальнейшую разработку собственной версии ингаляционного инсулина, известной как система ингаляционного инсулина AERx iDMS. [109] Аналогичным образом, компания Eli Lilly and Company прекратила разработку своего ингаляционного воздушного инсулина в марте 2008 года. [110] Afrezza , разработанный Mannkind , был разрешен FDA в июне 2014 года для использования у взрослых с диабетом I и II типа. , с ограничением на этикетке, ограничивающим его использование только теми, у кого также есть астма, активный рак легких или хроническая обструктивная болезнь легких. [111] Ингаляционный инсулин быстрого действия является компонентом комбинированного раствора лекарственного средства и устройства, который используется в начале каждого приема пищи. Он использует техносферную технологию, которая, по-видимому, имеет более практичный метод доставки и большую гибкость дозирования, а также новую форму инсулина для ингаляций (2,5 м). Для введения ингаляционного инсулина используется ингалятор размером с большой палец с улучшенной гибкостью дозировки. В его состав входит растворенный в порошке рекомбинантный человеческий инсулин (фумарил дикетопиперазин). Техносферный инсулин быстро всасывается поверхностью легких после ингаляции. В течение 12 часов после вдыхания оба вещества — инсулин и порошок (фумарил дикетопиперазин) — практически выводятся из легких здоровых людей. По сравнению с Эксуберой (8–9%), всего 0,3% ингаляционного инсулина все еще присутствовало в легких через 12 часов. Однако, поскольку сообщалось о повышении уровней антител в сыворотке без существенных клинических изменений, при его использовании сообщалось об остром бронхоспазме у пациентов с астмой и ХОБЛ, а также о значительном снижении диффузионной способности легких по монооксиду углерода по сравнению с подкожным введением инсулина. получил одобрение FDA с предупреждением (Стратегия оценки и смягчения рисков). [112] [111]
Существует несколько методов трансдермальной доставки инсулина. Пульсирующий инсулин использует микроструи для введения инсулина в организм человека, имитируя физиологическую секрецию инсулина поджелудочной железой. [113] Струйная инъекция имела разные пики и продолжительность доставки инсулина по сравнению с инъекцией иглой. Некоторые диабетики могут предпочесть струйные инъекции подкожным инъекциям. [114] Было обнаружено , что и электричество с использованием ионтофореза [115] , и ультразвук делают кожу временно пористой. Аспект введения инсулина остается экспериментальным, но аспект измерения уровня глюкозы в крови с помощью «наручных приборов» коммерчески доступен. Исследователи создали устройство, похожее на часы, которое проверяет уровень глюкозы в крови через кожу и вводит корректирующие дозы инсулина через поры кожи. Аналогичное устройство, но основанное на проникающих через кожу «микроиглах», находилось на стадии испытаний на животных в 2015 году. [116] За последние пару лет использование химических усилителей, электрических устройств и устройств с микроиглами показало огромные перспективы для улучшение проникновения инсулина по сравнению с пассивным транспортом через кожу. Трансдермальная доставка инсулина демонстрирует более удобный и минимально инвазивный подход к ежедневному лечению диабета, чем обычная подкожная инъекция, однако необходимы дополнительные исследования для решения таких вопросов, как долгосрочное использование, эффективность и надежность доставки, а также побочные эффекты, связанные с воспаление и раздражение. [117]
Инсулин может быть доставлен в центральную нервную систему интраназальным (ИН) путем практически без системного поглощения или связанных с ним периферических побочных эффектов. Было продемонстрировано, что введенный интраназально инсулин быстро накапливается в спинномозговой жидкости, что указывает на его эффективную транспортировку в мозг. Считается, что это накопление происходит вдоль обонятельных и близлежащих маршрутов. Хотя многочисленные исследования опубликовали обнадеживающие результаты, все еще проводятся дальнейшие исследования, чтобы понять его долгосрочные последствия и начать успешное клиническое применение. [118]
Основная привлекательность пероральных гипогликемических средств заключается в том, что большинство людей предпочитают таблетки или жидкость для перорального применения инъекциям. Однако инсулин представляет собой пептидный гормон , который переваривается в желудке и кишечнике и для того, чтобы эффективно контролировать уровень сахара в крови, его нельзя принимать перорально в его нынешней форме.
Предполагается, что потенциальный рынок пероральной формы инсулина огромен, поэтому многие лаборатории пытались разработать способы перемещения достаточного количества интактного инсулина из кишечника в воротную вену , чтобы оказать измеримое влияние на уровень сахара в крови. [119]
В настоящее время разрабатывается ряд стратегий дериватизации и составления рецептур в попытке разработать перорально доступный инсулин. [120] Многие из этих подходов используют системы доставки наночастиц [121] [122] [123] и некоторые из них проходят клинические испытания . [124] [125] [126]
Еще одним улучшением могла бы стать трансплантация поджелудочной железы или бета-клеток, чтобы избежать периодического введения инсулина. Это приведет к созданию саморегулирующегося источника инсулина. Трансплантация всей поджелудочной железы (как отдельного органа ) сложна и относительно редка. Ее часто выполняют в сочетании с трансплантацией печени или почки , хотя ее можно провести и отдельно. Также возможно провести трансплантацию только бета-клеток поджелудочной железы. Тем не менее, трансплантация островковых клеток в течение многих лет была экспериментальной, но некоторые исследователи из Альберты, Канада , разработали методы с высоким начальным уровнем успеха (около 90% в одной группе). Почти половина из тех, кому была проведена трансплантация островковых клеток, через год после операции отказались от инсулина; к концу второго года это число снижается примерно до одного из семи. Однако исследователи из Университета Иллинойса в Чикаго (UIC) немного модифицировали процедуру Эдмонтонского протокола трансплантации островковых клеток и добились независимости от инсулина у людей с диабетом, с меньшим количеством, но лучше функционирующих островковых клеток поджелудочной железы. [127] Необходимы долгосрочные исследования, чтобы подтвердить, улучшает ли он уровень инсулинонезависимых результатов.
Трансплантация бета-клеток может стать практичной в ближайшем будущем. Кроме того, некоторые исследователи изучали возможность трансплантации генетически модифицированных не-бета-клеток для секреции инсулина. [128] Клинически проверяемые результаты в настоящее время далеки от реализации. В исследовательских лабораториях разрабатываются несколько других нетрансплантационных методов автоматической доставки инсулина, но ни один из них не близок к клиническому одобрению.
{{cite book}}: |work=игнорируется ( помощь ){{cite book}}: |work=игнорируется ( помощь ){{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка )Если вы используете инсулин или лекарства для лечения диабета... вы не платите ни за какие лекарства, которые вам прописали.