Кремний — химический элемент ; он имеет символ Si и атомный номер 14. Это твердое, хрупкое кристаллическое твердое вещество с сине-серым металлическим блеском, неметалл и полупроводник . Он входит в 14-ю группу периодической таблицы: над ней находится углерод ; а ниже него — германий , олово , свинец и флеровий . Он относительно нереактивен.
Из-за его высокого химического сродства к кислороду только в 1823 году Йенс Якоб Берцелиус впервые смог получить его и охарактеризовать в чистом виде. Его оксиды образуют семейство анионов , известных как силикаты . Его температуры плавления и кипения 1414 °C и 3265 °C соответственно являются вторыми по величине среди всех металлоидов и неметаллов, уступая только бору . [а]
Кремний является восьмым наиболее распространенным элементом во Вселенной по массе, но очень редко встречается в чистом виде в земной коре. Он широко распространен в космосе в космической пыли , планетоидах и планетах в виде различных форм диоксида кремния (кремнезема) или силикатов . Более 90% земной коры состоит из силикатных минералов , что делает кремний вторым по распространенности элементом в земной коре (около 28% по массе) после кислорода .
Большая часть кремния используется в коммерческих целях без разделения, часто с очень незначительной обработкой природных минералов. Такое использование включает промышленное строительство с использованием глины , кварцевого песка и камня . Силикаты используются в портландцементе для изготовления строительного раствора и штукатурки , а также смешиваются с кварцевым песком и гравием для изготовления бетона для дорожек, фундаментов и дорог. Они также используются в белой керамике , такой как фарфор , а также в традиционном силикатном натриево - известковом стекле и многих других специальных стеклах . Соединения кремния, такие как карбид кремния , используются в качестве абразивов и компонентов высокопрочной керамики. Кремний является основой широко используемых синтетических полимеров, называемых силиконами .
Конец 20-го - начало 21-го века был описан как кремниевый век (также известный как век цифровых технологий или век информации ) из-за большого влияния, которое элементарный кремний оказывает на современную мировую экономику. Небольшая часть очень высокоочищенного элементарного кремния, используемого в полупроводниковой электронике (<15%), необходима для транзисторов и микросхем интегральных схем , используемых в большинстве современных технологий, таких как смартфоны и другие компьютеры . В 2019 году 32,4% сегмента рынка полупроводников приходилось на сети и коммуникационные устройства, а к 2027 году, по прогнозам, объем полупроводниковой промышленности достигнет 726,73 миллиарда долларов. [12]
Кремний является важным элементом в биологии. Большинству животных необходимы только следы, но некоторые морские губки и микроорганизмы, такие как диатомовые водоросли и радиолярии , выделяют скелетные структуры, состоящие из кремнезема. Кремнезем откладывается во многих тканях растений. [13]
Из-за обилия кремния в земной коре природные материалы на основе кремния использовались на протяжении тысячелетий. Кремниевые горные кристаллы были знакомы различным древним цивилизациям , например, додинастическим египтянам , которые использовали их для изготовления бус и небольших ваз , а также древним китайцам . Стекло , содержащее кремнезем, производилось египтянами, по крайней мере, с 1500 г. до н. э., а также древними финикийцами . Природные силикатные соединения также использовались в различных типах раствора для строительства древних человеческих жилищ . [14]

В 1787 году Антуан Лавуазье предположил, что кремнезем может быть оксидом фундаментального химического элемента , [15] но химическое сродство кремния к кислороду настолько велико, что у него не было возможности восстановить оксид и изолировать элемент. [16] После попытки изолировать кремний в 1808 году сэр Хамфри Дэви предложил название «кремний» для кремния, от латинского silex , silicis для кремня, и добавив окончание «-ium», потому что он считал, что это металл. [17] В большинстве других языков используются транслитерированные формы имени Дэви, иногда адаптируемые к местной фонологии (например, немецкий Silizium , турецкий silisyum , каталонский silici , армянский ցիում или Silitzioum ). Некоторые другие вместо этого используют кальку латинского корня (например, русский кремний от кремень «кремень»; греческий πυρίτιο от πυρ «огонь»; финский pii от piikivi «кремень», чешский křemík от křemen «кварц», «кремень»). . [18]
Считается, что Гей-Люссак и Тенар получили нечистый аморфный кремний в 1811 году путем нагревания недавно выделенного металлического калия с тетрафторидом кремния , но они не очистили и не охарактеризовали продукт, а также не идентифицировали его как новый элемент. [19] Свое нынешнее название кремний получил в 1817 году шотландским химиком Томасом Томсоном . Он сохранил часть имени Дэви, но добавил «-он», потому что считал кремний неметаллом , подобным бору и углероду . [20] В 1824 году Йонс Якоб Берцелиус получил аморфный кремний, используя примерно тот же метод, что и Гей-Люссак (восстановление фторосиликата калия расплавленным металлическим калием), но очищая продукт до коричневого порошка путем многократной промывки. [21] В результате ему обычно отдают должное за открытие элемента. [22] [23] В том же году Берцелиус первым получил тетрахлорид кремния ; Тетрафторид кремния был получен уже задолго до этого, в 1771 году, Карлом Вильгельмом Шееле путем растворения кремнезема в плавиковой кислоте . [16] В 1823 году Якоб Берцелиус впервые открыл тетрахлорид кремния (SiCl 4 ). [24] В 1846 году фон Эбельман синтезировал тетраэтилортосиликат (Si(OC 2 H 5 ) 4 ). [25] [24]
Кремний в его более распространенной кристаллической форме был получен только 31 год спустя Девиллем . [26] [27] Путем электролиза смеси хлорида натрия и хлорида алюминия , содержащей примерно 10% кремния, он смог получить слегка примесный аллотроп кремния в 1854 году . [28] Позже были разработаны более экономически эффективные методы изолировать несколько аллотропных форм, последней из которых был силицен в 2010 году. [29] [30] Тем временем исследования по химии кремния продолжались; Фридрих Велер открыл первые летучие гидриды кремния, синтезировав трихлорсилан в 1857 году и сам силан в 1858 году, но детальное исследование силанов было проведено только в начале 20 века Альфредом Стоком , несмотря на ранние предположения по этому поводу, датированные еще как начало синтетической органической химии в 1830-х годах. [31] [32] Точно так же первое кремнийорганическое соединение , тетраэтилсилан, было синтезировано Чарльзом Фриделем и Джеймсом Крафтсом в 1863 году, но детальная характеристика кремнийорганической химии была сделана только в начале 20 века Фредериком Киппингом . [16]
Начиная с 1920-х годов, работы Уильяма Лоуренса Брэгга по рентгеновской кристаллографии прояснили состав силикатов, которые ранее были известны из аналитической химии, но еще не были поняты, вместе с развитием кристаллохимии Лайнусом Полингом и Виктором Развитие геохимии Гольдшмидтом . В середине 20 в. развивается химия и промышленное применение силоксанов , растет применение кремнийорганических полимеров , эластомеров и смол . В конце 20 века была нанесена на карту сложность кристаллохимии силицидов , а также физика твердого тела легированных полупроводников . [16]
Первые полупроводниковые устройства использовали не кремний, а галенит , в том числе кристаллический детектор немецкого физика Фердинанда Брауна в 1874 году и радиокристаллический детектор индийского физика Джагадиша Чандры Бозе в 1901 году. [33] [34] Первым кремниевым полупроводниковым устройством был кремниевый радиокристаллический детектор, разработанный американским инженером Гринлифом Уиттиером Пикардом в 1906 году. [34]
В 1940 году Рассел Ол открыл p–n-переход и фотоэлектрические эффекты в кремнии. В 1941 году технологии производства кристаллов германия и кремния высокой чистоты были разработаны для кристаллов радиолокационных микроволновых детекторов во время Второй мировой войны . [33] В 1947 году физик Уильям Шокли выдвинул теорию полевого усилителя, сделанного из германия и кремния, но ему не удалось построить работающее устройство, прежде чем в конечном итоге вместо этого начать работать с германием. Первым работающим транзистором был транзистор с точечным контактом, созданный Джоном Бардином и Уолтером Брэттеном позже в том же году, когда они работали под руководством Шокли. [35] В 1954 году физико-химик Моррис Таненбаум изготовил первый кремниевый переходной транзистор в Bell Labs . [36] В 1955 году Карл Фрош и Линкольн Дерик из Bell Labs случайно обнаружили, что диоксид кремния ( SiO
2) можно было выращивать на кремнии [37] , а позже в 1958 году они предположили, что это может маскировать поверхности кремния во время диффузионных процессов . [38]
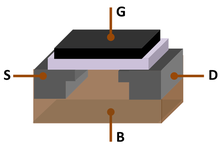
«Кремниевый век» относится к концу 20-го – началу 21-го века. [39] [40] [41] Это связано с тем, что кремний был доминирующим материалом Кремниевого века (также известного как век цифровых технологий или век информации ), аналогично тому, как каменный век , бронзовый век и железный век были определены доминирующие материалы в соответствующие эпохи цивилизации . [39]
Поскольку кремний является важным элементом в высокотехнологичных полупроводниковых устройствах, многие места в мире носят его имя. Например, долина Санта-Клара в Калифорнии получила прозвище «Силиконовая долина» , поскольку этот элемент является там базовым материалом в полупроводниковой промышленности . С тех пор подобное название получили многие другие места, в том числе Силиконовые Вади в Израиле; Кремниевый лес в Орегоне; Силиконовые холмы в Остине, штат Техас; Силиконовые склоны в Солт-Лейк-Сити, штат Юта; Кремниевая Саксония в Германии; Кремниевая долина в Индии; Кремниевая граница в Мехикали, Мексика; Silicon Fen в Кембридже, Англия; Силиконовая карусель в Лондоне; Силиконовая Глен в Шотландии; Силиконовое ущелье в Бристоле, Англия; Силиконовая аллея в Нью-Йорке; и Силиконовый пляж в Лос-Анджелесе. [42]

Атом кремния имеет четырнадцать электронов . В основном состоянии они расположены в электронной конфигурации [Ne]3s 2 3p 2 . Из них четыре являются валентными электронами , занимающими 3s-орбиталь и два 3p-орбитали. Как и другие члены его группы, более легкий углерод и более тяжелый германий , олово и свинец , он имеет такое же количество валентных электронов, как и валентные орбитали: следовательно, он может завершить свой октет и получить стабильную конфигурацию благородного газа аргона путем образуя гибридные орбитали sp 3 , образуя тетраэдрические SiX
4производные, в которых центральный атом кремния разделяет электронную пару с каждым из четырех атомов, с которыми он связан. [44] Первые четыре энергии ионизации кремния составляют 786,3, 1576,5, 3228,3 и 4354,4 кДж/моль соответственно; эти цифры достаточно высоки, чтобы исключить возможность простой катионной химии этого элемента. Следуя периодическим тенденциям , его ковалентный радиус одинарной связи 117,6 пм занимает промежуточное положение между радиусами углерода (77,2 пм) и германия (122,3 пм). Шестикоординационный ионный радиус кремния можно считать равным 40 пм, хотя это следует воспринимать как чисто условную цифру, учитывая отсутствие простого Si4+
катион в реальности. [45]
При стандартных температуре и давлении кремний представляет собой блестящий полупроводник с голубовато-серым металлическим блеском; что типично для полупроводников, его удельное сопротивление падает с повышением температуры. Это происходит потому, что кремний имеет небольшую энергетическую щель ( зону проводимости ) между самыми высокими занятыми энергетическими уровнями (валентной зоной) и самыми низкими незанятыми уровнями (зоной проводимости). Уровень Ферми находится примерно посередине между валентной зоной и зоной проводимости и представляет собой энергию, при которой состояние может быть занято электроном с такой же вероятностью, как и нет. Следовательно, чистый кремний эффективно является изолятором при комнатной температуре. Однако легирование кремния пниктогеном, таким как фосфор , мышьяк или сурьма , вводит один дополнительный электрон на легирующую примесь, и они затем могут быть возбуждены в зоне проводимости термически или фотолитически, создавая полупроводник n-типа . Точно так же легирование кремния элементом 13-й группы, таким как бор , алюминий или галлий , приводит к появлению акцепторных уровней, которые захватывают электроны, которые могут быть возбуждены из заполненной валентной зоны, создавая полупроводник p-типа . [46] Соединение кремния n-типа с кремнием p-типа создает p – n-переход с общим уровнем Ферми; электроны текут от n к p, а дырки – от p к n, создавая падение напряжения. Таким образом, этот p – n-переход действует как диод , который может выпрямлять переменный ток, что позволяет току легче проходить в одну сторону, чем в другую. Транзистор представляет собой n-p-n-переход с тонким слоем кремния слабо p-типа между двумя областями n-типа . Смещение эмиттера на небольшое прямое напряжение и коллектора на большое обратное напряжение позволяет транзистору действовать как триодный усилитель. [46]
Кремний кристаллизуется в гигантской ковалентной структуре при стандартных условиях, в частности в кубической кристаллической решетке алмаза ( пространственная группа 227 ). Таким образом, он имеет высокую температуру плавления 1414 ° C, поскольку для разрыва прочных ковалентных связей и плавления твердого тела требуется много энергии. При плавлении кремний сжимается, поскольку дальнодействующая тетраэдрическая сеть связей распадается, а пустоты в этой сети заполняются, подобно водяному льду, когда водородные связи разрываются при плавлении. Он не имеет термодинамически стабильных аллотропов при стандартном давлении, но известно несколько других кристаллических структур при более высоких давлениях. Общая тенденция заключается в увеличении координационного числа с давлением, кульминацией которого является образование гексагонального плотноупакованного аллотропа с плотностью около 40 гигапаскалей , известного как Si-VII (стандартная модификация - Si-I). Аллотроп под названием BC8 (или bc8), имеющий объемноцентрированную кубическую решетку с восемью атомами на примитивную элементарную ячейку ( пространственная группа 206 ), может быть создан при высоком давлении и остается метастабильным при низком давлении. Его свойства детально изучены. [47]
Кремний кипит при 3265 °C: хотя это и высокая температура, она все же ниже температуры, при которой сублимируется его более легкий родственный углерод (3642 °C), а кремний также имеет более низкую теплоту испарения, чем углерод, что согласуется с тем фактом, что кремний Связь Si слабее связи C–C. [46]
Также возможно построить слои силицена , аналогичные графену . [29] [30]
Природный кремний состоит из трех стабильных изотопов : 28 Si (92,23%), 29 Si (4,67%) и 30 Si (3,10%). [48] Из них только 29 Si используется в спектроскопии ЯМР и ЭПР , [49] поскольку он единственный имеет ядерный спин ( I =1/2). [31] Все три образуются в сверхновых типа Ia [50] [51] в процессе сжигания кислорода , при этом 28 Si образуется как часть альфа-процесса и, следовательно, является наиболее распространенным. Слияние 28 Si с альфа-частицами путем фоторасщепления в звездах известно как процесс горения кремния ; это последняя стадия звездного нуклеосинтеза перед быстрым коллапсом и сильным взрывом рассматриваемой звезды в сверхновой типа II . [52]
Охарактеризовано двадцать радиоизотопов , два самых стабильных из которых — 32 Si с периодом полураспада около 150 лет и 31 Si с периодом полураспада 2,62 часа. [48] Все остальные радиоактивные изотопы имеют период полураспада менее семи секунд, а у большинства из них период полураспада составляет менее одной десятой секунды. [48] Кремний имеет один известный ядерный изомер , 34m Si, с периодом полураспада менее 210 наносекунд. [48] 32 Si подвергается низкоэнергетическому бета-распаду до 32 P , а затем до стабильного 32 S. 31 Si может быть получен нейтронной активацией природного кремния и поэтому полезен для количественного анализа; его можно легко обнаружить по его характерному бета-распаду до стабильного 31 P , в котором испускаемый электрон несет энергию до 1,48 МэВ . [31]
Известные изотопы кремния имеют массовое число от 22 до 44. [48] Наиболее распространенным способом распада изотопов с массовыми числами ниже, чем у трех стабильных изотопов, является обратный бета-распад , в первую очередь с образованием изотопов алюминия (13 протонов) в качестве продуктов распада. . [48] Наиболее распространенным способом распада более тяжелых нестабильных изотопов является бета-распад, в результате которого в качестве продуктов распада в первую очередь образуются изотопы фосфора (15 протонов). [48]
Кремний может попадать в океаны через грунтовые воды и речной транспорт. Большие потоки поступления подземных вод имеют изотопный состав, отличный от поступления кремния из речных источников. Изотопные вариации в подземных водах и речном переносе способствуют вариациям океанических значений 30 Si. В настоящее время наблюдаются существенные различия в изотопном составе глубоководных вод бассейнов мирового океана . Между Атлантическим и Тихим океанами существует глубоководный градиент 30 Si, превышающий 0,3 части на тысячу. 30 Si чаще всего ассоциируется с продуктивностью океанов. [53]
Кристаллический массивный кремний довольно инертен, но становится более реакционноспособным при высоких температурах. Как и его сосед алюминий, кремний образует тонкий сплошной поверхностный слой диоксида кремния ( SiO
2), защищающий металл от окисления. Таким образом, кремний не вступает в реакцию с воздухом при температуре ниже 900 °C, но образование стекловидного диоксида быстро увеличивается между 950 °C и 1160 °C, а когда достигается 1400 °C, атмосферный азот также вступает в реакцию с образованием нитридов SiN и Si.
3Н
4. Кремний реагирует с газообразной серой при 600 °С и газообразным фосфором при 1000 °С. Тем не менее, этот оксидный слой не предотвращает реакцию с галогенами ; фтор энергично атакует кремний при комнатной температуре, хлор — при температуре около 300 °C, а бром и йод — при температуре около 500 °C. Кремний не реагирует с большинством водных кислот, но окисляется и образует комплексы смесями плавиковой кислоты , содержащими хлор или азотную кислоту, с образованием гексафторсиликатов . Он легко растворяется в горячей водной щелочи с образованием силикатов . [54] При высоких температурах кремний также реагирует с алкилгалогенидами ; эта реакция может катализироваться медью для прямого синтеза кремнийорганических хлоридов в качестве предшественников кремнийорганических полимеров. При плавлении кремний становится чрезвычайно реакционноспособным, сплавляясь с большинством металлов с образованием силицидов и восстанавливая большинство оксидов металлов, поскольку теплота образования диоксида кремния очень велика. Фактически расплавленный кремний реагирует практически со всеми известными материалами тигля (кроме собственного оксида SiO ).
2). [55] : 13 Это происходит из-за высоких сил связывания кремния для легких элементов и его высокой растворяющей способности для большинства элементов. [55] : 13 В результате контейнеры для жидкого кремния должны быть изготовлены из тугоплавких , инертных материалов, таких как диоксид циркония или бориды 4, 5 и 6 групп. [46] [56]
Тетраэдрическая координация является основным структурным мотивом в химии кремния, как и в химии углерода. Однако подоболочка 3p гораздо более размыта, чем подоболочка 2p, и не так хорошо гибридизуется с подоболочкой 3s. В результате химия кремния и его более тяжелых родственников существенно отличается от химии углерода [57] , и, таким образом, октаэдрическая координация также важна. [46] Например, электроотрицательность кремния (1,90) намного меньше, чем у углерода (2,55), потому что валентные электроны кремния находятся дальше от ядра, чем у углерода, и, следовательно, испытывают меньшие электростатические силы притяжения со стороны ядра. . Плохое перекрытие 3p-орбиталей также приводит к гораздо меньшей склонности к катенации (образованию связей Si-Si) для кремния, чем для углерода, из-за сопутствующего ослабления связи Si-Si по сравнению со связью C-C: [58] ] средняя энергия связи Si–Si составляет примерно 226 кДж/моль по сравнению со значением 356 кДж/моль для связи C–C. [59] Это приводит к тому, что соединения кремния с многократными связями обычно гораздо менее стабильны, чем их углеродные аналоги, что является примером правила двойной связи . С другой стороны, наличие радиальных узлов на 3p-орбиталях кремния предполагает возможность гипервалентности , как это видно в пяти- и шестикоординатных производных кремния, таких как SiX .−
5и СиФ2−
6. [60] [58] Наконец, из-за увеличения энергетического разрыва между валентными s- и p-орбиталями по мере спуска группы важность двухвалентного состояния возрастает от углерода к свинцу, так что для кремния известно несколько нестабильных двухвалентных соединений; это понижение основной степени окисления в сочетании с увеличением атомных радиусов приводит к усилению металлического характера вниз по группе. Кремний уже проявляет некоторое начальное металлическое поведение, особенно в поведении его оксидных соединений и реакции с кислотами и основаниями (хотя это требует некоторых усилий), и поэтому его часто называют металлоидом, а не неметаллом. [58] Германий показывает больше, а олово обычно считается металлом. [16]
Кремний демонстрирует явные отличия от углерода. Например, органическая химия имеет очень мало аналогий с химией кремния, в то время как силикатные минералы обладают структурной сложностью, невиданной у оксоуглеродов . [61] Кремний имеет тенденцию напоминать германий гораздо больше, чем углерод, и это сходство усиливается за счет сжатия d-блока , в результате чего размер атома германия оказывается намного ближе к размеру атома кремния, чем можно было бы предсказать по периодическим тенденциям. [62] Тем не менее, некоторые различия все же существуют из-за растущей важности двухвалентного состояния в германии по сравнению с кремнием. Кроме того, более низкая прочность связи Ge-O по сравнению с прочностью связи Si-O приводит к отсутствию «германоновых» полимеров, которые были бы аналогичны силиконовым полимерам. [59]

Кремний является восьмым по распространенности элементом во Вселенной после водорода , гелия , углерода , азота , кислорода , железа и неона . Это изобилие не очень хорошо воспроизводится на Земле из-за существенного разделения элементов, произошедшего во время формирования Солнечной системы . Кремний составляет 27,2% земной коры по массе, уступая только кислороду с 45,5%, с которым он всегда связан в природе. Дальнейшее фракционирование произошло при формировании Земли путем планетарной дифференциации : ядро Земли , составляющее 31,5% массы Земли, имеет приблизительный состав Fe.
25Ни
2Ко
0,1С
3; мантия составляет 68,1% массы Земли и состоит в основном из более плотных оксидов и силикатов, например оливина ( Mg, Fe) .
2SiO
4; в то время как более легкие кремнистые минералы, такие как алюмосиликаты , поднимаются на поверхность и образуют кору, составляя 0,4% массы Земли. [63] [64]
Кристаллизация магматических пород из магмы зависит от ряда факторов; среди них химический состав магмы, скорость охлаждения и некоторые свойства отдельных минералов, которые будут образовываться, такие как энергия решетки , температура плавления и сложность их кристаллической структуры. По мере охлаждения магмы первым появляется оливин , за ним следуют пироксен , амфибол , биотитовая слюда, ортоклазовый полевой шпат , мусковитовая слюда , кварц , цеолиты и, наконец, гидротермальные минералы. Эта последовательность демонстрирует тенденцию к усложнению силикатных единиц с охлаждением и введением гидроксидных и фторид -анионов в дополнение к оксидам. Многие металлы могут заменить кремний. После того, как эти магматические породы подвергаются выветриванию , переносу и отложению, образуются осадочные породы, такие как глина, сланец и песчаник. Метаморфизм также может происходить при высоких температурах и давлениях, создавая еще большее разнообразие минералов. [63]
Существует четыре источника поступления кремния в океан: химическое выветривание континентальных пород, речной транспорт, растворение континентальных терригенных силикатов и реакция между подводными базальтами и гидротермальными флюидами, выделяющими растворенный кремний. Все четыре этих потока взаимосвязаны в биогеохимическом цикле океана, поскольку все они изначально образовались в результате выветривания земной коры. [65]
Ежегодно в мировой океан выбрасывается примерно 300–900 мегатонн эоловой пыли. Из этой стоимости 80–240 мегатонн приходится на твердый кремний. Общий объем выпадений кремния в океан в виде твердых частиц по-прежнему меньше, чем объем притока кремния в океан речным транспортом. [66] Эоловые поступления литогенного кремния в виде частиц в Северную Атлантику и западную часть северной части Тихого океана являются результатом оседания пыли в океанах из пустыни Сахары и Гоби соответственно. [65] Речной транспорт является основным источником притока кремния в океан в прибрежных регионах, в то время как на отложение кремния в открытом океане большое влияние оказывает оседание эоловой пыли. [66]
Кремний чистотой 96–99% получают карботермическим восстановлением кварцита или песка коксом высокой чистоты . Восстановление проводят в электродуговой печи с избытком SiO .
2используется для предотвращения накопления карбида кремния (SiC): [31]

Эта реакция, известная как карботермическое восстановление диоксида кремния, обычно проводится в присутствии железного лома с низким содержанием фосфора и серы , образуя ферросилиций . [31] Ферросилиций, железо-кремниевый сплав, который содержит различные соотношения элементарного кремния и железа, составляет около 80% мирового производства элементарного кремния, при этом Китай, ведущий поставщик элементарного кремния, обеспечивает 4,6 миллиона тонн (или 2 /третей мирового производства) кремния, большая часть которого находится в форме ферросилиция. За ней следуют Россия (610 000 т), Норвегия (330 000 т), Бразилия (240 000 т) и США (170 000 т). [67] Ферросилиций в основном используется в черной металлургии (см. ниже) в качестве легирующей добавки в чугуне или стали, а также для раскисления стали на металлургических заводах. [31]
Другая реакция, иногда используемая, представляет собой алюминотермическое восстановление диоксида кремния следующим образом: [68]
При выщелачивании порошкообразного кремния чистотой 96–97% водой получается кремний чистотой ~98,5%, который используется в химической промышленности. Однако для полупроводниковых применений необходима еще большая чистота, и ее получают восстановлением тетрахлорсилана (тетрахлорида кремния) или трихлорсилана . Первый изготавливается путем хлорирования кремниевого лома, а второй является побочным продуктом производства силикона . Эти соединения летучи и, следовательно, могут быть очищены путем многократной фракционной перегонки с последующим восстановлением до элементарного кремния с использованием очень чистого металлического цинка в качестве восстановителя. Полученные таким образом губчатые кусочки кремния плавятся, а затем выращиваются с образованием цилиндрических монокристаллов, а затем очищаются зонным рафинированием . Другие пути используют термическое разложение силана или тетраиодсилана ( SiI
4). Другой используемый процесс — восстановление гексафторосиликата натрия , обычного отхода производства фосфатных удобрений, металлическим натрием : он сильно экзотермичен и, следовательно, не требует внешнего источника энергии. Сверхтонкий кремний производится с более высокой чистотой, чем почти любой другой материал: производство транзисторов требует уровня примесей в кристаллах кремния менее 1 части на 10 10 , а в особых случаях необходимы и достигаются уровни примесей ниже 1 части на 10 12 . [31]
Кремниевые наноструктуры могут быть изготовлены непосредственно из кварцевого песка с использованием традиционных металлотермических процессов или метода синтеза горением. Такие наноструктурированные кремниевые материалы можно использовать в различных функциональных применениях, включая анод литий-ионных батарей (LIB) или фотокаталитические приложения. [69]
Большая часть кремния используется в промышленности без очистки, часто со сравнительно небольшой переработкой его естественной формы. Более 90% земной коры состоит из силикатных минералов , которые представляют собой соединения кремния и кислорода, часто с ионами металлов, когда отрицательно заряженные силикатные анионы требуют катионов для уравновешивания заряда. Многие из них имеют прямое коммерческое использование, например, глины, кварцевый песок и большинство видов строительного камня. Таким образом, подавляющее большинство применений кремния приходится на использование в качестве структурных соединений, либо в виде силикатных минералов, либо в виде кремнезема (сырого диоксида кремния). Силикаты используются при производстве портландцемента (состоящего в основном из силикатов кальция), который используется в строительном растворе и современной штукатурке , но, что более важно, в сочетании с кварцевым песком и гравием (обычно содержащим силикатные минералы, такие как гранит), для изготовления бетона , который является основой большинства крупнейших промышленных строительных проектов современного мира. [70]
Кремнезем используется для изготовления огнеупорного кирпича , разновидности керамики. Силикатные минералы также присутствуют в белой керамике — важном классе изделий, обычно содержащих различные типы обожженных глинистых минералов (природные слоистые силикаты алюминия). Примером является фарфор , в основе которого лежит силикатный минерал каолинит . Традиционное стекло (натриево- известковое стекло на основе кремнезема ) также функционирует во многом таким же образом, а также используется для изготовления окон и контейнеров. Кроме того, специальные стекловолокна на основе диоксида кремния используются для производства оптического волокна , а также для производства стекловолокна для структурной поддержки и стекловаты для теплоизоляции .
Силиконы часто используются в гидроизоляционных материалах, формовочных массах, антиадгезивах , механических уплотнениях, высокотемпературных смазках и восках, а также в составах для уплотнения . Силикон также иногда используется в грудных имплантатах , контактных линзах, взрывчатых веществах и пиротехнике . [71] Первоначально Silly Putty изготавливалась путем добавления борной кислоты в силиконовое масло . [72] Другие соединения кремния действуют как высокотехнологичные абразивы и новая высокопрочная керамика на основе карбида кремния . Кремний входит в состав некоторых суперсплавов .
Элементарный кремний добавляется в расплавленный чугун в виде сплавов ферросилиция или кремнекальция для улучшения характеристик при отливке тонких сечений и предотвращения образования цементита при воздействии наружного воздуха. Присутствие элементарного кремния в расплавленном железе действует как поглотитель кислорода, поэтому содержание углерода в стали, которое необходимо поддерживать в узких пределах для каждого типа стали, можно более тщательно контролировать. Производство и использование ферросилиция контролирует сталелитейную промышленность, и хотя эта форма элементарного кремния сильно загрязнена, на ее долю приходится 80% мирового использования свободного кремния. Кремний является важным компонентом электротехнической стали , изменяя ее удельное сопротивление и ферромагнитные свойства.
Свойства кремния могут быть использованы для модификации сплавов другими металлами, кроме железа. Кремний «металлургического сорта» — это кремний чистотой 95–99%. Около 55% мирового потребления кремния металлургической чистоты идет на производство алюминиево-кремниевых сплавов ( силуминовых сплавов) для отливок алюминиевых деталей , главным образом для использования в автомобильной промышленности . Важность кремния при литье алюминия заключается в том, что значительное количество кремния (12%) в алюминии образует эвтектическую смесь , которая затвердевает с очень небольшим термическим сжатием. Это значительно уменьшает разрывы и трещины, образующиеся в результате напряжений при охлаждении литейных сплавов до затвердевания. Кремний также значительно повышает твердость и, следовательно, износостойкость алюминия. [73] [74]

Большая часть производимого элементарного кремния остается в виде сплава ферросилиция, и только около 20% очищается до металлургической чистоты (всего 1,3–1,5 миллиона метрических тонн / год). По оценкам, 15% мирового производства кремния металлургического качества подвергается дальнейшей очистке до полупроводниковой чистоты. [74] Обычно это «девять-9» или чистота 99,9999999%, [75] практически бездефектный монокристаллический материал . [76]
Монокристаллический кремний такой чистоты обычно производится методом Чохральского и используется для производства кремниевых пластин, используемых в полупроводниковой промышленности , в электронике, а также в некоторых дорогостоящих и высокоэффективных фотоэлектрических приложениях. [77] Чистый кремний является собственным полупроводником , а это означает, что в отличие от металлов он проводит электронные дырки и электроны, высвобождаемые из атомов под действием тепла; Электропроводность кремния увеличивается с повышением температуры. Чистый кремний имеет слишком низкую проводимость (то есть слишком высокое удельное сопротивление ), чтобы его можно было использовать в качестве элемента схемы в электронике. На практике чистый кремний легируют небольшими концентрациями некоторых других элементов, которые значительно увеличивают его проводимость и регулируют его электрический отклик, контролируя количество и заряд ( положительный или отрицательный ) активированных носителей. Такой контроль необходим для транзисторов , солнечных элементов , полупроводниковых детекторов и других полупроводниковых устройств, используемых в компьютерной индустрии и других технических приложениях. [78] В кремниевой фотонике кремний может использоваться в качестве среды рамановского лазера непрерывного действия для производства когерентного света. [79]
В обычных интегральных схемах пластина монокристаллического кремния служит механической опорой для схем, которые создаются путем легирования и изолируются друг от друга тонкими слоями оксида кремния , изолятора, который легко изготавливается на поверхности Si с помощью процессов термического окисления . или локальное окисление (LOCOS) , которое предполагает воздействие на элемент кислорода в соответствующих условиях, которые можно предсказать с помощью модели Дила-Гроува . Кремний стал самым популярным материалом как для мощных полупроводников, так и для интегральных схем, поскольку он может выдерживать самые высокие температуры и наибольшую электрическую активность, не подвергаясь лавинному пробою ( электронная лавина создается, когда тепло создает свободные электроны и дырки, которые, в свою очередь, пропускают больший ток). , который производит больше тепла). Кроме того, изолирующий оксид кремния не растворяется в воде, что дает ему преимущество перед германием (элементом с аналогичными свойствами, который также может использоваться в полупроводниковых устройствах) при определенных технологиях изготовления. [80]
Производство монокристаллического кремния дорогое, и его использование обычно оправдано только при производстве интегральных схем, где крошечные дефекты кристалла могут мешать работе крошечных цепей. Для других целей могут быть использованы другие типы чистого кремния. К ним относятся гидрогенизированный аморфный кремний и улучшенный кремний металлургического класса (UMG-Si), используемый в производстве недорогой электроники большой площади в таких приложениях, как жидкокристаллические дисплеи , а также недорогие тонкопленочные солнечные панели большой площади. клетки . Такие полупроводниковые сорта кремния либо немного менее чисты, либо являются поликристаллическими, а не монокристаллическими, и производятся в сопоставимых количествах с монокристаллическим кремнием: от 75 000 до 150 000 метрических тонн в год. Рынок меньшего сорта кремния растет быстрее, чем рынок монокристаллического кремния. По прогнозам, к 2013 году производство поликристаллического кремния, используемого в основном в солнечных элементах, достигнет 200 000 метрических тонн в год, в то время как ожидается, что производство монокристаллического кремния полупроводникового качества останется менее 50 000 тонн в год. [74]
Кремниевые квантовые точки создаются путем термической обработки водородного силсесквиоксана в нанокристаллы размером от нескольких нанометров до нескольких микрон, демонстрирующие люминесцентные свойства, зависящие от размера. [81] [82] Нанокристаллы демонстрируют большие стоксовы сдвиги , преобразующие фотоны ультрафиолетового диапазона в фотоны видимого или инфракрасного диапазона, в зависимости от размера частиц, что позволяет использовать их в дисплеях с квантовыми точками и люминесцентных солнечных концентраторах из-за их ограниченного самопоглощения. Преимущество использования квантовых точек на основе кремния по сравнению с кадмием или индием заключается в нетоксичности и отсутствии металлов в кремнии. [83] [84] Еще одним применением кремниевых квантовых точек является обнаружение опасных материалов. Датчики используют люминесцентные свойства квантовых точек за счет гашения фотолюминесценции в присутствии опасного вещества. [85] Существует множество методов, используемых для определения опасных химических веществ, некоторые из которых включают перенос электронов, резонансный перенос энергии флуоресценции и генерацию фототока. [86] Тушение электронного переноса происходит, когда нижняя незанятая молекулярная орбиталь (LUMO) имеет немного меньшую энергию, чем зона проводимости квантовой точки, что обеспечивает перенос электронов между ними и предотвращает рекомбинацию дырок и электронов внутри нанокристаллов. . Эффект также может быть достигнут обратным, если молекула-донор имеет высшую занятую молекулярную орбиталь (ВЗМО) немного выше края валентной зоны квантовой точки, что позволяет электронам перемещаться между ними, заполняя дырки и предотвращая рекомбинацию. Резонансный перенос энергии флуоресценции происходит, когда между квантовой точкой и молекулой-гасителем образуется комплекс. Комплекс будет продолжать поглощать свет, но когда энергия преобразуется в основное состояние, он не испускает фотон, гасящий материал. Третий метод использует другой подход: вместо мониторинга фотолюминесцентного дисплея измеряется фототок , излучаемый квантовыми точками. Если концентрация желаемого химического вещества увеличивается, фототок, излучаемый нанокристаллами, в ответ изменится. [87]

Хотя кремний легко доступен в форме силикатов , очень немногие организмы используют его напрямую. Диатомовые водоросли , радиолярии и кремнистые губки используют биогенный кремнезем в качестве структурного материала для своих скелетов. Некоторые растения накапливают кремнезем в своих тканях и нуждаются в кремнии для роста, например рис . Кремний может поглощаться растениями в виде ортокремниевой кислоты (также известной как монокремниевая кислота) и транспортироваться через ксилему , где он образует аморфные комплексы с компонентами клеточной стенки. Было показано, что это улучшает прочность клеточных стенок и структурную целостность некоторых растений, тем самым уменьшая количество насекомых-травоядных и патогенных инфекций. В некоторых растениях кремний может также усиливать выработку летучих органических соединений и фитогормонов, которые играют важную роль в защитных механизмах растений. [90] [91] [92] У более развитых растений фитолиты кремнезема (фитолиты опала) представляют собой твердые микроскопические тела, встречающиеся в клетке. [93] [94] [91]
Известно, что некоторые садовые культуры защищают себя от грибковых патогенов растений с помощью кремнезема до такой степени, что применение фунгицидов может оказаться неэффективным, если не сопровождается достаточным количеством кремния. Кремнеземные защитные молекулы растений активируют некоторые фитоалексины , то есть некоторые из них являются сигнальными веществами, вызывающими приобретенный иммунитет . При недостатке некоторые растения заменяют его увеличенным производством других защитных веществ. [91]
Жизнь на Земле в основном состоит из углерода , но астробиология считает, что внеземная жизнь может иметь и другие гипотетические типы биохимии . Кремний считается альтернативой углероду, так как он может создавать сложные и стабильные молекулы с четырьмя ковалентными связями, необходимыми для ДНК -аналога, и доступен в больших количествах. [95]
Диатомовые водоросли используют кремний в форме биогенного кремнезема (bSi), [96] который поглощается белком-транспортером кремния (SIT) и преимущественно используется в структуре клеточной стенки в виде панцирей. [97] Кремний попадает в океан в растворенной форме, такой как кремниевая кислота или силикат. [98] Поскольку диатомеи являются одними из основных потребителей этих форм кремния, они вносят большой вклад в концентрацию кремния по всему океану. Кремний образует профиль питательных веществ в океане из-за продуктивности диатомей на небольших глубинах. [98] Следовательно, концентрация кремния ниже в мелководном океане и выше в глубоком океане.
Продуктивность диатомовых водорослей в верхних слоях океана способствует увеличению количества кремния, экспортируемого в нижние слои океана. [99] Когда клетки диатомовых водорослей лизируются в верхних слоях океана, их питательные вещества, такие как железо, цинк и кремний, передаются в нижние слои океана посредством процесса, называемого морским снегом . Морской снег предполагает перенос твердых частиц органического вещества вниз за счет вертикального смешивания растворенного органического вещества. [100] Было высказано предположение, что кремний имеет решающее значение для продуктивности диатомовых водорослей, и пока существует кремниевая кислота, доступная для использования диатомовыми водорослями, диатомовые водоросли также могут способствовать концентрации других важных питательных веществ в глубоком океане. [101]
В прибрежных зонах диатомеи служат основными фитопланктонными организмами и вносят большой вклад в производство биогенного кремнезема. Однако в открытом океане роль диатомовых водорослей в ежегодном мировом производстве кремнезема снижается. Диатомовые водоросли в субтропических круговоротах Северной Атлантики и Северной Тихого океана обеспечивают лишь около 5-7% мирового ежегодного производства морского кремнезема. Южный океан производит около одной трети мирового морского биогенного кремнезема. [65] Южный океан называют «биогеохимическим водоразделом» [102], поскольку из этого региона выносится лишь незначительное количество кремния.
Существуют некоторые доказательства того, что кремний важен для здоровья человека, поскольку он влияет на его ногти, волосы, кости и кожные ткани [103] , например, в исследованиях, которые показывают, что женщины в пременопаузе, которые потребляют больше кремния с пищей, имеют более высокую плотность костей и что добавки кремния может увеличить объем и плотность костей у пациентов с остеопорозом . [104] Кремний необходим для синтеза эластина и коллагена , наибольшее количество которых в организме человека содержится в аорте , [105] и считается важным элементом ; [106] тем не менее, трудно доказать его необходимость, поскольку кремний очень распространен, и, следовательно, симптомы дефицита трудно воспроизвести. [107] [108]
В настоящее время Ассоциация американских чиновников по контролю за продуктами питания для растений (AAPFCO) рассматривает вопрос о повышении кремния до статуса «полезного для растений вещества». [109] [110]
Люди могут подвергнуться воздействию элементарного кремния на рабочем месте, вдыхая его, проглатывая или контактируя с кожей или глазами. В последних двух случаях кремний представляет небольшую опасность в качестве раздражителя. Это опасно при вдыхании. [111] Управление по охране труда (OSHA) установило законный предел воздействия кремния на рабочем месте на уровне 15 мг/м 3 общего воздействия и 5 мг/м 3 воздействия на органы дыхания в течение восьмичасового рабочего дня. Национальный институт безопасности и гигиены труда (NIOSH) установил рекомендуемый предел воздействия (REL) на уровне 10 мг/м 3 общего воздействия и 5 мг/м 3 воздействия на органы дыхания в течение восьмичасового рабочего дня. [112] Вдыхание пыли кристаллического кремнезема может привести к силикозу — профессиональному заболеванию легких, характеризующемуся воспалением и рубцеванием в виде узловых поражений в верхних долях легких . [113]
Для компании Excell Minerals была проведена презентация о признании кремния признанным питательным веществом для растений.
{{cite book}}: |journal=игнорируется ( помощь )