Этинилэстрадиол ( ЭЭ ) – препарат эстрогена , который широко используется в противозачаточных таблетках в сочетании с прогестинами . [7] [8] В прошлом ЭЭ широко использовался по различным показаниям, таким как лечение симптомов менопаузы , гинекологических заболеваний и некоторых гормоночувствительных видов рака . Обычно его принимают внутрь , но также используют в виде пластыря и вагинального кольца . [7] [12]
Общие побочные эффекты ЭЭ включают, среди прочего, болезненность и увеличение груди , головную боль , задержку жидкости и тошноту . [7] У мужчин ЭЭ может дополнительно вызывать развитие молочных желез , феминизацию в целом, гипогонадизм и сексуальную дисфункцию . Редкие, но серьезные побочные эффекты включают образование тромбов , повреждение печени и рак матки . [7]
ЭЭ является эстрогеном или агонистом рецепторов эстрогена , биологической мишени эстрогенов, таких как эстрадиол . [7] Это синтетическое производное эстрадиола , природного эстрогена, и отличается от него по-разному. [7] По сравнению с эстрадиолом, ЭЭ более устойчив к метаболизму , имеет значительно улучшенную биодоступность при пероральном приеме и демонстрирует относительно повышенное воздействие на определенные части тела, такие как печень и матка . [7] Эти различия делают ЭЭ более подходящим для использования в противозачаточных таблетках, чем эстрадиол, хотя также приводят к повышенному риску образования тромбов и некоторым другим редким побочным эффектам. [7]
ЭЭ был разработан в 1930-х годах и был введен в медицинское применение в 1943 году. [13] [14] Препарат начал использоваться в противозачаточных таблетках в 1960-х годах. [15] Сегодня ЭЭ содержится почти во всех комбинированных формах противозачаточных таблеток и является почти единственным эстрогеном, используемым для этой цели, что делает его одним из, если не наиболее широко используемых эстрогенов. [16] [17]
Есть много применений для EE. Чаще всего он используется в качестве контрацепции в комбинированных оральных контрацептивах (КОК), также известных как противозачаточные средства , для предотвращения беременности после секса. ЭЭ в составе противозачаточных средств не только используется для предотвращения беременности, но также может использоваться для лечения отсутствия менструации, симптомов во время менструации и прыщей .
ЭЭ также используется в качестве менопаузальной гормональной терапии . [18] Основной причиной использования ЗГТ у женщин в период менопаузы является облегчение распространенных вазомоторных симптомов, таких как приливы , ночная потливость и приливы . Исследования показали, что замена эстрогена помогает улучшить эти симптомы по сравнению с плацебо. [19] Другие распространенные симптомы менопаузы, такие как сухость влагалища (которая может вызывать боль во время полового акта), вагинальный зуд и депрессивное настроение, могут принести пользу от ЗГТ. Помимо лечения симптомов менопаузы, ЭЭ используется в качестве компонента феминизирующей гормональной терапии для трансгендерных женщин . [20] Однако он больше не используется и не рекомендуется для этой цели, поскольку его в значительной степени вытеснил эстрадиол . [20]
ЭЭ также можно использовать для лечения гипогонадизма у женщин, профилактики остеопороза у женщин и в качестве паллиативной помощи при раке простаты у мужчин и раке молочной железы у женщин. [8] [21] Его также использовали для снижения полового влечения у сексуальных преступников . [22] [23]
ЭЭ или любой эстроген в отдельности противопоказаны женщинам с маткой из-за повышенного риска рака эндометрия ; назначение прогестагена с эстрогеном снижает риск. [24]
ЭЭ доступен в сочетании с прогестином в большом количестве КОК. [25] Он также доступен в сочетании с прогестинами в виде трансдермального противозачаточного пластыря и противозачаточного вагинального кольца . [12] Кроме того, существует единственный препарат (торговая марка FemHRT), содержащий очень низкие дозы ЭЭ (2,5 и 5 мкг) плюс прогестин в пероральной таблетке , который до сих пор используется для гормональной терапии в период менопаузы. [12] [18] ЭЭ ранее был доступен отдельно под торговыми марками, такими как Эстинил и Линорал, в форме 0,002, 0,01, 0,02, 0,025, 0,05, 0,1, 0,5 и 1,0 мг (2, 10, 20, 25, 50). , 100, 500 и 1000 мкг) таблетки. [26] [27] [28] [29] [30]
Количество ЭЭ в КОК с годами сократилось. [8] Ранее КОК содержали высокие дозы ЭЭ – до 100 мкг/день. [31] Дозы более 50 мкг ЭЭ считаются высокими дозами, дозы 30 и 35 мкг ЭЭ считаются низкими дозами, а дозы от 10 до 25 мкг ЭЭ считаются очень низкими дозами. [32] Сегодня КОК обычно содержат от 10 до 50 мкг ЭЭ. [32] Более высокие дозы ЭЭ были прекращены из-за высокого риска ВТЭ и сердечно-сосудистых проблем. [31]
ЭЭ следует избегать лицам с историей или известной предрасположенностью к артериальному или венозному тромбозу ( сгусткам крови ) из-за повышенного риска сердечно-сосудистых проблем, таких как венозная тромбоэмболия (ВТЭ), инфаркт миокарда и ишемический инсульт . [33] Сюда входят женщины с:
За исключением случаев, когда ЭЭ используется для лечения, следует избегать применения ЭЭ у женщин с текущим раком молочной железы из-за возможного ухудшения прогноза. [34]
Также следует избегать ЭЭ у кормящих женщин, у которых срок после родов составляет менее 21 дня, из-за повышенного риска ВТЭ. [35] Использование ЭЭ кормящими грудью женщинами в течение как минимум 21 дня после родов должно быть обсуждено с врачом и включать информацию о преимуществах, недостатках и альтернативах использования ЭЭ. [35]
Из-за риска холестатической гепатотоксичности широко распространено мнение, что КОК, содержащие ЭЭ, следует избегать у женщин с холестазом беременности в анамнезе , опухолями печени , активным гепатитом и семейными дефектами желчевыделения. [36]
Тяжесть побочных эффектов может варьироваться в зависимости от дозы и пути введения ЭЭ. [40] Общие побочные эффекты ЭЭ такие же, как и у других эстрогенов, и включают болезненность молочных желез , головную боль , задержку жидкости ( вздутие живота ), тошноту , головокружение и увеличение веса . [10] [36] Эстрогеновый компонент пероральных контрацептивов, который почти всегда представляет собой ЭЭ, может вызывать болезненность и полноту груди . [26] У мужчин ЭЭ имеет дополнительные побочные эффекты, включая гинекомастию (развитие молочных желез), феминизацию в целом, гипогонадизм , бесплодие и сексуальную дисфункцию (например, снижение либидо и эректильную дисфункцию ). У мужчин, получавших терапию высокими дозами эстрогенов (200 мкг/день перорального ЭЭ в течение более трех месяцев), гинекомастия наблюдалась в 98% случаев, а снижение либидо - в 42–73%. [41]
ВТЭ представляет собой тромб в вене и включает тромбоз глубоких вен (ТГВ) и легочную эмболию (ЛЭ). [7] [43] [44] Известно, что эстрогены повышают риск ВТЭ из-за их влияния на синтез в печени факторов свертывания крови . [7] [43] [44] ЭЭ несет в себе больший риск образования тромбов и ВТЭ, чем природный эстрадиол , что, как полагают, связано со структурными различиями между двумя соединениями и различной восприимчивостью к инактивации печени . [7]
По оценкам метаанализа 2012 года , абсолютный риск ВТЭ составляет 2 на 10 000 женщин при неиспользовании, 8 на 10 000 женщин при приеме ЭЭ и противозачаточных таблеток, содержащих левоноргестрел , и от 10 до 15 на 10 000 женщин при приеме противозачаточных таблеток, содержащих ЭЭ и левоноргестрел. прогестин третьего или четвертого поколения , такой как дезогестрел или дроспиренон . [45] Для сравнения, абсолютный риск ВТЭ обычно оценивается от 1 до 5 на 10 000 женщин-лет при неиспользовании, от 5 до 20 на 10 000 женщин-лет при беременности и от 40 до 65 на 10 000 женщин-лет при неиспользовании. послеродовой период. [45] Современные КОК связаны с примерно в 2–4 раза более высоким риском ВТЭ, чем их неиспользование. [45] Путь введения ЭЭ, по-видимому, не влияет на риск ВТЭ, поскольку противозачаточные вагинальные кольца и противозачаточные пластыри , содержащие ЭЭ/прогестин, имеют такой же или даже более высокий риск ВТЭ, чем КОК. [45] [46] Беременность связана с увеличением риска ВТЭ примерно в 4,3 раза. [45] Подсчитано, что по меньшей мере от 300 до 400 здоровых молодых женщин умирают каждый год в Соединенных Штатах из-за ВТЭ, вызванной противозачаточными таблетками, содержащими ЭЭ. [47]
Современные КОК содержат от 10 до 35 мкг ЭЭ, но обычно 20, 30 или 35 мкг. [45] [48] Первоначальные составы КОК, появившиеся на рынке в 1960-х годах, содержали от 100 до 150 мкг ЭЭ. [49] [39] [48] Однако вскоре было обнаружено, что ЭЭ связана с повышенным риском ВТЭ и что этот риск зависит от дозы. [48] После этих событий доза ЭЭ была значительно снижена и теперь всегда составляет менее 50 мкг. [50] [51] [52] Эти более низкие дозы значительно снижают риск ВТЭ без потери контрацептивной эффективности. [48] Герстман и др. (1991) обнаружили, что КОК, содержащие более 50 мкг ЭЭ, имели в 1,7 раза, а КОК, содержащие 50 мкг ЭЭ, в 1,5 раза больший риск ВТЭ, чем КОК, содержащие менее 50 мкг. [37] Кокрейновский обзор 2014 года показал, что КОК, содержащие 50 мкг ЭЭ с левоноргестрелом, имеют в 2,1–2,3 раза больший риск, чем КОК, содержащие 30 мкг или 20 мкг ЭЭ с левоноргестрелом соответственно. [45] КОК, содержащие 20 мкг ЭЭ, также связаны со значительно меньшим риском сердечно-сосудистых событий, чем КОК, содержащие 30 или 40 мкг ЭЭ. [53] Однако прекращение приема КОК чаще происходит при дозах ЭЭ от 10 до 20 мкг из-за проблемных изменений в характере кровотечений. [54]
Женщины с тромбофилией имеют значительно более высокий риск ВТЭ при использовании контрацепции, содержащей ЭЭ, чем женщины без тромбофилии. [45] [46] В зависимости от состояния риск ВТЭ может быть увеличен в 5–50 раз по сравнению с неиспользованием препарата у таких женщин. [45] [46]
Уровни глобулина, связывающего половые гормоны (ГСПГ), указывают на воздействие эстрогенов на печень и могут быть суррогатным маркером риска свертывания крови и ВТЭ при терапии эстрогенами, хотя эта тема обсуждается. [55] [56] [57] Уровни ГСПГ при приеме противозачаточных таблеток, содержащих различные прогестины, повышаются в 1,5–2 раза при приеме левоноргестрела , в 2,5–4 раза при приеме дезогестрела и гестодена , в 3,5–4 раза при приеме дроспиренона и диеногеста . и в 4–5 раз с ацетатом ципротерона . [55] Противозачаточные вагинальные кольца и противозачаточные пластыри также повышают уровень ГСПГ в 2,5 и 3,5 раза соответственно. [55] Противозачаточные таблетки, содержащие высокие дозы этинилэстрадиола (>50 мкг), могут повысить уровень ГСПГ в 5–10 раз, что аналогично повышению, которое происходит во время беременности. [58] И наоборот, повышение уровня ГСПГ намного ниже при приеме эстрадиола , особенно при парентеральном применении. [59] [60] [61] [62] [63] Было обнаружено, что высокие дозы парентеральной терапии полиэстрадиолфосфатом повышают уровень ГСПГ примерно в 1,5 раза. [62]
При пероральном применении в высоких дозах, например, в качестве терапии высокими дозами эстрогенов у мужчин с раком простаты и у женщин с раком молочной железы, синтетические и небиоидентичные эстрогены , такие как ЭЭ и диэтилстильбэстрол , связаны с довольно высокой частотой тяжелых сердечно-сосудистых осложнений . такие как ВТЭ, инфаркт миокарда и инсульт . [21] [64] [65] Диэтилстильбэстрол связан с риском сердечно-сосудистой токсичности и смерти до 35%, а также с 15%-ной частотой ВТЭ у мужчин, получавших его по поводу рака простаты. [64] [65] ЭЭ имеет в некоторой степени меньший риск сердечно-сосудистых осложнений, чем диэтилстильбэстрол при использовании при лечении рака простаты у мужчин. [8] Тем не менее, как ЭЭ, так и диэтилстильбэстрол оказывают крайне непропорциональное воздействие на синтез белка в печени , что, как полагают, является причиной их сердечно-сосудистой токсичности. [7] [65]
В отличие от пероральных синтетических эстрогенов, таких как ЭЭ и диэтилстильбестрол, высокие дозы полиэстрадиолфосфата и трансдермального эстрадиола не повышают риск сердечно-сосудистой смертности или тромбоэмболии у мужчин с раком простаты. [65] [66] [67] Однако при применении высоких доз полиэстрадиолфосфата наблюдалось значительное увеличение сердечно-сосудистой заболеваемости . [65] [66] [67] В любом случае эти эстрогены считаются гораздо более безопасными, чем пероральные синтетические эстрогены, такие как ЭЭ и диэтилстильбэстрол. [65] [66] [67] Кроме того, сульфонат этинилэстрадиола (ЭЭС), пероральный, но парентеральный пролекарство длительного действия, используется при лечении рака простаты и, как говорят, имеет значительно лучший профиль сердечно-сосудистая безопасность, чем EE. [8]
Из-за непропорционального воздействия на синтез белка в печени и связанных с ним сердечно-сосудистых рисков синтетические эстрогены, такие как ЭЭ и диэтилстильбэстрол, больше не используются в гормональной терапии в период менопаузы. [8] Их также заменяют парентеральными формами эстрадиола, такими как полиэстрадиолфосфат и трансдермальный эстрадиол при лечении рака простаты. [65]
В более низких дозах, которые сейчас используются в противозачаточных таблетках, ЭЭ редко ассоциировался с холестатической гепатотоксичностью , подобно 17α-алкилированным андрогенам / анаболическим стероидам и 17α-этинилированным прогестинам 19-нортестостерона . [68] [69] Холестаз может проявляться в виде зуда и желтухи . [70] Глюкуронидные метаболиты ЭЭ, воздействуя на белки ABCB11 (BSEP) и MRP2 (ABCC2) и, как следствие, изменяя отток желчи и экскрецию солей желчи , по-видимому, ответственны за холестаз. [71] Очень высокие концентрации эстрадиола через его метаболит эстрадиола глюкуронид также участвуют в холестазе, например, в холестазе беременных . [69] Однако частота и тяжесть холестатической гепатотоксичности, по-видимому, намного выше при использовании ЭЭ, чем при использовании эстрадиола, что, как полагают, связано с реактивным замещением этинила C17α в ЭЭ, а также с его значительно сниженной восприимчивостью к печеночному метаболизму. [36] [72] В то время как отклонения от нормы функциональных проб печени (LFT) обычно обнаруживаются примерно у 1% женщин, не принимающих противозачаточные таблетки или принимающих противозачаточные таблетки с низкими дозами ЭЭ, это число увеличивается до более чем 10% женщин, принимающих противозачаточные таблетки. противозачаточные таблетки, содержащие 50 мкг ЭЭ/день или более. [72] [70] При приеме противозачаточных таблеток, содержащих 50 мкг/день ЭЭ, уровень аланинаминотрансферазы (АЛТ) увеличивается на 50%, гематокрит - на 19%, лейкоцитов - на 50%, а гамма-глутамилтрансфераза (ГГТ) снижается на 30% . [72] Однако значения обычно остаются в пределах нормы. [72] Помимо аномальных показателей LFT, у половины женщин, принимающих противозачаточные таблетки с 50 мкг/день ЭЭ, могут наблюдаться патологические изменения в частичных функциях печени и морфологии печени. [72] Противозачаточные таблетки, содержащие ЭЭ, также были связаны с 25-50-кратным увеличением риска редких доброкачественных опухолей печени и 3-6-кратным увеличением риска гепатоцеллюлярной карциномы , [70] [72 ] 73] [74] , а также повышенный риск других осложнений со стороны печени. [75] [76] В свое время считалось, что противозачаточные таблетки, содержащие ЭЭ, являются причиной 84% всех связанных с наркотиками и гистологически подтвержденных повреждений печени. [72] Однако в настоящее время эти риски снижаются с помощью современных противозачаточных таблеток с более низкими дозами ЭЭ, содержащих 35 мкг ЭЭ в день или меньше. [70] [74]
Высокие дозы ЭЭ, которые использовались в ранних КОК, были связаны со значительно повышенным риском рака эндометрия при применении некоторых препаратов, например, тех, которые содержат прогестаген диметистерон . [77] Не встречающие сопротивления эстрогены, такие как ЭЭ, оказывают канцерогенное действие на эндометрий, а прогестагены защищают от этих эффектов, но диметистерон является относительно слабым прогестагеном и не способен адекватно противодействовать канцерогенным эффектам ЭЭ на эндометрий, что, в свою очередь, приводит к повышенному риску рака эндометрия. . [77] КОК, содержащие диметистерон, с тех пор были прекращены (вместо них использовались более мощные прогестагены), а дозы ЭЭ в КОК в целом были резко снижены, что устранило риск. [77] В свою очередь, большинство исследований современных КОК выявили снижение риска рака эндометрия. [78]
Сточные воды содержат различные эстрогены, в том числе ЭЭ, которые не полностью расщепляются при очистке сточных вод . [79] Поступление искусственных эстрогенов в пресноводные экосистемы влияет на популяции рыб и земноводных . Хроническое воздействие низких уровней ЭЭ в течение семи лет привело к исчезновению популяции толстоголовых гольянов в экспериментальном озере в Онтарио, Канада . [79] ЭЭ изменил оогенез у самок рыб и феминизированных самцов рыб так, что они продуцировали белок, связанный с созреванием икры, вителлогенин , а также икру на ранних стадиях. [79] У амфибий воздействие ЭЭ может снизить успешность вылупления и изменить развитие гонад . [80] Воздействие гормонов может изменить развитие гонад лягушек, даже если это закодировано в их генах . [80] Исследование норковых лягушек выявило больше головастиков -интерсексуалов у тех, кто экспериментально подвергался воздействию ЭЭ, чем у тех, кто не подвергался воздействию ЭЭ, а у зеленых лягушек показатели успешного вылупления были гораздо ниже. [80]
Эстрогены, такие как ЭЭ, относительно безопасны при острой передозировке . [ нужна цитата ]
ЭЭ метаболизируется некоторыми изоформами цитохрома P450 , включая CYP3A4 и CYP2C9 . [81] Таким образом, индукторы ферментов, таких как CYP3A4, могут снижать циркулирующие концентрации ЭЭ. [36] Примеры индукторов включают противосудорожные средства, такие как фенитоин , примидон , этосуксимид , фенобарбитал и карбамазепин ; азольные противогрибковые средства , такие как флуконазол ; и антибиотики рифамицина , такие как рифампицин ( рифампицин ). [36] И наоборот, ингибиторы CYP3A4 и других ферментов цитохрома P450 могут повышать уровни ЭЭ в крови. [36] Примером является тролеандомицин , который является мощным и высокоселективным ингибитором CYP3A4. [36]
Было обнаружено, что парацетамол (ацетаминофен) конкурентно ингибирует сульфатирование ЭЭ, при этом предварительное введение 1000 мг парацетамола значительно увеличивает уровни AUC ЭЭ (на 22%) и снижает уровни AUC сульфата этинилэстрадиола (сульфата ЭЭ) у женщин. [36] То же самое было обнаружено для аскорбиновой кислоты (витамина С) и ЭЭ, хотя значимость взаимодействия считалась сомнительной. [36]
В отличие от эстрадиола, маловероятно, что существует фармакокинетическое взаимодействие между курением (которое мощно индуцирует определенные ферменты цитохрома P450 и заметно увеличивает 2-гидроксилирование эстрадиола) и ЭЭ. [36] Это говорит о том, что эстрадиол и ЭЭ метаболизируются различными ферментами цитохрома P450. [36] Однако существует повышенный риск сердечно-сосудистых осложнений при курении и ЭЭ, как и в случае курения и других эстрогенов. [36]
Известно, что ЭЭ ингибирует несколько ферментов цитохрома P450 , включая CYP1A2 , CYP2B6 , CYP2C9 , CYP2C19 и CYP3A4 , и, возможно, является индуктором CYP2A6 . [82] В результате это может повлиять на метаболизм и концентрацию многих других лекарств. [82] Примеры известных взаимодействий включают бупропион , кофеин , мефенитоин , мидазолам , никотин , нифедипин , омепразол , пропранолол , прогуанил , селегилин , теофиллин и тизанидин . [82] [36] Одним из наиболее заметных взаимодействий является то, что ЭЭ сильно повышает уровень селегилина , субстрата CYP2B6 и CYP2C19. [82] ЭЭ может также индуцировать глюкуронидацию и, возможно, изменять сульфатирование . [82] Было обнаружено, что он увеличивает клиренс и снижает концентрацию различных глюкуронидированных препаратов. [82] Примеры включают клофибрат , ламотриджин , лоразепам , оксазепам и пропранолол . [82]
Известно также, что прогестины, которые часто используются в сочетании с ЭЭ, ингибируют ферменты цитохрома Р450, и это также может способствовать взаимодействию лекарств с контрацептивами, содержащими ЭЭ. [82] Примеры включают гестоден , дезогестрел и этоногестрел , которые являются ингибиторами CYP3A4 и CYP2C19. [82] Кроме того, известно, что эти прогестины постепенно ингибируют метаболизм и повышают концентрацию самого ЭЭ. [36]
ЭЭ представляет собой эстроген, аналогичный природным эстрогенам, таким как эстрадиол, конъюгированным эстрогенам (премарин) и синтетическим эстрогенам, таким как диэтилстильбэстрол . Он связывается и активирует обе изоформы рецептора эстрогена , ERα и ERβ . [8] В одном исследовании было обнаружено , что EE имеет 233% и 38% сродства эстрадиола к ERα и ERβ соответственно. [83] В другом исследовании было обнаружено, что он обладает 194% и 151% сродством эстрадиола к ERα и ERβ соответственно. [84] ЭЭ также, по-видимому, действует как мощный агонист рецептора эстрогена, связанного с G-белком (GPER) (аффинность неизвестна), мембранного рецептора эстрогена , аналогично эстрадиолу. [85] [86] [87] [88] Эстрогены оказывают антигонадотропное действие за счет активации ERα. [89] В качестве контрацептива ЭЭ действует совместно с прогестином, подавляя всплеск лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) в середине цикла посредством своего антигонадотропного действия, тем самым ингибируя фолликулогенез и предотвращая овуляцию и, следовательно, возможность беременности . _ [90] [91]
ЭЭ представляет собой эстроген длительного действия с задержкой в ядре около 24 часов. [38]
При пероральном приеме ЭЭ примерно в 100 раз более эффективен по массе, чем природные эстрогены, такие как микронизированный эстрадиол и конъюгированные эстрогены, что во многом обусловлено значительно большей устойчивостью к метаболизму первого прохождения . [92] [93] [94] В частности, он в 80–200 раз более эффективен, чем эстропипат (сульфат пиперазина эстрона), который имеет аналогичную эффективность с микронизированным эстрадиолом с точки зрения системной эстрогенной активности. [95] [96] Напротив, эффективность ЭЭ и натуральных эстрогенов аналогична при внутривенном введении из-за обхода метаболизма первого прохождения. [48] По сравнению с его пролекарством местранолом , ЭЭ примерно в 1,7 раза более эффективен по массе при пероральном приеме. [93]

ЭЭ является мощным функциональным антиандрогеном как у женщин, так и у мужчин. [117] Он опосредует свои антиандрогенные эффекты путем 1) стимуляции выработки глобулина , связывающего половые гормоны (ГСПГ) в печени , что снижает концентрацию свободного и, следовательно, биоактивного тестостерона в крови; и 2) подавлением секреции лютеинизирующего гормона (ЛГ) гипофизом , что снижает выработку тестостерона половыми железами . [117] [118] [25] [119] Противозачаточные таблетки, содержащие ЭЭ, полезны при лечении андроген-зависимых состояний, таких как прыщи и гирсутизм , благодаря их антиандрогенному действию. [117] [120]
Было обнаружено, что противозачаточные таблетки, содержащие ЭЭ, снижают общий уровень тестостерона у женщин в среднем на 30%, повышают уровень циркулирующего ГСПГ в среднем примерно в 3 раза (но варьируется в зависимости от прогестина, увеличивается в диапазоне от 1,5 до 5 раз). и снизить концентрацию свободного тестостерона в среднем на 60% (диапазон от 40 до 80%). [121] [55] [122] [25] Противозачаточные таблетки, содержащие высокие дозы ЭЭ, могут повысить уровень ГСПГ у женщин в 5–10 раз. [58] Это похоже на 5-10-кратное увеличение уровня ГСПГ, которое происходит во время беременности . [58] Из-за заметного повышения уровня ГСПГ уровень свободного тестостерона становится очень низким во время лечения противозачаточными таблетками, содержащими ЭЭ. [10] Исследование у мужчин показало, что лечение относительно низкой дозой 20 мкг/день ЭЭ в течение пяти недель повышало уровень циркулирующего ГСПГ на 150% и, из-за сопутствующего снижения уровня свободного тестостерона, повышало общий уровень циркулирующего тестостерона. на 50% (за счет усиления выработки тестостерона гонадами за счет снижения отрицательной обратной связи андрогенов на оси гипоталамус-гипофиз-гонады ). [118] Стимуляция выработки ГСПГ в печени с помощью ЭЭ гораздо сильнее, чем с другими эстрогенами, такими как эстрадиол, из-за высокой устойчивости ЭЭ к инактивации в печени и, следовательно, его непропорционального воздействия в этой части тела. [7] [10] [123]
Эстрогены являются антигонадотропинами и способны подавлять секрецию ЛГ и ФСГ гипофизом и, как следствие, выработку тестостерона гонадами. [124] [125] Терапия высокими дозами эстрогена , в том числе ЭЭ, способна подавить уровень тестостерона у мужчин примерно на 95% или до уровня кастрации/женщины. [126] [124] [125] Дозировка ЭЭ, необходимая для использования в качестве компонента гормональной терапии для предоперационных трансгендерных женщин, составляет от 50 до 100 мкг/день. [127] Эта высокая дозировка связана с высокой частотой ВТЭ, особенно у людей старше 40 лет, и было сказано, что ее не следует использовать. [127] Дозировка ЭЭ, используемая при лечении рака простаты у мужчин, составляет от 150 до 1000 мкг/день (0,15–1,0 мг/день). [8] [128] Было обнаружено, что доза ЭЭ в размере 50 мкг два раза в день (всего 100 мкг/день) подавляет уровень тестостерона у мужчин в такой же степени, как и 3 мг/день перорального диэтилстильбестрола , что является минимальной дозой диэтилстильбестрола. требуется для последовательного подавления уровня тестостерона до кастрационного уровня. [129] Доза ЭЭ, подавляющая овуляцию, сама по себе, а не в сочетании с прогестином, у женщин составляет 100 мкг/день. [130] [131] Однако было обнаружено, что его эффективность в ингибировании овуляции составляет от 75 до 90% при дозировке 20 мкг/день и примерно на 97 или 98% при дозировке 50 мкг/день. [132] [133] [134] [135] В другом исследовании овуляция произошла у 25,2% при дозе ЭЭ 50 мкг/день. [136]
Более низкие дозы ЭЭ также оказывают значительное антигонадотропное действие. [127] «Очень низкая» доза ЭЭ в 15 мкг/день была описана как «пограничная» доза, необходимая для подавления уровней ЛГ и тестостерона у мужчин, а исследование показало, что уровни ЛГ и тестостерона «надежно» подавлялись у мужчин. мужчинам в дозировке 30 мкг/сут ЭЭ. [8] Однако другие клинические исследования показали, что 20 мкг/день ЭЭ повышают уровень тестостерона на 50% у мужчин (как описано выше) [118] и что дозы 32 мкг/день и 42 мкг/день ЭЭ подавляют уровень ФСГ у мужчин. мужчин, но существенно не влиял на уровень ЛГ. [8] Более сильное подавление уровня тестостерона наблюдалось у мужчин после ежедневного лечения комбинированными пероральными контрацептивами, содержащими 50 мкг этинилэстрадиола и 0,5 мг норгестрела , в течение 9 дней. [8] Однако исследование показало, что прогестин был более важным компонентом, ответственным за подавление уровня тестостерона. [8] Соответственно, прогестиновый компонент КОК в первую очередь отвечает за подавление овуляции у женщин. [8] Было обнаружено , что комбинация 20 мкг/день ЭЭ и 10 мг/день метилтестостерона подавляет секрецию ФСГ у мужчин до степени, достаточной для остановки сперматогенеза . [8] Исследования на женщинах показали, что 50 мкг ЭЭ в день подавляют уровни ЛГ и ФСГ примерно на 70% у женщин в постменопаузе. [96]
Помимо антигонадотропного действия ЭЭ может существенно подавлять выработку андрогенов надпочечниками в высоких концентрациях. [8] [137] [138] Одно исследование показало, что лечение высокой дозой ЭЭ в 100 мкг/день подавляло уровень циркулирующих надпочечниковых андрогенов на 27–48% у трансгендерных женщин. [8] [137] [138] Это может дополнительно способствовать подавлению уровня андрогенов эстрогенами. [8] [137] [138]
ЭЭ оказывает заметное влияние на синтез белка в печени даже при низких дозах и независимо от пути введения . [8] [7] Эти эффекты опосредованы его эстрогенной активностью. [8] [7] Препарат дозозависимо увеличивает циркулирующие уровни ГСПГ, кортикостероидсвязывающего глобулина (КБГ) и тироксинсвязывающего глобулина (ТБГ), а также влияет на широкий спектр других белков печени. [8] [7] ЭЭ влияет на уровень триглицеридов при дозе всего 1 мкг/день и на уровни холестерина ЛПНП и ЛПВП при дозе всего 2,5 мкг/день. [139] ЭЭ влияет на несколько белков печени даже в дозе 5 мкг/день. [8] При дозах выше 20 мкг/день дополнительное влияние ЭЭ на синтез белка в печени становится все меньше. [8]
Было обнаружено, что ЭЭ в дозе 5 мкг/день повышает уровень ГСПГ на 100% у женщин в постменопаузе, тогда как дозировка ЭЭ в дозе 20 мкг/день повышает его на 200%. [8] Андрогены снижают выработку ГСПГ в печени и, как было обнаружено, противодействуют влиянию ЭЭ на уровни ГСПГ. [8] Это приобретает особую актуальность, если учесть, что многие прогестины, используемые в КОК, обладают различной степенью слабой андрогенной активности. [8] Комбинация 20 мкг/день ЭЭ и 0,25 мг/день левоноргестрела , прогестина с относительно высокой андрогенностью, снижает уровень ГСПГ на 50%; 30 мкг/день ЭЭ и 0,25 мг/день левоноргестрела не влияют на уровень ГСПГ; 30 мкг ЭЭ/день и 0,15 мг/день левоноргестрела повышают уровень ГСПГ на 30%; а трехфазные КОК, содержащие ЭЭ и левоноргестрел, повышают уровень ГСПГ на 100–150%. [8] Комбинация 30 мкг/день ЭЭ и 150 мкг/день дезогестрела , прогестина с относительно слабой андрогенностью, чем левоноргестрел, повышает уровень ГСПГ на 200%, тогда как комбинация 35 мкг/день ЭЭ и 2 мг/день ацетата ципротерона , прогестин с мощной антиандрогенной активностью, повышает уровень ГСПГ на 400%. [8] Таким образом, тип и дозировка прогестина, содержащегося в КОК, эффективно смягчают влияние ЭЭ на уровень ГСПГ. [8]
Было обнаружено, что доза 10 мкг ЭЭ/день повышает уровень CBG на 50%, а доза 20 мкг ЭЭ/день повышает его на 100%. [8] Прогестины, являющиеся производными прогестерона, не влияют на уровни CBG, в то время как андрогенные прогестины, такие как производные 19-нортестостерона, оказывают лишь слабое влияние на уровни CBG. [8] КОК могут повысить уровень КБГ на 100–150%. [8] Было обнаружено, что доза ЭЭ в 5 мкг/день повышает уровень ТБГ на 40%, а доза ЭЭ в 20 мкг/день повышает их на 60%. [8] Прогестины, являющиеся производными прогестерона, не влияют на уровень ТБГ, тогда как прогестины с андрогенной активностью могут снижать уровни ТБГ. [8] Было обнаружено , что комбинация 30 мкг/день ЭЭ и 1 мг/день норэтистерона , умеренно андрогенного прогестина, повышает уровень ТБГ на 50–70%, в то время как комбинация 30 мкг/день ЭЭ и 150 мкг/день дезогестрел увеличил их на 100%. [8]


ЭЭ оказывает сильное и непропорциональное влияние на синтез белка в печени по сравнению с эстрадиолом. [7] Печень , а также матка экспрессируют 17β-гидроксистероиддегидрогеназу (17β-HSD), и этот фермент служит для инактивации эстрадиола и эффективного подавления его активности в этих тканях, обратимо превращая его в гораздо менее мощный эстроген эстрон (который примерно 4% эстрогенной активности эстрадиола). [7] В отличие от эстрадиола, 17α-этинильная группа ЭЭ предотвращает окисление положения ЭЭ С17β 17β-HSD, и по этой причине ЭЭ не инактивируется в этих тканях и обладает в них гораздо более сильной относительной эстрогенной активностью. [7] [140] [11] Это механизм непропорционально сильного воздействия ЭЭ на выработку белка в печени, [7] [140] что приводит к значительному увеличению величины воздействия на ВТЭ и сердечно-сосудистые риски по сравнению с эстрадиолом. [141]
С другой стороны, из-за потери инактивации ЭЭ с помощью 17β-HSD в эндометрии (матке) ЭЭ относительно более активен, чем эстрадиол в эндометрии, и по этой причине связан со значительно более низкой частотой вагинальных кровотечений. и пятнистость в сравнении. [7] Это особенно справедливо в случае комбинированной терапии эстрогенами и прогестагенами (например, КОК или менопаузальной ЗГТ), поскольку прогестагены индуцируют экспрессию 17β-HSD в эндометрии. [7] Уменьшение вагинальных кровотечений и кровянистых выделений при приеме ЭЭ является одной из основных причин его использования в КОК вместо эстрадиола, [3] несмотря на его потенциально более низкий профиль безопасности (связанный с его неблагоприятным воздействием на синтез белка в печени и ВТЭ). заболеваемость). [142]
Было обнаружено, что ЭЭ оказывает непропорциональное влияние на синтез белка в печени и риск ВТЭ, независимо от того, является ли путь введения пероральным, трансдермальным или вагинальным, что указывает на то, что использование парентерального пути вместо перорального не приводит к пропорциональному действию ЭЭ на печень. относительно непеченочных действий. [140] [8] Однако влияние ЭЭ на синтез белка в печени в любом случае снижается при парентеральном введении. [8] Было обнаружено, что доза 10 мкг/день вагинального ЭЭ эквивалентна 50 мкг перорального ЭЭ с точки зрения воздействия на синтез белка в печени, например, стимуляция выработки печеночным ГСПГ. [8] Таким образом, было обнаружено, что парентеральный ЭЭ, который обходит первое прохождение через печень, которое происходит при пероральном ЭЭ, оказывает в 5 раз меньшее влияние на синтез белка в печени по весу, чем пероральный ЭЭ. [8] В отличие от ЭЭ, а также перорального эстрадиола, трансдермальный эстрадиол практически не оказывает влияния на синтез белка в печени при типичных дозировках в период менопаузы. [7]
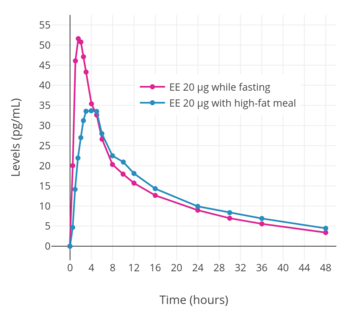
Пероральная биодоступность ЭЭ составляет в среднем 45% с широким диапазоном от 20% до 74% (хотя чаще всего от 38 до 48%) , что обусловлено высокой межиндивидуальной вариабельностью . [10] [4] Хотя биодоступность ЭЭ при пероральном приеме относительно низкая, она значительно выше, чем у микронизированного эстрадиола (5%). [2] [10] Было обнаружено , что после однократного приема ЭЭ в дозе 20 мкг в сочетании с 2 мг норэтистерона ацетата у женщин в постменопаузе концентрации ЭЭ достигают максимума 50 пг/мл в среднем за 1,5 часа. [7] После первой дозы средние уровни ЭЭ в целом дополнительно увеличиваются примерно на 50%, пока не будут достигнуты равновесные концентрации ; [7] [143] Равновесное состояние достигается через неделю ежедневного приема. [8] Для сравнения, средние пиковые уровни эстрадиола, достигаемые при приеме 2 мг микронизированного эстрадиола или валерата эстрадиола, составляют 40 пг/мл после первой дозы и 80 пг/мл после трех недель приема. [7] Эти максимальные концентрации эстрадиола находятся в том же диапазоне, что и концентрации ЭЭ, которые образуются при пероральном приеме ЭЭ, которая в 100 раз ниже по весу, что соответствует примерно 100-кратному увеличению эффективности ЭЭ при пероральном приеме. относительно эстрадиола. [92] [7] В соответствии с высокой межиндивидуальной вариабельностью пероральной биодоступности ЭЭ, существует большая степень межиндивидуальных различий в уровнях ЭЭ. [7] [144] Было обнаружено, что доза ЭЭ 50 мкг/день позволяет достичь широкого диапазона уровней ЭЭ в крови, от примерно 100 до 2000 пг/мл. [145] [144] Было обнаружено, что прием ЭЭ в сочетании с пищей с высоким содержанием жиров значительно снижает его пиковые концентрации. [143] [7]
Уровни ЭЭ после однократного приема 50 мкг внутривенной инъекции в несколько раз выше, чем уровни ЭЭ после однократного приема 50 мг перорально. [145] Помимо разницы в уровнях, процесс исключения для обоих маршрутов аналогичен. [145]
В фармакокинетике ЭЭ могут существовать гендерные различия , например, ЭЭ может иметь более высокую эффективность при пероральном приеме у женщин, чем у мужчин. [8] Исследование показало, что комбинация 60 мкг/день ЭЭ и 0,25 мг/день левоноргестрела у женщин и мужчин приводила к пиковым уровням ЭЭ 495 пг/мл и 251 пг/мл ( уровни площади под кривой). ЭЭ 6,216 пг/мл/час и 2,850 пг/мл/час, а период полувыведения 16,5 часов и 10,2 часов соответственно. [8] Было высказано предположение, что это явление может представлять собой «механизм защиты» мужчин от воздействия эстрогена из окружающей среды . [8]
Связывание ЭЭ с белками плазмы составляет от 97 до 98%, и он связывается почти исключительно с альбумином . [5] [7] [10] [146] В отличие от эстрадиола, который связывается с высоким сродством к SHBG, EE имеет очень низкое сродство к этому белку, около 2% от сродства к эстрадиолу, и, следовательно, не связывается с ним существенно. [147]
Из-за высокого метаболизма первого прохождения в кишечнике и печени только 1% пероральной дозы ЭЭ попадает в кровоток в виде самого ЭЭ. [7] Во время метаболизма первого прохождения ЭЭ активно конъюгируется посредством глюкуронидации и сульфатирования с образованием гормонально инертных глюкуронидов этинилэстрадиола и сульфата этинилэстрадиола (сульфат ЭЭ), а уровни сульфата ЭЭ в кровообращении в 6-22 раза выше, чем у ЭЭ-сульфата. ЭЭ. [7] [4] Для сравнения: при пероральном приеме 2 мг микронизированного эстрадиола уровни эстрона и сульфата эстрона в 4-6 и 200 раз выше, чем уровни эстрадиола соответственно. [7] В отличие от эстрадиола, ЭЭ из-за стерических затруднений со стороны его этинильной группы C17α не метаболизируется и не инактивируется 17β-HSD, [11] и это основной фактор, ответственный за резкое увеличение эффективности перорального ЭЭ по сравнению с эстрадиолом. пероральный эстрадиол. [7] ЭЭ также не метаболизируется в эстрадиол. [148]
Помимо сульфатной конъюгации, ЭЭ в основном метаболизируется путем гидроксилирования в катехол-эстрогены . [7] В основном это происходит за счет 2-гидроксилирования в 2-гидрокси-EE, которое катализируется преимущественно CYP3A4 . [10] Также сообщалось о гидроксилировании ЭЭ в положениях C4, C6α и C16β в 4-, 6α- и 16β-гидрокси-ЭЭ, но, по-видимому, оно лишь в небольшой степени способствует его метаболизму. [10] 2- и 4-метокси-ЭЭ также образуются в результате трансформации 2- и 4-гидрокси-ЭЭ катехол-О-метилтрансферазой . [7] В отличие от эстрадиола, 16α-гидроксилирование не происходит с EE из-за стерических затруднений со стороны его этинильной группы при C17α. [10] [7] Этинилирование ЭЭ в значительной степени необратимо, поэтому ЭЭ не метаболизируется в эстрадиол, в отличие от эфиров эстрадиола . [7] Обзор показал, что диапазон периода полувыведения ЭЭ, о котором сообщается в литературе, составляет от 13,1 до 27,0 часов. [2] В другом обзоре сообщается, что период полувыведения ЭЭ составляет от 10 до 20 часов. [10] Однако другие источники сообщают, что период полувыведения ЭЭ составляет от 7 часов [11] до 36 часов. [9]
В отличие от эстрадиола, при котором наблюдается быстрый рост его уровня и который остается повышенным на платообразной кривой в течение многих часов, уровни ЭЭ быстро падают после достижения пика. [7] Считается, что это связано с тем, что эстрон и сульфат эстрона могут обратимо превращаться обратно в эстрадиол и служить гормонально инертным резервуаром для эстрадиола, тогда как резервуар сульфата ЭЭ для ЭЭ намного меньше по сравнению с этим. [7] [4] В любом случае, благодаря образованию сульфата ЭЭ, энтерогепатическая рециркуляция участвует в фармакокинетике ЭЭ аналогично эстрадиолу, хотя и в меньшей степени. [7] [149] Вклад энтерогепатической рециркуляции в общий уровень ЭЭ в крови составляет от 12 до 20% или менее и не наблюдается постоянно. [8] [149] Вторичный пик уровня ЭЭ через 10–14 часов после приема часто можно наблюдать при пероральном приеме ЭЭ. [149]
ЭЭ после окислительного образования очень реактивного метаболита необратимо ингибирует ферменты цитохрома Р450 , участвующие в его метаболизме, и это также может играть роль в повышении эффективности ЭЭ по сравнению с эстрадиолом. [7] Действительно, считается, что ЭЭ оказывает заметное влияние на метаболизм в печени, и это, среди прочего, одна из причин того, что природные эстрогены, такие как эстрадиол, могут быть предпочтительными. [146] После 1 года терапии наблюдалось двукратное накопление уровней ЭЭ при приеме КОК, содержащих ЭЭ. [149]
ЭЭ выводится 62% с калом и 38% с мочой . [10]
ЭЭ, также известный как 17α-этинилэстрадиол или как 17α-этинилэстра-1,3,5(10)-триен-3,17β-диол, представляет собой синтетический эстрановый стероид и производное эстрадиола с этинильной заменой в положении C17α . [1] [150] 17α-этинилирование эстрадиола с образованием ЭЭ аналогично 17α-замене тестостерона с образованием производных тестостерона, таких как 17α-этинилированные прогестины, такие как этистерон (17α-этинилтестостерон) и норэтистерон (17α-этинил-19- нортестостерон), а также 17α-алкилированные андрогены / анаболические стероиды , такие как метилтестостерон (17α-метилтестостерон).
Существует ряд производных от EE. [1] [150] К ним относятся местранол (EE 3-метиловый эфир), хинестрол (EE 3-циклопентиловый эфир), этинилэстрадиолсульфонат (EE 3-изопропилсульфонат) и моксэстрол (11β-метокси-EE). [1] [150] [8] Первые три являются пролекарствами ЭЭ, а второй - нет. [8] Существует несколько аналогов EE с другими заменами в положении C17α. [1] [150] Примеры включают производные эстрадиола метилэстрадиол (17α-метилэстрадиол) и этилэстрадиол (17α-этилэстрадиол), а также производные эстриола этинилэстриол (17α-этинилэстрадиол) и нилестриол (3-циклопентиловый эфир 17α-этинилэстриола). [1] [150] Андростановые аналоги ЭЭ со значительной, хотя и слабой эстрогенной активностью включают этиниландростенедиол (17α-этинил-5-андростенедиол), 17α-этинил-3β-андростандиол , 17α-этинил-3α-андростандиол и метандриол (17α-метил -5-андростенедиол).
ЭЭ был первым перорально активным синтетическим эстрогеном и был описан в 1938 году Хансом Херлоффом Инхоффеном и Вальтером Хольвегом из Schering AG в Берлине . [151] [152] [153] [ 154] [155] Одобрено FDA .в США25 июня 1943 года и продавался компанией Schering под торговой маркой Estinyl . [14] FDA отозвало одобрение эстинила с 4 июня 2004 г. по запросу компании Schering , которая прекратила его продажу. [156]
ЭЭ никогда не применялся для внутримышечных инъекций . [157]
ЭЭ был впервые использован в КОК в качестве альтернативы местранолу в 1964 году и вскоре после этого заменил местранол в КОК. [15]
Ранние КОК содержали от 40 до 100 мкг ЭЭ/день и от 50 до 150 мкг/день местранола. [158] [159]
Этинилэстрадиол — английское непатентованное название препарата и его МНН., США, БАНи ЯН. [160] [1] [161] [150] Его также писали как этинилэстрадиол , этинилэстрадиол и этинилэстрадиол (все имеют одинаковое произношение), и последний раньше был его ЗАПРЕЩЕННЫМ.но в конечном итоге был изменен. [160] [1] [150] Кроме того, в названии ЭЭ часто включается пробел, так что он пишется как этинилэстрадиол (а также его варианты), и это его USP.имя. [160] [150] Родовое название EE на французском языке и его DCF.это этинилэстрадиол , по -испански это этинилэстрадиол , по- итальянски и его DCITявляются этинилэстрадиолом , а по латыни — этинилэстрадиолом . [160] [150]
В медицинской литературе название препарата часто сокращают как ЕЕ или ЕЕ2 .
ЭЭ продается как самостоятельный пероральный препарат под торговыми марками Esteed , Estinyl , Feminone , Lynoral , Menolyn , Novestrol , Palonyl , Spanestrin и Ylestrol , среди других, хотя большинство или все эти препараты в настоящее время сняты с производства. [162] [163] [150] Он продается под очень большим количеством торговых марок по всему миру в сочетании с прогестинами для использования в качестве перорального контрацептива. [160] Кроме того, ЭЭ продается в США в сочетании с норэлгестромином под торговыми марками Орто Эвра и Ксулан в качестве противозачаточного пластыря , в сочетании с этоногестрелом под торговой маркой NuvaRing в качестве противозачаточного вагинального кольца и в сочетании с ацетатом норэтистерона . под торговой маркой FemHRT в заместительной гормональной терапии для лечения симптомов менопаузы. [12]
EE широко продается по всему миру. [160] [150] Он продается исключительно или почти исключительно в сочетании с прогестинами. [160]
Сродство связывания EE2 с рецептором эстрогена аналогично сродству эстрадиола. [...] При ежедневном приеме уровни EE2 повышаются до устойчивого состояния, которое достигается примерно через 1 неделю.
Этинилэстрадиол — синтетический и сравнительно мощный эстроген. В результате алкилирования в положении 17-C он не является субстратом для 17β-дегидрогеназы, фермента, который превращает природный эстрадиол-17β в менее мощный эстрон в органах-мишенях.
В 1964 году этинилэстрадиол был представлен в качестве альтернативы местранолу в качестве эстрогенного [...]
ЭТИНИЛ ЭСТРАДИОЛ: ТАБЛЕТКА; ПЕРОРАЛЬНО: ЭСТИНИЛ: ШЕРИНГ: 0,02 мг; 0,05 мг; 0,5 мг
Этинилэстрадиол 0,05мг КПР 0,05мг Этинилэстрадиол (G03CA01) (FR) Этинилэстрадиол таблетки 50 мкг Этинилэстрадиол (G03CA01) (RUS) Этинилэстрадиол 25мкг (Jenapharm) Драже: Этинилэстрадиол 25мкг (G03CA01) (DE) Этинилест радиол пч 0,002мг СЛР 0,002мг этинилэстрадиол (FR) Этинилэстрадиол таблетка 0,05 мг этинилэстрадиол 0,05 мг (G03CA01) (NL) [...] Этинилэстрадиол табл. 0,5 мг (Nycomed pharma a/s) этинилэстрадиол (L02AA03) (NO) Этифоллин табл. 50 мкг (Nycomed pharma) а/с) этинилэстрадиол (G03CA01) (NO)
Этинилоэстрадиол (Линорал, таблетки по 0,05 мг, 0,1 мг, 1 мг)
Низкие дозы КОК содержат <50 мкг эстрогена и являются основным выбором для пероральной контрацепции. КОК, содержащие ≥50 мкг эстрогена, больше не следует регулярно использовать в качестве контрацепции. [...] Эстрогеновый компонент КОК может вызвать чувство переполнения и болезненности груди.
По рекомендации Консультативного комитета по препаратам для лечения бесплодия и материнства Управление по контролю за продуктами и лекарствами (FDA) недавно распорядилось удалить с рынка все пероральные контрацептивы с содержанием этинилэстрадиола более 50 мкг.
Составы пероральных контрацептивов, содержащие более 50 мкг этинилэстрадиола, были удалены с рынка США в 1989 году, а продаваемые в настоящее время составы обычно содержат от 20 до 35 мкг этинилэстрадиола.
Дальнейшие исследования показали, что терапевтический эффект этинилэстрадиола при установленном ЭАЭ опосредован через GPER, но не через ERα, и, возможно, включает продукцию противовоспалительного цитокина Il-10.115.
Кроме того, было показано, что терапевтический эффект этинилэстрадиола при уже установленном заболевании требует экспрессии GPER, но не ERα, и связан с выработкой противовоспалительного цитокина IL-10 (Yates et al., 2010).
Синтетический эстроген этинилэстрадиол, чаще используемый в пероральных контрацептивах, имеет биологическую активность, в 100 раз превышающую биологическую активность нативного и конъюгированного вещества.
EE2 имеет примерно в 100 раз большую эффективность, чем эквивалентная масса конъюгированного лошадиного эстрогена или сульфата эстрона для стимуляции синтеза печеночных белков. [...] EE2 примерно в 1,7 раза сильнее, чем местранол той же массы.
Мейер и др. обнаружили, что этинилэстрадиол в 75–100 раз более эффективен, чем конъюгированный эстроген, исходя из доз, необходимых для снижения уровня тестостерона до уровня взрослых женщин, причем необходимы 0,1 мг первого и от 7,5 до 10 мг второго.
Относительная эффективность некоторых эстрогенов оценивалась путем определения влияния на ФСГ в плазме, измерения системного эффекта, а также по увеличению ГСПГ, КБГ и ангиотензиногена, все из которых указывают на влияние на печень. Сульфат пиперазина эстрона и микронизированный эстрадиол были одинаково эффективны в отношении увеличения ГСПГ, тогда как конъюгированные эстрогены были в 3,2 раза более эффективными, DES был в 28,4 раза более эффективным, а этинилэстрадиол был в 600 раз более эффективным. Что касается снижения ФСГ, конъюгированные эстрогены были в 1,4 раза, ДЭС - в 3,8 раза, а этинилэстрадиол был в 80-200 раз более эффективным, чем сульфат пиперазина эстрона.
Не подлежит сомнению, что конверсия эндометрия при инъекциях как синтетических, так и нативных препаратов эстрогенных гормонов удается, однако мнение о том, могут ли нативные, перорально вводимые препараты вызывать пролиферацию слизистой оболочки, у разных авторов меняется. ПЕДЕРСЕН-БЬЕРГААРД (1939) сумел показать, что 90% фолликулина, поступившего в кровь воротной вены, инактивируется в печени. Ни KAUFMANN (1933, 1935), ни RAUSCHER (1939, 1942), ни HERRNBERGER (1941) не смогли вызвать пролиферацию кастрационного эндометрия с помощью больших доз перорально вводимых препаратов эстрона или эстрадиола. Другие результаты сообщают НЕЙСТАЕДТЕР (1939), ЛАУТЕРВЕЙН (1940) и ФЕРИН (1941); им удалось превратить атрофический кастрационный эндометрий в однозначную пролиферацию слизистой оболочки с помощью 120–300 эстрадиола или 380 эстрона.
Этинилэстрадиол [эстинил, феминон, линорал, новестрол, палонил]
ЭТИНИЛЭСТРАДИОЛ USP (Эстид®, Эстинил®, Линорал®, Менолин®, Новестрол®, Палонил®, Спэнестрин®, Илестрол®)