Болезнь Лайма , также известная как Лайм-боррелиоз , представляет собой трансмиссивное заболевание, вызываемое бактериями Borrelia , которые распространяются клещами рода Ixodes . [3] [8] [9] Наиболее частым признаком инфекции является расширяющаяся красная сыпь , известная как мигрирующая эритема (МЭ), которая появляется на месте укуса клеща примерно через неделю. [1] Сыпь обычно не вызывает ни зуда, ни боли. [1] Примерно у 70–80% инфицированных людей появляется сыпь. [1] Ранняя диагностика может быть затруднена. [10] Другие ранние симптомы могут включать лихорадку, головные боли и усталость . [1] При отсутствии лечения симптомы могут включать потерю способности двигать одной или обеими сторонами лица , боли в суставах , сильные головные боли с скованностью шеи или учащенным сердцебиением . [1] Через несколько месяцев или лет могут возникнуть повторные эпизоды боли в суставах и отека. [1] Иногда могут возникать стреляющие боли или покалывание в руках и ногах. [1] Несмотря на соответствующее лечение, примерно у 10–20% пострадавших развиваются боли в суставах, проблемы с памятью и усталость в течение как минимум шести месяцев. [1] [11]
Болезнь Лайма передается человеку при укусах зараженных клещей рода Ixodes . [12] В Соединенных Штатах опасные клещи обычно относятся к типу Ixodes scapularis . «В большинстве случаев клещ должен быть прикреплен на 36–48 часов или более, прежде чем бактерия болезни Лайма сможет передаться. Если вы удалите клеща быстро (в течение 24 часов), вы можете значительно снизить свои шансы заболеть болезнью Лайма». [13] [14] В Европе клещи Ixodes ricinus могут распространять бактерии быстрее. [14] [15] В Северной Америке бактериальные виды Borrelia burgdorferi и B. mayonii вызывают болезнь Лайма. [3] [16] В Европе и Азии заболевание также вызывают Borrelia afzelii , Borrelia garinii , B. spielmanii и четыре других вида. [3] По всей видимости, болезнь не передается между людьми, другими животными и через пищу. [13] Диагноз ставится на основании сочетания симптомов, истории контакта с клещами и, возможно, тестирования на наличие специфических антител в крови. [4] [17] На ранних стадиях заболевания анализы крови часто оказываются ложноотрицательными. [3] Тестирование отдельных клещей обычно бесполезно. [18]
Профилактика включает усилия по предотвращению укусов клещей путем ношения одежды, закрывающей руки и ноги, и использования репеллентов на основе ДЭТА или пикаридина . [3] [8] Использование пестицидов для уменьшения численности клещей также может быть эффективным. [3] Клещей можно удалить с помощью пинцета . [19] Если удаленный клещ полон крови, для предотвращения развития инфекции можно использовать однократную дозу доксициклина , но обычно это не рекомендуется, поскольку развитие инфекции встречается редко. [3] Если развивается инфекция, эффективен ряд антибиотиков, включая доксициклин, амоксициллин и цефуроксим . [3] Стандартное лечение обычно длится две или три недели. [3] У некоторых людей в результате лечения повышается температура, появляются боли в мышцах и суставах, которые могут длиться один или два дня. [3] У тех, у кого развиваются стойкие симптомы, длительная антибиотикотерапия не оказалась полезной. [3] [20]
Болезнь Лайма — наиболее распространенное заболевание, распространяемое клещами в Северном полушарии. [21] [7] Инфекции наиболее распространены весной и в начале лета. [3] Болезнь Лайма была впервые диагностирована как отдельное заболевание в 1975 году в Лайме, штат Коннектикут . Первоначально его ошибочно приняли за ювенильный ревматоидный артрит . [22] Используемая бактерия была впервые описана в 1981 году Вилли Бургдорфером . [23] Хронические симптомы после лечения известны как «синдром болезни Лайма после лечения» (PTLDS). [20] PTLDS отличается от хронической болезни Лайма , термина, который больше не поддерживается учеными и по-разному используется разными группами. [20] [24] Некоторые медицинские работники заявляют, что PTLDS вызван стойкой инфекцией, но это не соответствует действительности, поскольку после стандартного лечения не может быть обнаружено никаких доказательств стойкой инфекции. [25]
По состоянию на 2023 год [обновлять]проводились клинические испытания предлагаемых вакцин против болезни Лайма на людях, но вакцины не было. Вакцина LYMERix была произведена, но прекращена в 2002 году из-за недостаточного спроса. [26] Существует несколько вакцин для профилактики болезни Лайма у собак.
Болезнь Лайма может поражать несколько систем организма и вызывать широкий спектр симптомов. Не у всех больных болезнью Лайма наблюдаются все симптомы, и многие из них не являются специфичными для болезни Лайма, но могут возникать и при других заболеваниях. [31]
Инкубационный период от заражения до появления симптомов обычно составляет одну-две недели, но может быть намного короче (дни) или намного дольше (от месяцев до лет). [32] Симптомы Лайма чаще всего возникают с мая по сентябрь в Северном полушарии, поскольку в большинстве случаев ответственна нимфальная стадия клеща. [32] Существует бессимптомная инфекция, но она встречается менее чем у 7% инфицированных людей в Соединенных Штатах. [33] Бессимптомная инфекция может быть гораздо более распространена среди инфицированных в Европе. [34]
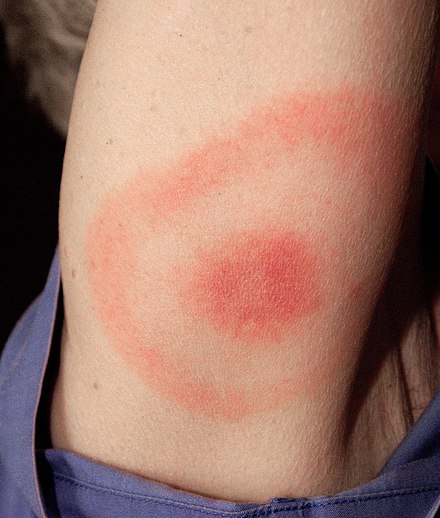
Ранняя локализованная инфекция может возникнуть, когда инфекция еще не распространилась по организму. Поражается только тот участок, где инфекция впервые вступила в контакт с кожей. Первоначальным признаком около 80% инфекций Лайма является мигрирующая эритема (МЭ) сыпь в месте укуса клеща, часто возле складок кожи, таких как подмышки , пах или задняя часть колена , на туловище , под лямками одежды. , или в волосах, ушах или шее детей. [27] [3] Большинство заразившихся людей не помнят, что видели клеща или укуса. Сыпь обычно появляется через одну или две недели (3–32 дня) после укуса и увеличивается на 2–3 см в день до диаметра 5–70 см (в среднем 16 см). [27] [3] [28] Сыпь обычно круглая или овальная, красная или синеватая, с приподнятым или более темным центром. [3] [29] [30] Примерно в 79% случаев в Европе и только в 19% случаев в эндемичных районах США сыпь постепенно исчезает от центра к краям, возможно, образуя узор «бычий глаз». [28] [29] [30] Сыпь может казаться теплой, но обычно не вызывает зуда, редко бывает болезненной или болезненной, и, если ее не лечить, на ее разрешение уходит до четырех недель. [3]
Сыпь ЭМ часто сопровождается симптомами вирусоподобного заболевания, включая усталость, головную боль, боли в теле, лихорадку и озноб, но обычно не сопровождается тошнотой или проблемами верхних дыхательных путей. Эти симптомы могут также появляться без сыпи или сохраняться после исчезновения сыпи. Лайм может прогрессировать до более поздних стадий без этих симптомов или сыпи. [3]
Людей с высокой температурой в течение более двух дней или у которых другие симптомы вирусоподобного заболевания не улучшаются, несмотря на лечение антибиотиками при болезни Лайма, или у которых аномально низкие уровни лейкоцитов, эритроцитов или тромбоцитов в крови , следует обследовать на предмет возможного коинфекция с другими клещевыми заболеваниями, такими как эрлихиоз и бабезиоз . [35]
В течение нескольких дней или недель после начала местной инфекции бактерии Borrelia могут распространиться через лимфатическую систему или кровоток. В 10–20% нелеченных случаев ЭМ-сыпи развиваются на участках тела, не имеющих никакого отношения к первоначальному укусу клеща. [27] Также распространены преходящие мышечные боли и боли в суставах . [27]
Примерно у 10–15% людей, не получавших лечения, болезнь Лайма вызывает неврологические проблемы, известные как нейроборрелиоз . [36] Ранний нейроборрелиоз обычно появляется через 4–6 недель (диапазон 1–12 недель) после укуса клеща и включает в себя некоторую комбинацию лимфоцитарного менингита, краниального неврита, радикулопатии и/или множественного мононеврита. [35] [37] Лимфоцитарный менингит вызывает характерные изменения в спинномозговой жидкости (СМЖ) и может сопровождаться в течение нескольких недель различной головной болью и, реже, обычно легкими признаками менингита , такими как неспособность полностью сгибать шею и непереносимость яркого света. но обычно нет или только очень низкая температура. [38] Через несколько месяцев нейроборрелиоз может также проявлять отоларингологические симптомы . До 76,5% из них проявляются шумом в ушах , наиболее распространенным симптомом. Следующими наиболее распространенными симптомами были головокружение и головокружение (53,7%), а также потеря слуха (16,7%). [39] У детей также может возникнуть частичная потеря зрения . [35] Черепно-мозговой неврит – воспаление черепных нервов . При болезни Лайма чаще всего возникает паралич лицевого нерва , затрудняющий моргание, улыбку и жевание на одной или обеих сторонах лица. Это также может вызвать периодическое двоение в глазах . [35] [38] Радикулопатия Лайма – это воспаление корешков спинномозговых нервов , которое часто вызывает боль и реже слабость , онемение или изменение чувствительности в областях тела, обслуживаемых нервами, связанными с пораженными корешками , например конечностями или часть(и) туловища. Боль часто описывается как не похожая ни на одну другую, ощущавшуюся ранее, мучительная, мигрирующая, усиливается ночью, редко симметричная и часто сопровождается сильным нарушением сна. [37] [40] Множественный мононеврит — это воспаление, вызывающее сходные симптомы в одном или нескольких несвязанных периферических нервах. [36] [35] Редко ранний нейроборрелиоз может включать воспаление головного или спинного мозга с такими симптомами, как спутанность сознания, ненормальная походка, движения глаз или речи , нарушение движений , нарушение планирования движений или дрожь . [35] [37]
В Северной Америке паралич лицевого нерва является типичным ранним проявлением нейроборрелиоза, встречающимся у 5–10% нелеченых людей и примерно в 75% случаев, сопровождающимся лимфоцитарным менингитом. [35] [41] Сообщается о радикулопатии Лайма вдвое реже, но многие случаи могут быть нераспознанными. [42] У взрослых европейцев наиболее частым проявлением является комбинация лимфоцитарного менингита и радикулопатии, известная как синдром Баннварта , сопровождающаяся в 36-89% случаев параличом лицевого нерва. [37] [40] При этом синдроме корешковая боль, как правило, начинается в той же области тела, что и начальная мигрирующая эритема , если таковая имеется, и предшествует возможному параличу лицевого нерва и другим нарушениям движений . [40] В крайних случаях может возникнуть необратимое нарушение двигательной или сенсорной функции нижних конечностей. [34] У европейских детей наиболее частыми проявлениями являются паралич лицевого нерва (в 55%), другие краниальные невриты и лимфоцитарный менингит (в 27%). [37]
Примерно в 4–10% нелеченых случаев в США и в 0,3–4% нелеченых случаев в Европе, обычно в период с июня по декабрь, примерно через месяц (диапазон 4–7 месяцев) после укуса клеща инфекция может вызвать сердечную недостаточность. осложнения, известные как кардит Лайма . [43] [44] Симптомы могут включать учащенное сердцебиение ( у 69% людей), головокружение , обморок , одышку и боль в груди . [43] Могут также присутствовать другие симптомы болезни Лайма, такие как ЭМ- сыпь, боли в суставах , паралич лицевого нерва , головные боли или корешковые боли . [43] Однако у некоторых людей кардит может быть первым проявлением болезни Лайма. [43] Лайм-кардит у 19–87% людей отрицательно влияет на систему электропроводности сердца, вызывая атриовентрикулярную блокаду , которая часто проявляется в виде сердечных ритмов, которые в течение нескольких минут чередуются между аномально медленными и аномально быстрыми. [43] [44] У 10–15% людей болезнь Лайма вызывает осложнения миокарда , такие как кардиомегалия , дисфункция левого желудочка или застойная сердечная недостаточность. [43]
Другое кожное заболевание, встречающееся в Европе, но не в Северной Америке, — это боррелиальная лимфоцитома , пурпурная шишка, которая развивается на мочке уха, соске или мошонке . [45]

Лайм-артрит возникает у 60% людей, не получавших лечения, обычно начинается примерно через шесть месяцев после заражения. [27] Обычно поражается только один или несколько суставов, часто коленный или, возможно , тазобедренный , другие крупные суставы или височно-нижнечелюстной сустав . [35] [47] Обычно возникает большой суставной выпот и отек, но только легкая или умеренная боль. [35] Без лечения отек и боль обычно проходят со временем, но периодически возвращаются. [35] Кисты Бейкера могут образовываться и разрываться.
В ранних исследованиях болезни Лайма в США была описана редкая периферическая невропатия , которая включала онемение, покалывание или жжение, начинающееся в ступнях или руках и со временем, возможно, распространяющееся вверх по конечностям. В более позднем анализе, который обнаружил плохую документацию этого проявления, эксперты задались вопросом, существует ли оно вообще в США или оно просто очень редкое. [35] [48]
Неврологический синдром, называемый энцефалопатией Лайма, связан с тонкими нарушениями памяти и когнитивных функций, бессонницей , общим недомоганием и изменениями личности. [49] Лаймская энцефалопатия вызывает споры в США и не регистрировалась в Европе. [7] Такие проблемы, как депрессия и фибромиалгия, встречаются у людей с болезнью Лайма так же часто, как и у населения в целом. [50] [51] Не существует убедительных доказательств того, что болезнь Лайма вызывает психические расстройства, поведенческие расстройства (например, СДВГ ) или нарушения развития (например, аутизм ). [52]
Хронический атрофический акродерматит — хроническое заболевание кожи, наблюдаемое преимущественно в Европе среди пожилых людей. [45] Оно начинается с красновато-синего пятна обесцвеченной кожи, часто на тыльной стороне рук или ног. Поражение медленно атрофируется в течение нескольких недель или месяцев, при этом кожа сначала становится тонкой и морщинистой, а затем, при отсутствии лечения, полностью сухой и лишенной волос. [53] Это также связано с периферической нейропатией. [48]

Болезнь Лайма вызывают спирохеты , спиральные бактерии рода Borrelia . Спирохеты окружены пептидогликанами и жгутиками , а также имеют внешнюю мембрану, аналогичную грамотрицательным бактериям. Из-за двойной мембранной оболочки бактерии Borrelia часто ошибочно называют грамотрицательными , несмотря на значительные различия в компонентах их оболочки от грамотрицательных бактерий. [54] Родственные Лайму виды Borrelia известны под общим названием Borrelia burgdorferi sensu lato и демонстрируют большое генетическое разнообразие . [55]
B. burgdorferi sensu lato представляет собой комплекс видов, состоящий из 20 признанных и трех предполагаемых геновидов. Известно, что восемь видов вызывают болезнь Лайма: B. mayonii (обнаружен в Северной Америке), B. burgdorferi sensu stricto (обнаружен в Северной Америке и Европе), B. afzelii , B. garinii, B. spielmanii и B. lusitaniae ( обнаружен в Северной Америке и Европе). все найдены в Евразии ). [56] [57] [16] [9] Некоторые исследования также показали, что B. valaisiana может иногда заражать людей, но этот вид, по-видимому, не является важной причиной заболеваний. [58] [59]


В жизненном цикле клеща происходят три стадии – личинка, нимфа и взрослая особь. На стадии нимфы клещи чаще всего переносят болезнь Лайма и обычно наиболее активны в конце весны и начале лета в регионах с мягким климатом. На взрослой стадии передача болезни Лайма встречается реже, поскольку взрослые клещи с меньшей вероятностью кусают людей и, как правило, больше по размеру, поэтому их легко увидеть и удалить. [60]
Болезнь Лайма классифицируется как зооноз , так как она передается человеку из естественного резервуара среди мелких млекопитающих и птиц клещами , питающимися обеими группами хозяев . [61] Твердые клещи рода Ixodes являются переносчиками болезни Лайма (также переносчиком бабезий ). [62] Большинство инфекций вызываются клещами, находящимися в нимфальной стадии , поскольку они очень маленькие и могут питаться в течение длительного периода времени незамеченными. [61] Нимфальные клещи обычно имеют размер макового зернышка, иногда с темной головой и полупрозрачным телом. [63] Или нимфальные клещи могут быть темнее. [64] Молодые личинки клещей заражаются очень редко. [65] Хотя олени являются предпочтительными хозяевами взрослых оленьих клещей, а в отсутствие оленей популяция клещей намного ниже, клещи обычно не приобретают боррелии от оленей, а вместо этого они получают их от инфицированных мелких млекопитающих, таких как белоногие мыши. , а иногда и птицы. [66] Районы, где распространен Лайм, расширяются. [67]
В средней кишке клеща белок А внешней поверхности боррелий (OspA) связывается с клещевым рецептором OspA, известным как TROSPA. Когда клещ питается, боррелии подавляют активность OspA и повышают активность OspC, другого поверхностного белка. После того, как бактерии мигрируют из средней кишки в слюнные железы, OspC связывается с Salp15, белком слюны клещей, который, по-видимому, оказывает иммуносупрессивное действие, усиливая инфекцию. [68] Успешное инфицирование хозяина-млекопитающего зависит от бактериальной экспрессии OspC. [69]
Укусы клещей часто остаются незамеченными из-за небольшого размера клеща в нимфальной стадии, а также выделений клеща, которые не позволяют хозяину чувствовать зуд или боль от укуса. Однако передача происходит довольно редко: лишь около 1,2–1,4 процента обнаруженных укусов клещей приводят к болезни Лайма. [70]

В Европе основным переносчиком является Ixodes ricinus , которого еще называют овечьим клещом или клещевиной . [71] В Китае Ixodes persulcatus (таежный клещ), вероятно, является наиболее важным переносчиком. [72] В Северной Америке черноногий клещ или олений клещ ( Ixodes scapularis ) является основным переносчиком на восточном побережье. [65]
Одинокий звездчатый клещ ( Amblyomma americanum ), который встречается на юго-востоке Соединенных Штатов вплоть до Техаса , вряд ли является переносчиком спирохет болезни Лайма [73] , хотя он может быть вовлечен в родственный синдром, называемый сыпью , связанной с южным клещом. болезнь , напоминающая легкую форму болезни Лайма. [74]
На западном побережье США основным переносчиком является западный черноногий клещ ( Ixodes pacificus ). [75] Тенденция этого вида клещей питаться преимущественно видами-хозяевами, такими как ящерица западного забора , которые устойчивы к инфекции Borrelia , по-видимому, снижает передачу болезни Лайма на Западе. [76] [77]
Передача инфекции может происходить через плаценту во время беременности, и, как и в случае ряда других спирохетальных заболеваний, при отсутствии лечения инфекции возможны неблагоприятные исходы беременности; своевременное лечение антибиотиками снижает или устраняет этот риск. [78] [79] [80] [81] [82]
Нет никаких научных доказательств, подтверждающих передачу болезни Лайма через переливание крови, половой контакт или грудное молоко. [83]
Клещи, передающие B. burgdorferi человеку, также могут переносить и некоторые другие микробы, такие как Babesia microti и Anaplasma phagocytophilum , которые вызывают заболевания бабезиоз и гранулоцитарный анаплазмоз человека (HGA) соответственно. [84] Среди людей с ранней болезнью Лайма, в зависимости от их местоположения, у 2–12% также будет HGA, а у 2–10% — бабезиоз. [52] В некоторых регионах клещи также переносят вирусы, вызывающие клещевой энцефалит и вирусную болезнь Повассан . [85] [52] Коинфекции болезни Лайма могут не требовать дополнительного лечения, поскольку они могут пройти самостоятельно или, как в случае с HGA, их можно лечить доксициклином, назначенным при болезни Лайма. [35] Стойкая лихорадка или соответствующие аномальные лабораторные данные могут указывать на коинфекцию. [52]
B. burgdorferi может распространяться по всему организму в ходе болезни и обнаруживается в коже, сердце, суставах, периферической и центральной нервной системе. [69] [86] Б. Бургдорфери не производит токсинов. [87] Таким образом, многие признаки и симптомы болезни Лайма являются следствием иммунного ответа на спирохеты в этих тканях. [88]
B. burgdorferi попадает в кожу при укусе зараженного иксодового клеща. Слюна клеща, сопровождающая спирохету в кожу в процессе питания, содержит вещества, нарушающие иммунный ответ в месте укуса. [89] Это обеспечивает защитную среду, в которой спирохеты могут занести инфекцию. Спирохеты размножаются и мигрируют наружу в пределах дермы . Воспалительная реакция хозяина на бактерии в коже вызывает характерное круговое ЭМ-поражение. [69] Однако нейтрофилы , необходимые для устранения спирохет из кожи, не появляются в необходимом количестве при развивающемся ЭМ-поражении, поскольку слюна клеща ингибирует функцию нейтрофилов. Это позволяет бактериям выживать и в конечном итоге распространяться по всему организму. [90]
Через несколько дней или недель после укуса клеща спирохеты распространяются через кровоток в суставы, сердце, нервную систему и отдаленные участки кожи, где их присутствие приводит к появлению разнообразных симптомов диссеминированного заболевания. Распространению B. burgdorferi способствует прикрепление плазмина протеазы хозяина к поверхности спирохеты. [91]
При отсутствии лечения бактерии могут сохраняться в организме в течение месяцев или даже лет, несмотря на выработку иммунной системой антител к B. burgdorferi . [92] Спирохеты могут избежать иммунного ответа за счет снижения экспрессии поверхностных белков, на которые нацелены антитела, антигенных вариаций поверхностного белка VlsE, инактивации ключевых иммунных компонентов, таких как комплемент , и сокрытия во внеклеточном матриксе , что может мешать действие иммунных факторов. [93] [94]
В головном мозге B. burgdorferi может вызывать астроглиоз ( пролиферацию с последующим апоптозом ) астроцитов , что может способствовать нейродисфункции. [95] Спирохеты могут также побуждать клетки-хозяева выделять хинолиновую кислоту , которая стимулирует рецептор NMDA на нервных клетках, что может быть причиной усталости и недомогания, наблюдаемых при энцефалопатии Лайма . [96] Кроме того, диффузная патология белого вещества при энцефалопатии Лайма может нарушать связи серого вещества и может быть причиной дефицита внимания, памяти, зрительно-пространственных способностей, сложных когнитивных функций и эмоционального статуса. Заболевания белого вещества могут иметь больший потенциал для выздоровления, чем заболевания серого вещества, возможно, потому, что потеря нейронов встречается реже. Наблюдалось разрешение гиперинтенсивности белого вещества на МРТ после лечения антибиотиками. [97]
Уровень триптофана , предшественника серотонина , снижается в центральной нервной системе при ряде инфекционных заболеваний, поражающих мозг, включая болезнь Лайма. [98] Исследователи выясняют, является ли секреция нейрогормонов причиной нервно-психических расстройств, развивающихся у некоторых людей с боррелиозом. [99]
Воздействие бактерии Borrelia во время болезни Лайма, возможно, вызывает длительную и повреждающую воспалительную реакцию , [100] форму аутоиммунного заболевания, вызванного патогеном. [101] Возникновение этой реакции может быть связано с формой молекулярной мимикрии , при которой боррелии избегают уничтожения иммунной системой, напоминая нормальные части тканей организма. [102] [103]
Хронические симптомы аутоиммунной реакции могут объяснить, почему некоторые симптомы сохраняются даже после того, как спирохеты были выведены из организма. Эта гипотеза может объяснить, почему хронический артрит сохраняется после терапии антибиотиками, подобно ревматической лихорадке , но ее более широкое применение является спорным. [104] [105]
Болезнь Лайма диагностируется на основании симптомов, объективных физических данных (таких как сыпь при мигрирующей эритеме (МЭ), паралич лицевого нерва или артрит ), истории возможного контакта с инфицированными клещами и, возможно, лабораторных анализов. [3] [27] Людям с симптомами ранней стадии болезни Лайма следует провести общее обследование кожи тела на наличие ЭМ-сыпей и спросить, проявлялись ли ЭМ-типы сыпи в течение последних 1–2 месяцев. [35] Наличие ЭМ-сыпи и недавнее воздействие клещей (т. е. нахождение на открытом воздухе в вероятном месте обитания клещей, где распространен Лайм , в течение 30 дней после появления сыпи) достаточны для диагностики Лайма; лабораторное подтверждение не требуется и не рекомендуется. [3] [27] [106] [107] Большинство людей, заразившихся, не помнят ни клеща, ни укуса, и ЭМ-сыпь не обязательно должна выглядеть как яблочко (большинство ЭМ-сыпей в США так не выглядит) или сопровождаться по любым другим симптомам. [3] [108] В США болезнь Лайма наиболее распространена в штатах Новой Англии и Среднеатлантических штатах, а также в некоторых частях Висконсина и Миннесоты , но она распространяется и на другие регионы. [67] Несколько приграничных районов Канады также подвержены высокому риску болезни Лайма. [109]
При отсутствии ЭМ-сыпи или заражения клещами в анамнезе диагноз Лайма зависит от лабораторного подтверждения. [62] [110] Бактерии, вызывающие болезнь Лайма, трудно наблюдать непосредственно в тканях организма, а также их сложно и слишком долго выращивать в лаборатории. [3] [62] Вместо этого наиболее широко используемые тесты направлены на наличие антител против этих бактерий в крови. [111] Положительный результат теста на антитела сам по себе не доказывает активную инфекцию, но может подтвердить инфекцию, которая подозревается на основании симптомов, объективных данных и истории заражения человека клещами. [62] Поскольку до 5–20% здорового населения имеют антитела против Лайма, людям без анамнеза и симптомов, указывающих на болезнь Лайма, не следует проходить тестирование на антитела Лайма: положительный результат, скорее всего, будет ложным, что может привести к ненужному лечению. [35] [37]
В некоторых случаях, когда анамнез, признаки и симптомы убедительно указывают на раннюю диссеминированную болезнь Лайма, можно начать эмпирическое лечение и пересмотреть его по мере получения результатов лабораторных исследований. [41] [112]
Тесты на антитела в крови с помощью ИФА и вестерн-блоттинга являются наиболее широко используемым методом диагностики Лайма. Центры по контролю и профилактике заболеваний (CDC) рекомендуют двухуровневый протокол : сначала проводится чувствительный тест ELISA, а если он положительный или сомнительный, то проводится более специфичный вестерн-блоттинг. [113] Иммунной системе требуется некоторое время, чтобы выработать большое количество антител. После начала инфекции Лайма антитела типов IgM и IgG обычно впервые обнаруживаются соответственно через 2–4 недели и 4–6 недель, а пик – через 6–8 недель. [114] При первом появлении ЭМ-сыпи обнаруживаемые антитела могут отсутствовать. Поэтому рекомендуется не проводить тестирование и ставить диагноз на основании наличия ЭМ-сыпи. [35] В течение 30 дней после предполагаемого начала инфекции Лайма инфекция может быть подтверждена обнаружением антител IgM или IgG; после этого рекомендуется рассматривать только антитела IgG. [114] Положительный результат теста IgM и отрицательный IgG после первого месяца заражения обычно указывает на ложноположительный результат. [115] Количество антител IgM обычно снижается через 4–6 месяцев после заражения, тогда как антитела IgG могут оставаться обнаруживаемыми в течение многих лет. [114]
В случаях нейроборрелиоза могут использоваться и другие тесты. В Европе нейроборрелиоз обычно вызывается Borrelia garinii и почти всегда сопровождается лимфоцитарным плеоцитозом , т.е. плотность лимфоцитов (клеток, борющихся с инфекцией) и белка в спинномозговой жидкости (СМЖ) обычно повышается до характерно аномального уровня, в то время как уровень глюкозы остается нормальным. [38] [35] [40] Кроме того, иммунная система вырабатывает антитела против Лайма внутри интратекального пространства, которое содержит спинномозговую жидкость. [35] [40] Для точного диагноза нейроборрелиоза в Европе требуется подтверждение плеоцитоза и интратекальной продукции антител с помощью люмбальной пункции и анализа спинномозговой жидкости (за исключением случаев периферической нейропатии, связанной с хроническим атрофическим акродерматитом , которая обычно вызывается Borrelia afzelii и подтверждается). по результатам анализа крови на антитела). [37] В Северной Америке нейроборрелиоз вызывается Borrelia burgdorferi и может не сопровождаться такими же признаками СМЖ; они подтверждают диагноз нейроборрелиоза центральной нервной системы (ЦНС) в случае положительного результата, но не исключают его в случае отрицательного результата. [116] Американские рекомендации считают анализ спинномозговой жидкости необязательным, когда симптомы ограничены периферической нервной системой (ПНС), например, паралич лицевого нерва без явных симптомов менингита. [35] [117] В отличие от анализов крови и интратекальных антител, тесты на плеоцитоз спинномозговой жидкости возвращаются к норме после прекращения инфекции и, следовательно, могут использоваться в качестве объективных маркеров успеха лечения и принимать решения о необходимости отступления. [40] При инфекциях ПНС для объективного мониторинга реакции на лечение можно использовать электромиографию и исследования нервной проводимости . [38]
При кардите Лайма электрокардиограммы используются для выявления нарушений сердечной проводимости, тогда как эхокардиография может выявить дисфункцию миокарда . [43] Биопсия и подтверждение наличия клеток Borrelia в ткани миокарда могут использоваться в определенных случаях, но обычно не выполняются из-за риска процедуры. [43]
Тесты полимеразной цепной реакции (ПЦР) на болезнь Лайма также были разработаны для обнаружения генетического материала ( ДНК ) спирохеты, вызывающей болезнь Лайма. Культура или ПЦР являются современными средствами обнаружения присутствия микроорганизма, поскольку серологические исследования проверяют только на наличие антител Borrelia . Преимущество ПЦР в том, что она намного быстрее, чем культура. Однако ПЦР-тесты подвержены ложноположительным результатам, например, из-за обнаружения остатков мертвых клеток боррелий или загрязнения образца. [118] [37] Даже при правильном выполнении ПЦР часто дает ложноотрицательные результаты, поскольку во время инфекции в крови и спинномозговой жидкости (СМЖ) можно обнаружить мало клеток Borrelia. [119] [37] Следовательно, ПЦР-тесты рекомендуются только в особых случаях, например, при диагностике артрита Лайма, поскольку это высокочувствительный способ обнаружения ДНК ospA в синовиальной жидкости. [120] Хотя чувствительность ПЦР в спинномозговой жидкости низкая, ее использование может рассматриваться при подозрении на ложноотрицательные результаты интратекального теста на выработку антител, например, при очень раннем (< 6 недель) нейроборрелиозе или у людей с иммуносупрессией . [37]
Доступны несколько других форм лабораторного тестирования болезни Лайма, некоторые из которых не прошли адекватной валидации. Антигены OspA , выделяемые живыми бактериями Borrelia в мочу, являются перспективным изучаемым методом. [121] В настоящее время рассматривается возможность использования наночастиц-ловушек для их обнаружения, и OspA связан с активными симптомами болезни Лайма. [122] [123] Высокие титры антител иммуноглобулина G (IgG) или иммуноглобулина M (IgM) к антигенам боррелий указывают на заболевание, но более низкие титры могут вводить в заблуждение, поскольку антитела IgM могут оставаться после первоначальной инфекции, а антитела IgG могут оставаться годами. [124]
Центры по контролю и профилактике заболеваний (CDC) не рекомендуют тесты на антигены в моче, ПЦР-тесты мочи, иммунофлуоресцентное окрашивание на формы B. burgdorferi с дефицитом клеточной стенки и тесты на трансформацию лимфоцитов. [119]
Нейровизуализация является спорной в отношении того, выявляет ли она специфические закономерности, уникальные для нейроборрелиоза , но может помочь в дифференциальной диагностике и понимании патофизиологии заболевания. [125] Несмотря на противоречивые данные, некоторые данные показывают, что определенные нейровизуализационные тесты могут предоставить данные, которые полезны в диагностике человека. Магнитно-резонансная томография (МРТ) и однофотонная эмиссионная компьютерная томография (ОФЭКТ) — два теста, которые могут выявить аномалии в мозге человека, страдающего этим заболеванием. Результаты нейровизуализации при МРТ включают поражения перивентрикулярного белого вещества, а также увеличение желудочков и атрофию коры. Результаты считаются в некоторой степени обычными, поскольку было обнаружено, что поражения обратимы после лечения антибиотиками. Изображения, полученные с помощью ОФЭКТ, показывают многочисленные области, где к коре и подкорковому белому веществу поступает недостаточное количество крови. Однако известно, что ОФЭКТ-изображения неспецифичны, поскольку они демонстрируют гетерогенную картину изображения. Аномалии, наблюдаемые на изображениях ОФЭКТ, очень похожи на те, которые наблюдаются у людей с церебральным васкулитом и болезнью Крейтцфельдта-Якоба , что делает их сомнительными. [126]
Сообщается, что в общественных клиниках неправильно диагностируется 23–28% высыпаний при мигрирующей эритеме (МЭ) и 83% других объективных проявлений ранней болезни Лайма. [110] ЭМ-сыпь часто ошибочно принимают за укусы пауков , целлюлит или опоясывающий лишай . [110] Многие ошибочные диагнозы объясняются широко распространенным заблуждением, что ЭМ сыпь должна выглядеть как яблочко. [3] Собственно, ключевыми отличительными особенностями ЭМ сыпи являются скорость и степень ее распространения соответственно до 2–3 см/день и диаметр не менее 5 см, а в 50% случаев более 16 см. см. Сыпь распространяется от центра, который может выглядеть, а может и не отличаться, или отделяться кольцевидными просветлениями от остальной части сыпи. [27] [28] По сравнению с ЭМ-сыпью, укусы пауков чаще встречаются в конечностях, имеют тенденцию быть более болезненными и зудящими или опухшими, а некоторые из них могут вызывать некроз (тонущий темно-синий участок омертвевшей кожи). [27] [3] Целлюлит чаще всего развивается вокруг раны или язвы, редко имеет круглую форму и чаще всего становится опухшим и болезненным. [27] [3] ЭМ-сыпи часто появляются в местах, необычных для целлюлита, таких как подмышки, пах, живот или задняя часть колена. [27] Как и болезнь Лайма, опоясывающий лишай часто начинается с головной боли, лихорадки и усталости, за которыми следуют боль или онемение. Однако, в отличие от Лайма, при опоясывающем лишае эти симптомы обычно сопровождаются появлением сыпи, состоящей из множества маленьких волдырей вместе с дерматомом нерва , и опоясывающий лишай также можно подтвердить с помощью быстрых лабораторных тестов. [127]
Паралич лицевого нерва , вызванный болезнью Лайма (LDFP), часто ошибочно принимают за паралич Белла . [41] Хотя паралич Белла является наиболее распространенным типом одностороннего паралича лицевого нерва (около 70% случаев), LDFP может составлять около 25% случаев паралича лицевого нерва в районах, где распространена болезнь Лайма. [41] По сравнению с LDFP, паралич Белла гораздо реже поражает обе стороны лица. [41] Несмотря на то, что LDFP и паралич Белла имеют схожие симптомы и развиваются одинаково, если их не лечить, лечение кортикостероидами полезно при параличе Белла, но вредно для LDFP. [41] Недавняя история контакта с вероятным местом обитания клещей в теплые месяцы, ЭМ-сыпь, вирусоподобные симптомы, такие как головная боль и лихорадка, и/или паралич обеих сторон лица, должны быть оценены на предмет вероятности LDFP; если он превышает минимальный, следует начать эмпирическую терапию антибиотиками без кортикостероидов и провести повторную оценку после завершения лабораторных исследований на болезнь Лайма. [41]
В отличие от вирусного менингита , лимфоцитарный менингит Лайма, как правило, не вызывает лихорадки, длится дольше и рецидивирует. [38] [35] Лимфоцитарный менингит также характеризуется возможным сочетанием ЭМ-сыпи , параличом лицевого нерва или частичной обструкцией зрения и наличием гораздо более низкого процента полиморфно-ядерных лейкоцитов в спинномозговой жидкости . [35]
Радикулопатию Лайма, поражающую конечности, часто ошибочно диагностируют как радикулопатию, вызванную сдавлением нервных корешков, например ишиас . [110] [128] Хотя большинство случаев радикулопатии являются компрессионными и разрешаются консервативным лечением (например, отдыхом) в течение 4–6 недель, рекомендации по лечению радикулопатии рекомендуют сначала оценить риски других возможных причин, которые, хотя и менее часты, требуют немедленной диагностики. и лечение, включая такие инфекции, как болезнь Лайма и опоясывающий лишай. [129] Активный отдых на свежем воздухе в вероятных местах обитания клещей в течение последних 3 месяцев, возможно, сопровождавшийся сыпью или вирусоподобными симптомами, а также текущей головной болью, другими симптомами лимфоцитарного менингита или параличом лицевого нерва, может привести к подозрению на болезнь Лайма и рекомендации. серологических и люмбальной пункции для подтверждения. [129]
Радикулопатию Лайма, поражающую туловище, можно ошибочно диагностировать как множество других заболеваний, таких как дивертикулит и острый коронарный синдром . [42] [110] Диагностика поздней стадии болезни Лайма часто осложняется многогранным внешним видом и неспецифическими симптомами, что побудило одного рецензента назвать Лайма новым «великим имитатором». [130] Поскольку у всех людей с поздней стадией инфекции тест на антитела будет положительным, простой анализ крови может исключить болезнь Лайма как возможную причину симптомов у человека. [131]
Укусы клещей можно предотвратить, избегая или сокращая время пребывания в вероятных местах обитания клещей и принимая меры предосторожности во время пребывания в них и при выходе из них. [132] [8]
Большинство случаев заражения человека болезнью Лайма вызвано укусами нимфы Ixodes в период с апреля по сентябрь. [27] [132] Клещи предпочитают влажные, затененные места в лесах , кустарниках, высокой траве, опавших листьях или деревянных кучах. [27] [133] Плотность клещей, как правило, самая высокая в лесных массивах, за которыми следуют неухоженные края между лесом и газонами (около половины), декоративные растения и многолетние почвопокровные растения (около четверти), а также газоны (примерно в 30 раз меньше). [134] Личинки и нимфы Ixodes, как правило, многочисленны и там, где гнездятся мыши, например, в каменных стенах и деревянных бревнах. [134] Личинки и нимфы Ixodes обычно ждут потенциальных хозяев («поиски») на листьях или траве близко к земле с вытянутыми передними лапами; Когда хозяин касается его конечностей, клещ быстро цепляется и взбирается на хозяина в поисках места на коже, чтобы укусить. [135] По оценкам, на северо-востоке США 69% укусов клещей происходят в жилых домах, 11% — в школах и лагерях, 9% — в парках и зонах отдыха, 4% — на работе, 3% — во время охоты и 4% — в других местах. области. [134] Действия, связанные с укусами клещей в жилых помещениях, включают работу во дворе, расчистку кустарника, работу в саду, игры во дворе и впуск в дом собак или кошек, которые бродят по лесистым или травянистым участкам. [134] [132] В парках укусы клещей часто случаются во время походов или кемпинга. [134] Ходить по скошенной лужайке или по центру тропы, не касаясь прилегающей растительности, менее рискованно, чем ползать или сидеть на бревенчатой или каменной стене. [134] [136] Домашним животным не следует позволять свободно бродить в вероятных местах обитания клещей. [133]
В качестве меры предосторожности CDC рекомендует замачивать или опрыскивать одежду, обувь и туристическое снаряжение, такое как палатки, рюкзаки и спальные мешки, 0,5% раствором перметрина и развешивать их для просушки перед использованием. [132] [137] Перметрин не имеет запаха и безопасен для человека, но очень токсичен для клещей. [138] Проползая по обработанной перметрином ткани всего 10–20 секунд, нимфы клещей раздражаются, отпадают или умирают. [138] [139] Обувь и носки с закрытым носком, обработанные перметрином, уменьшают в 74 раза количество укусов нимф, которые впервые контактируют с обувью человека, также носящего обработанные шорты (поскольку нимфы обычно ищут у земли, это типичный сценарий контакта). [138] Лучшей защиты можно добиться, заправляя обработанные перметрином брюки (брюки) в обработанные носки и обработанную рубашку с длинными рукавами в брюки, чтобы свести к минимуму зазоры, через которые клещ может попасть на кожу пользователя. [136] Светлая одежда поможет легче увидеть клещей и удалить их до того, как они укусят. [136] Обработанная перметрином униформа военных и рабочих на открытом воздухе снижает количество случаев укусов на 80–95%. [139] Защита перметрином сохраняется в течение нескольких недель ношения и стирок для вещей, обработанных клиентом, и до 70 стирок для вещей, обработанных на заводе. [137] Перметрин не следует наносить на кожу человека, нижнее белье или кошек. [137] [140]
Агентство по охране окружающей среды рекомендует использовать на открытых участках кожи несколько репеллентов от клещей, в том числе ДЭТА , пикаридин , IR3535 (производное аминокислоты бета-аланина), масло лимонного эвкалипта (OLE, натуральное соединение) и активный ингредиент OLE пара-ментан-диол ( ПМД) . [132] [141] [142] В отличие от перметрина, репелленты отталкивают, но не убивают клещей, защищают только в течение нескольких часов после нанесения и могут быть смыты потом или водой. [137] Самым популярным репеллентом является ДЭТА в США и пикаридин в Европе. [142] В отличие от ДЭТА, пикаридин не имеет запаха и с меньшей вероятностью вызовет раздражение кожи или повреждение ткани или пластика. [142] Репелленты с более высокой концентрацией могут действовать дольше, но не более эффективны; против клещей 20% пикаридин может действовать в течение 8 часов по сравнению с 55–98,11% ДЭТА в течение 5–6 часов или 30–40% OLE в течение 6 часов. [137] [141] Репелленты не следует наносить под одежду, на глаза, рот, раны или порезы, а также на детей младше 2 месяцев (3 лет при ОЛ или ПМД). [137] [132] Если используется солнцезащитный крем , поверх него следует нанести репеллент. [137] Репелленты не следует распылять непосредственно на лицо, их следует распылять на руку, а затем втирать в лицо. [137]
После входа в помещение следует проверить одежду, снаряжение и домашних животных на наличие клещей. [132] Одежду можно положить в горячую сушилку на 10 минут, чтобы убить клещей (простой стирки или теплой сушилки недостаточно). [132] Принятие душа как можно скорее, поиск клещей по всему телу и их удаление снижают риск заражения. [132] Некормленные нимфы клеща имеют размер макового зернышка, но через день-два после укуса и прикрепления к человеку они выглядят как небольшой кровяной пузырь . [143] Особенно тщательно следует проверять следующие области: подмышки, между ног, заднюю часть колен, пупок, туловище, а у детей — уши, шею и волосы. [132]

Прикрепившиеся клещи следует немедленно удалить. Риск заражения увеличивается со временем прикрепления, но в Северной Америке риск болезни Лайма невелик, если клеща удалить в течение 36 часов. [144] Центры по контролю и профилактике заболеваний рекомендуют вставлять пинцет с тонким кончиком между кожей и клещом, крепко сжимая его и вытягивая закрытый пинцет прямо из кожи, не скручивая, не дергая, не сжимая и не раздавливая клеща. [145] После удаления клеща все части клеща, оставшиеся на коже, следует по возможности удалить чистым пинцетом. [145] Затем рану и руки следует промыть спиртом или водой с мылом. [145] От клеща можно избавиться, поместив его в контейнер со спиртом, запечатанный пакет, скотч или спустив в унитаз. [145] Укушенный человек должен записать, где и когда произошел укус, чтобы можно было сообщить об этом врачу, если в ближайшие несколько недель у человека появится сыпь или симптомы гриппа. [145] CDC рекомендует не использовать пальцы, лак для ногтей, вазелин или нагревать клеща, чтобы попытаться удалить его. [145]
В Австралии, где распространен австралийский паралитический клещ , Австралазийское общество клинической иммунологии и аллергии рекомендует не использовать пинцет для удаления клещей, поскольку если у человека аллергия, это может привести к анафилаксии . [146] Вместо этого следует распылить средство на клеща, чтобы он замерз, а затем отпал. [146] Другой метод заключается в использовании около 20 см зубной нити или лески для медленного завязывания узла между кожей и клещом, а затем его отрывания от кожи. [147] [148]
Риск передачи инфекции увеличивается с продолжительностью прикрепления клеща. [27] Для бактерий, которые заставляют Лайм проникать изнутри клеща в его слюну, требуется от 36 до 48 часов. [27] Если оленьий клещ, который с достаточной вероятностью является переносчиком боррелий, обнаружен прикрепленным к человеку и удален, а также если клещ был прикреплен в течение 36 часов или набух, необходимо ввести однократную дозу доксициклина в течение 72 часов после удаления. может снизить риск болезни Лайма. Обычно это не рекомендуется всем укушенным людям, так как развитие инфекции происходит редко: около 50 укушенных людей должны лечиться таким образом, чтобы предотвратить один случай мигрирующей эритемы (т. е. типичной сыпи, обнаруживаемой примерно у 70–80% инфицированных людей). ). [3] [27]
Некоторые методы озеленения могут снизить риск укусов клещей во дворах жилых домов. [143] [149] К ним относятся подстригание газонов, удаление опавших листьев и сорняков, а также отказ от использования почвенного покрова. [143] Для отделения газонов от деревянных свай, лесных массивов , каменных стен и кустарников рекомендуется использовать барьер из камня или древесной щепы шириной 3 фута . [149] Без растительности на барьере клещи, как правило, не пересекают его; на него также можно распылять акарициды для уничтожения клещей. [149] Зона, безопасная для клещей, находящаяся на расстоянии не менее 9 футов от барьера, должна концентрировать человеческую деятельность во дворе, включая любые внутренние дворики, игровые площадки и сады. [149] Такие материалы, как деревянный настил, бетон, кирпич, гравий или щепа, используемые на земле под внутренними двориками и игровыми площадками, отпугивают там клещей. [143] Может быть добавлен забор высотой 8 футов, чтобы держать оленей подальше от зоны, безопасной для клещей. [149] [143]
Работники, работающие на открытом воздухе, подвергаются риску заболевания болезнью Лайма, если работают на участках, зараженных клещами. Это включает в себя строительство, ландшафтный дизайн, лесное хозяйство, расчистку кустарников, геодезию, сельское хозяйство, работы на железных дорогах, работы на нефтяных месторождениях, работы на инженерных линиях, управление парками или дикой природой. [150] [151] Работники северо-восточных и северо-центральных штатов США подвергаются наибольшему риску заражения инфицированными клещами. Клещи могут также передавать работникам этих и других регионов страны другие клещевые заболевания. На рабочих площадках с лесом, кустами, высокой травой или опавшими листьями клещей может быть больше. Работникам, работающим на открытом воздухе, следует быть особенно осторожными, чтобы защитить себя поздней весной и летом, когда молодые клещи наиболее активны. [152]
Клещи могут питаться кровью самых разных видов хозяев, включая ящериц , птиц , мышей , кошек , собак , оленей , крупный рогатый скот и людей . Степень, в которой клещ может питаться, размножаться и распространяться, будет зависеть от типа и доступности его хозяев. Будет ли он распространять болезнь, также зависит от его доступных хозяев. Некоторые виды, такие как ящерицы, называются «хозяевами разбавления», поскольку они не склонны поддерживать возбудителей болезни Лайма и, таким образом, снижают вероятность того, что болезнь будет передана питающимися ими клещами. Белохвостый олень является одновременно источником пищи и «репродуктивным хозяином», где клещи имеют тенденцию спариваться. Белоногая мышь является резервуарным хозяином , в котором может выжить возбудитель болезни Лайма. Наличие хозяев может оказать существенное влияние на передачу болезни Лайма. Большее разнообразие хозяев или тех, кто не поддерживает возбудитель, имеет тенденцию снижать вероятность передачи заболевания. [153]
В Соединенных Штатах одним из подходов к снижению заболеваемости болезнью Лайма и другими клещевыми болезнями оленей является значительное сокращение популяции оленей, от которой взрослые клещи зависят в плане питания и размножения. Случаи болезни Лайма снизились после уничтожения оленей на острове Монхеган, штат Мэн , [154] и после борьбы с оленями в бухте Мамфорд, штат Коннектикут. [155] Защитники предложили сократить популяцию оленей до уровня 8–10 оленей на квадратную милю по сравнению с уровнями 60 или более оленей на квадратную милю в районах страны с самым высоким уровнем заболеваемости болезнью Лайма. [156]
Другие отметили, что, хотя олени являются репродуктивными хозяевами, они не являются резервуарами Borrelia burgdorferi . Исследователи предположили, что более мелкие и менее заметные резервуары Лайма, такие как белоногие мыши и восточные бурундуки , могут более сильно влиять на возникновение болезни Лайма. Исследования экосистемы в штате Нью-Йорк показывают, что белоногие мыши процветают, когда леса разбиты на более мелкие изолированные участки леса с меньшим количеством хищников-грызунов. Чем больше грызунов являются переносчиками болезни, тем выше вероятность того, что клещ будет питаться грызуном-переносчиком болезни, и что кто-то подхватит клеща-переносчика болезни в своем саду или на прогулке в лесу. Данные показывают, что чем меньше лесная площадь, тем больше на ней будет клещей и тем выше вероятность, что они переносят болезнь Лайма, что подтверждает идею о том, что вырубка лесов и фрагментация среды обитания влияют на клещей, хозяев и передачу болезней. [153]
По оценкам, клещевыми болезнями поражаются около 80% крупного рогатого скота во всем мире. [157] Они также поражают кошек, собак и других домашних животных. Регулярный ветеринарный контроль клещей домашних животных с использованием акарицидов был предложен как способ снижения воздействия клещей на человека. Однако химический контроль с помощью акарицидов в настоящее время подвергается критике по ряду причин. У клещей развивается устойчивость к акарицидам; акарициды стоят дорого; и существуют опасения по поводу их токсичности и возможности воздействия химических остатков на продукты питания и окружающую среду. [158]
В Европе известными резервуарами Borrelia burgdorferi были 9 мелких млекопитающих, 7 млекопитающих среднего размера и 16 видов птиц (включая воробьиных, морских птиц и фазанов). [159] Эти животные, по-видимому, передают спирохеты клещам и, таким образом, участвуют в естественной циркуляции B. burgdorferi в Европе. Подозреваются также домовая мышь и другие виды мелких грызунов, особенно в Восточной Европе и России. [159] «Видами-резервуарами, содержащими наибольшее количество патогенов, являются европейская косуля Capreolus capreolus ; [160] « похоже, что она не служит основным резервуаром B. burgdorferi », - считают Дженсон и др. (1992) [161] (некомпетентный хозяин для B. burgdorferi и вируса КЭ), но важен для питания таких клещей, [162] как благородный олень и дикий кабан ( Sus scrofa ), [160] у которых были идентифицированы один вид Rickettsia и три вида Borrelia », [ 160] с высоким риском коинфекции косули. [163] Тем не менее, в 2000-х годах у косуль в Европе « было выявлено два вида Rickettsia и два вида Borrelia ». [160]
По состоянию на 2023 год [обновлять]человеческих вакцин от болезни Лайма не было. [26] Единственной человеческой вакциной, вышедшей на рынок, была LYMErix, которая была доступна с 1998 года, но прекращена в 2002 году . [164] В третьем квартале 2022 года планировалось начать третью фазу испытаний вакцины-кандидата VLA15, наряду с другими исследованиями. непрерывный. Для профилактики болезни Лайма у собак доступно несколько вакцин.
Вакцина LYMErix была доступна с 1998 по 2002 год. Рекомбинантная вакцина против болезни Лайма, основанная на белке внешней поверхности A (OspA) B. burgdorferi с гидроксидом алюминия в качестве адъюванта, была разработана компанией SmithKline Beecham . В клинических испытаниях с участием более 10 000 человек было обнаружено, что вакцина обеспечивает защитный иммунитет к болезни Лайма у 76% взрослых после трех доз только с легкими или умеренными и преходящими побочными эффектами . [165] [166] 21 декабря 1998 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило LYMErix на основании этих испытаний на людях в возрасте от 15 до 70 лет. [166] [164]
После одобрения вакцины ее внедрение в клиническую практику было медленным по ряду причин, включая ее стоимость, которая часто не возмещалась страховыми компаниями. [167] Впоследствии сотни получателей вакцины сообщили, что у них развились аутоиммунные и другие побочные эффекты. При поддержке некоторых правозащитных групп против GlaxoSmithKline был подан ряд коллективных исков , в которых утверждалось, что вакцина вызвала эти проблемы со здоровьем. Эти заявления были расследованы FDA и Центрами по контролю заболеваний, которые не обнаружили никакой связи между вакциной и аутоиммунными жалобами. [168]
Несмотря на отсутствие доказательств того, что жалобы были вызваны вакциной, продажи резко упали, и компания GlaxoSmithKline отозвала LYMErix с рынка США в феврале 2002 г. [169] на фоне негативного освещения в СМИ и опасений по поводу побочных эффектов вакцины. [168] [170] Судьба LYMErix была описана в медицинской литературе как «поучительная история»; [170] в редакционной статье журнала Nature отзыв LYMErix был назван примером того, как «необоснованные общественные опасения оказывают давление на разработчиков вакцин, выходящее за рамки разумных соображений безопасности». [171] Первоначальный разработчик вакцины OspA в Институте Макса Планка рассказал журналу Nature : «Это просто показывает, насколько иррациональным может быть мир… Не было никакого научного обоснования для отказа от первой вакцины OspA LYMErix». [168] [172]
Вальнева разработала кандидатную вакцину VLA15 на основе субъединиц шестивалентного белка (OspA) . В июле 2017 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предоставило ей ускоренный статус . [173] [174] В апреле 2020 года Pfizer заплатила 130 миллионов долларов за права на вакцину, и компании совместно разрабатывают ее, проводя несколько испытаний второй фазы. . [175]
Третья фаза испытаний VLA15 была запланирована на конец 2022 года с набором добровольцев на испытательных полигонах, расположенных на северо-востоке США и в Европе. [176] [177] Участники должны были получить первоначальную серию из трех доз вакцины в течение пяти-девяти месяцев, а затем ревакцинацию через двенадцать месяцев, причем как начальную серию, так и ревакцинацию планировалось завершить. до пикового сезона болезни Лайма в этом году. [177]
Вакцина мРНК, разработанная для того, чтобы вызвать сильный быстрый иммунный ответ на слюну клеща, позволила иммунной системе обнаружить и удалить клещей у подопытных животных до того, как они смогут передать инфекционные бактерии. [178] Вакцина содержит мРНК, необходимые организму для построения 19 белков в слюне клеща, которые, способствуя быстрому развитию эритемы (зудящего покраснения) в месте укуса, защищают морских свинок от болезни Лайма. Он также защитил подопытных животных, если клещ не был удален, если остался прикрепленным только один клещ, а не три. [179] [180]
Вакцины для собак были разработаны и одобрены для профилактики болезни Лайма у собак. В настоящее время доступны три вакцины против болезни Лайма. LymeVax, разработанный Fort Dodge Laboratories, содержит неповрежденные мертвые спирохеты, которые подвергают хозяина воздействию организма. Вакцина компании Intervet- Schering-Plough Galaxy Lyme нацелена на белки OspC и OspA . Антитела OspC убивают любые бактерии, которые не были убиты антителами OspA. Рекомбинантный препарат Лайма для собак, разработанный компанией Merial , вырабатывает антитела против белка OspA, поэтому клещ, питающийся вакцинированной собакой, всасывает кровь, полную антител против OspA, которые убивают спирохеты в кишечнике клеща до того, как они передаются собаке. [181]
Антибиотики являются основным методом лечения. [3] [27] Конкретный подход к их использованию зависит от конкретного человека и стадии заболевания. [27] Для большинства людей с ранней локализованной инфекцией пероральный прием доксициклина широко рекомендуется в качестве первого выбора, поскольку он эффективен не только против бактерий Borrelia , но и против множества других заболеваний, переносимых клещами. [27] Людям, принимающим доксициклин, следует избегать пребывания на солнце из-за более высокого риска солнечных ожогов . [35] Доксициклин противопоказан детям младше восьми лет и женщинам, которые беременны или кормят грудью; [27] альтернативами доксициклину являются амоксициллин , цефуроксим аксетил и азитромицин . [27] Азитромицин рекомендуется только в случае непереносимости других антибиотиков. [35] Стандартное лечение целлюлита , цефалексин , бесполезно при болезни Лайма. [35] Если неясно, вызвана ли сыпь болезнью Лайма или целлюлитом, IDSA рекомендует лечение цефуроксимом или амоксициллином/клавулановой кислотой , поскольку они эффективны против обеих инфекций. [35] Лица с ранней диссеминированной или поздней инфекцией Лайма могут иметь симптоматическое заболевание сердца, артрит Лайма или неврологические симптомы, такие как паралич лицевого нерва , радикулопатия , менингит или периферическая невропатия . [27] В таких случаях в качестве препарата первого выбора рекомендуется внутривенное введение цефтриаксона ; [27] в качестве альтернатив доступны цефотаксим и доксициклин. [27]
Схемы лечения болезни Лайма варьируются от 14 дней при раннем локализованном заболевании до 14–21 дня при раннем диссеминированном заболевании и до 14–28 дней при позднем диссеминированном заболевании. [182] Неврологические осложнения болезни Лайма можно лечить с помощью доксициклина , поскольку его можно принимать внутрь и он имеет более низкую стоимость, хотя в Северной Америке доказательства эффективности являются лишь косвенными. [117] В случае неудачи рекомендации рекомендуют повторное лечение инъекционным цефтриаксоном . [117] Если через несколько месяцев после лечения артрита Лайма отек суставов сохраняется или возвращается, можно рассмотреть возможность второго курса антибиотиков; внутривенные антибиотики предпочтительны для повторного лечения в случае плохой реакции на пероральные антибиотики. [27] [35] Помимо этого, длительный курс лечения антибиотиками продолжительностью более 28 дней не рекомендуется, поскольку нет доказательств его эффективности. [27] [183] Уровни антител IgM и IgG могут повышаться в течение многих лет даже после успешного лечения антибиотиками. [27] Поскольку уровень антител не является показателем успеха лечения, тестирование на них не рекомендуется. [27]
Паралич лицевого нерва может пройти без лечения; однако лечение антибиотиками рекомендуется для предотвращения других осложнений Лайма. [35] Кортикостероиды не рекомендуются, если паралич лицевого нерва вызван болезнью Лайма. [41] Людям с параличом лицевого нерва рекомендуется частое использование искусственных слез во время бодрствования, а также мазь и пластырь или заклеивание глаз во время сна. [41] [184]
Около трети людей с кардитом Лайма нуждаются во временном кардиостимуляторе до тех пор, пока не исчезнут нарушения сердечной проводимости, а 21% нуждаются в госпитализации. [43] Лайм-кардит не следует лечить кортикостероидами. [43]
Людям с артритом Лайма следует ограничить уровень физической активности, чтобы не повредить пораженные суставы, а в случае хромоты следует использовать костыли. [185] Боль, связанную с болезнью Лайма, можно лечить с помощью нестероидных противовоспалительных препаратов (НПВП). [35] Инъекции кортикостероидов в суставы не рекомендуются при артрите Лайма, который лечат антибиотиками. [35] [185] Люди с артритом Лайма, получавшие внутривенные антибиотики или пероральные антибиотики в течение двух месяцев, у которых через два месяца после лечения продолжает наблюдаться отек суставов и имеют отрицательный результат ПЦР на ДНК боррелий в синовиальной жидкости, считаются постантибиотическим заболеванием Лайма. артрит; это чаще встречается после заражения определенными штаммами боррелий у людей с определенными генетическими и иммунологическими характеристиками. [35] [52] [185] Пост-антибиотический артрит Лайма можно симптоматически лечить с помощью НПВП, модифицирующих течение заболевания противоревматических препаратов (БПВП), артроскопической синовэктомии или физиотерапии. [52] [185]
Людей, получающих лечение, следует информировать о возможности повторного заражения и о том, как его предотвратить. [112]
Типичный первый признак болезни Лайма — сыпь мигрирующей эритемы (МЭ) — проходит в течение нескольких недель даже без лечения. [3] Однако у нелеченых людей инфекция часто распространяется на нервную систему, сердце или суставы, что может привести к необратимому повреждению тканей организма. [35]
Наилучшие перспективы имеют люди, которые получают рекомендованное лечение антибиотиками в течение нескольких дней после появления первоначальной ЭМ-сыпи. [110] Восстановление не может быть полным или немедленным. Процент людей, достигших полного выздоровления в Соединенных Штатах, увеличивается примерно с 64–71% в конце лечения ЭМ-сыпи до примерно 84–90% через 30 месяцев; более высокие проценты зарегистрированы в Европе. [186] [187] Неэффективность лечения, т.е. сохранение исходных или появление новых признаков заболевания, наблюдается лишь у небольшого числа людей. [186] Остальные люди считаются выздоровевшими, но продолжают испытывать субъективные симптомы, например , боли в суставах или мышцах или усталость . [188] Эти симптомы обычно легкие и не приводят к инвалидности. [188]
У людей, получающих лечение только после проявления заболевания со стороны нервной системы, помимо субъективных симптомов может возникнуть объективный неврологический дефицит. [35] В Европе в среднем через 32–33 месяца после появления первых симптомов Лайма у людей, получавших в основном доксициклин по 200 мг в течение 14–21 дня, процент людей с затяжными симптомами был намного выше среди тех, у кого диагностирован нейроборрелиоз ( 50%) чем среди тех, у кого только ЭМ-сыпь (16%). [189] В другом европейском исследовании, через 5 лет после лечения нейроборрелиоза, сохраняющиеся симптомы реже встречались у детей (15%), чем у взрослых (30%), а в последнем исследовании они были реже среди тех, кто лечился в течение 30 дней после появления первых симптомов. (16%), чем среди тех, кто лечился позже (39%); среди тех, у кого сохранялись симптомы, 54% были ограничены в повседневной деятельности, а 19% находились на больничном или были нетрудоспособны. [190]
Некоторые данные показывают, что около 90% параличов лицевого нерва Лайма , лечившихся антибиотиками, полностью выздоравливают в среднем через 24 дня после появления, а большинство остальных выздоравливают с лишь легкими отклонениями. [191] [192] Однако в Европе у 41% людей, лечившихся от лицевого паралича, при наблюдении до 6 месяцев спустя наблюдались другие сохраняющиеся симптомы, в том числе у 28% - онемение или изменение чувствительности и у 14% - усталость или проблемы с концентрацией внимания. [192] Паралич обеих сторон лица связан с более тяжелым и длительным периодом восстановления. [191] [192] Исторические данные показывают, что нелеченные люди с параличом лицевого нерва выздоравливают почти с такой же скоростью, но у 88% впоследствии развивается артрит Лайма. [191] [193] Другие исследования показывают, что синкинезии (непроизвольные движения лицевой мышцы при произвольном движении другой мышцы) могут стать очевидными только через 6–12 месяцев после того, как паралич лицевого нерва, по-видимому, разрешился, поскольку поврежденные нервы восстанавливаются и иногда соединяются с неправильными. мышцы. [194] Синкинезия связана с применением кортикостероидов . [194] При долгосрочном наблюдении 16–23% случаев паралича лицевого нерва Лайма не выздоравливают полностью. [194]
В Европе около четверти людей с синдромом Баннварта ( радикулопатия Лайма и лимфоцитарный менингит ), получавших внутривенное введение цефтриаксона в течение 14 дней (в среднем через 30 дней после появления первых симптомов), пришлось пройти повторное лечение через 3–6 месяцев из-за неудовлетворительного клинического ответа или сохраняющейся объективной цели . маркеры инфекции в спинномозговой жидкости ; через 12 месяцев 64% полностью выздоровели, у 31% наблюдались легкие или редкие симптомы, не приводящие к инвалидности, которые не требовали регулярного использования анальгетиков, а у 5% были симптомы, которые приводили к инвалидности или требовали значительного использования анальгетиков. [40] Наиболее распространенными сохраняющимися симптомами, не приводящими к инвалидности, были головная боль, усталость , изменение чувствительности , боли в суставах , нарушения памяти , недомогание , корешковые боли , нарушения сна , мышечные боли и нарушения концентрации . Затяжные симптомы, приводящие к инвалидности, включали паралич лицевого нерва и другие нарушения движений . [40]
Выздоровление от позднего нейроборрелиоза обычно занимает больше времени и является менее полным, чем при раннем нейроборрелиозе, вероятно, из-за необратимых неврологических повреждений. [35]
Примерно у половины людей с кардитом Лайма развивается полная блокада сердца , но она обычно проходит в течение недели. [43] Другие нарушения сердечной проводимости Лайма обычно разрешаются в течение 6 недель. [43] Около 94% людей полностью выздоравливают, но 5% нуждаются в постоянном кардиостимуляторе , а у 1% возникает стойкая блокада сердца (фактический процент может быть выше из-за невыявленных случаев). [43] Осложнения Лайма -миокарда обычно легкие и проходят самостоятельно. [43] Однако в некоторых случаях Лайм-кардит может привести к летальному исходу. [43]
Рекомендуемое лечение антибиотиками эффективно примерно в 90% случаев артрита Лайма, хотя разрешение воспаления может занять несколько месяцев, и часто требуется второй курс антибиотиков. [35] Рефрактерный к антибиотикам артрит Лайма также в конечном итоге разрешается, обычно в течение 9–14 месяцев (диапазон от 4 месяцев до 4 лет); БПВП или синовэктомия могут ускорить выздоровление. [185]
Повторное заражение не является редкостью. В исследовании, проведенном в США, у 6–11% людей, лечившихся от ЭМ-сыпи, в течение 30 месяцев наблюдалась еще одна ЭМ-сыпь. [186] Вторая сыпь обычно возникает из-за заражения другим штаммом боррелий . [195]
Хронические симптомы, такие как боль, усталость или когнитивные нарушения, испытывают 10–20% людей, заразившихся болезнью Лайма, даже после завершения лечения. [196] [197] Причина неизвестна. Одна из гипотез заключается в том, что аутоиммунитет, вызванный инфекцией, может сохраняться в течение длительного времени после устранения вызвавшей инфекции. Известно, что аутоиммунные реакции возникают после других инфекций, в том числе кампилобактерий ( синдром Гийена-Барре ), хламидиоза (реактивный артрит) и ангины (ревмокардит). Другая причина заключается в том, что стойкая, трудно поддающаяся обнаружению инфекция вызывает PTLDS. Третье предположение заключается в том, что симптомы не связаны с предыдущим случаем болезни Лайма, а имеют другие причины. [197]
Доказанного лечения PTLDS не существует. В то время как антибиотики кратковременного действия эффективны на ранних стадиях болезни Лайма, антибиотики длительного действия неэффективны. В плацебо-контролируемых исследованиях они оказались неэффективными и несут риск серьезных, иногда смертельных осложнений. Как правило, лечение является симптоматическим и аналогично лечению фибромиалгии или ME/CFS . PTLDS обычно со временем становится лучше, но восстановление может занять много месяцев. [197]

Болезнь Лайма регулярно встречается в регионах с умеренным климатом Северного полушария . [198] По оценкам, в Соединенных Штатах болезнь диагностируется и лечится у 476 000 человек в год. Это число, вероятно, завышено из-за гипердиагностики и чрезмерного лечения. [5] [6] Ежегодно в Европе диагностируют и лечат более 200 000 человек. [7] [3] [199] Существует предположение, что популяция клещей и возникновение болезни Лайма увеличиваются и распространяются на новые территории, отчасти из-за потепления и изменения климата . Однако системы клещевых заболеваний сложны, и определить, вызваны ли изменения изменением климата или другими факторами, может быть сложно. [153] [200]
В Северной Африке B. burgdorferi sensu lato был идентифицирован в Марокко , Алжире , Египте и Тунисе . [201] [202] [203]
Болезнь Лайма в странах Африки к югу от Сахары в настоящее время неизвестна, но данные указывают на то, что она может встречаться у людей в этом регионе. Обилие хозяев и клещей-переносчиков будет способствовать распространению инфекции Лайма в Африке. [204] В Восточной Африке два случая болезни Лайма были зарегистрированы в Кении . [205] По данным Федерации обществ инфекционных заболеваний Южной Африки, болезнь Лайма не является эндемической ни в Южной Африке, ни в Мозамбике. [206]
Клещи, зараженные B. burgdorferi sensu lato, чаще встречаются в Японии, а также на северо-западе Китая, Непале , Таиланде и Дальнем Востоке России. [207] [208] Боррелии также были выделены в Монголии . [209]
Болезнь Лайма не считается эндемической для Австралии. [210] Хотя были сообщения о людях, заразившихся болезнью Лайма в Австралии, и даже были свидетельства наличия близкородственных видов Borrelia у клещей, [211] доказательства, связывающие эти случаи с местной передачей, ограничены. В Австралии продолжаются исследования по определению потенциальных видов Borrelia , вызывающих изнурительные симптомокомплексы, связанные с клещами (DSCATT). [212]
В Европе болезнь Лайма вызывается инфицированием одним или несколькими патогенными европейскими геновидами спирохеты B. burgdorferi sensu lato , в основном передаваемыми клещом Ixodes ricinus . [213] Случаи заражения клещами B. burgdorferi sensu lato встречаются преимущественно в Центральной Европе, особенно в Словении и Австрии, но были изолированы почти во всех странах континента. [214] Число случаев в южной Европе, например в Италии и Португалии, намного меньше. [215] Число диагностированных случаев в некоторых западных странах, таких как Исландия, растет. [216] Болезнь Лайма в Исландии встречается редко. В среднем ежегодно диагностируется около 6–7 случаев, преимущественно локализованных инфекций, проявляющихся мигрирующей эритемой. Ни один из случаев не имел однозначного исландского происхождения, и ежегодное число случаев не увеличивалось. [217]
В Соединенном Королевстве число лабораторно подтвержденных случаев болезни Лайма неуклонно растет с тех пор, как в 1986 г. была введена добровольная отчетность [218] , когда в Великобритании и Ирландии вместе взятых было зарегистрировано 68 случаев. [219] В Великобритании было 23 подтвержденных случая в 1988 году и 19 в 1990 году, [220] но 973 в 2009 году [218] и 953 в 2010 году. [221] Предварительные данные за первые три квартала 2011 года показывают рост на 26%. за тот же период 2010 г. [222]
Однако считается, что фактическое количество случаев значительно превышает приведенные выше цифры: по оценкам Агентства по охране здоровья Великобритании , в год регистрируется от 2000 до 3000 случаев [221] (в среднем около 15 случаев). % инфекций, приобретенных за границей [218] ), в то время как д-р Даррел Хо-Йен, директор Шотландской справочной лаборатории токсоплазмы и Национальной службы тестирования на болезнь Лайма, считает, что число подтвержденных случаев следует умножить на 10, «чтобы принять во внимание ошибочные диагностированные случаи, тесты, дающие ложные результаты, пациенты, которые не прошли тестирование, люди, которые инфицированы, но не проявляют симптомов, неуведомление и инфицированные люди, которые не обращаются к врачу». [223] [224]
Несмотря на то, что болезнь Лайма ( инфекция Borrelia burgdorferi ) является заболеванием, подлежащим уведомлению в Шотландии [225] с января 1990 г. [226] , о котором поэтому следует сообщать на основании клинических подозрений, считается, что многие врачи общей практики не знают об этом требовании. [227] Обязательная отчетность, ограничивающаяся только результатами лабораторных анализов, была введена на всей территории Великобритании в октябре 2010 года в соответствии с Положением об охране здоровья (уведомление) 2010 года. [218]
Хотя большее число случаев болезни Лайма зарегистрировано в Нью-Форест , Солсбери-Плейн , Эксмур , Саут-Даунс , некоторых частях Уилтшира и Беркшира , Тетфорд-Форест [228] , а также на западном побережье и островах Шотландии, [229] зараженные клещами широко распространены, и их можно встретить даже в парках Лондона. [220] [230] В отчете 1989 года было обнаружено, что 25% работников лесного хозяйства в Нью-Форесте были серопозитивными , как и от 2% до 4–5% от общего местного населения в этом районе. [231] [232]
Тесты на домашних собаках, проведенные по всей стране в 2009 году, показали, что около 2,5% клещей в Великобритании могут быть инфицированы, что значительно выше, чем считалось ранее. [233] [234] Предполагается, что глобальное потепление может привести к увеличению активности клещей в будущем, а также к увеличению количества времени, которое люди проводят в общественных парках, что увеличивает риск заражения. [235] Однако ни одно опубликованное исследование не доказало, что это так.
Многие исследования в Северной Америке изучали экологические и экологические корреляты количества людей, страдающих болезнью Лайма. Исследование 2005 года с использованием моделирования климатической пригодности I. scapularis прогнозировало, что изменение климата приведет к общему увеличению на 213% подходящих мест обитания переносчиков к 2080 году, с расширением на север в Канаде, повышением пригодности в центральной части США и уменьшением количества подходящих мест обитания и сокращения переносчиков в на юге США [236] Обзор опубликованных исследований, проведенный в 2008 году, пришел к выводу, что наличие лесов или лесных массивов было единственной переменной, которая постоянно повышала риск болезни Лайма, тогда как другие переменные окружающей среды показали мало или совсем не согласовывались между исследованиями. [237] Авторы утверждают, что факторы, влияющие на плотность клещей и риск для человека между участками, все еще плохо изучены, и что будущие исследования должны проводиться в течение более длительных периодов времени, стать более стандартизированными по регионам и включать существующие знания о региональной экологии болезни Лайма . [237]
Ареал клещей, способных переносить болезнь Лайма, расширился с ограниченной территории Онтарио и теперь включает районы южного Квебека, Манитобы, северного Онтарио, южного Нью-Брансуика, юго-запада Новой Шотландии и ограниченных частей Саскачевана и Альберты, а также Британской Колумбии. Случаи были зарегистрированы даже на востоке, вплоть до острова Ньюфаундленд. [109] [238] [239] [240] Прогноз на основе модели, сделанный Leighton et al. (2012) предполагают, что ареал клеща I. scapularis расширится в Канаду на 46 км/год в течение следующего десятилетия, при этом потепление климатических температур станет основным фактором увеличения скорости распространения. [241]
Исследование 2007 года показало, что инфекция Borrelia burgdorferi является эндемической для Мексики: четыре случая, зарегистрированные в период с 1999 по 2000 год. [242]
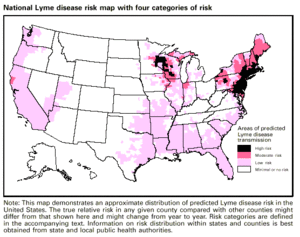
Болезнь Лайма — наиболее распространенное клещевое заболевание в Северной Америке и Европе и одно из самых быстрорастущих инфекционных заболеваний в Соединенных Штатах. Среди случаев, зарегистрированных в Центрах по контролю и профилактике заболеваний США, соотношение случаев заражения болезнью Лайма составляет 7,9 случаев на каждые 100 000 человек. В десяти штатах, где болезнь Лайма наиболее распространена, в 2005 году средний показатель составил 31,6 случаев на каждые 100 000 человек. [243] [244] [245]
Хотя болезнь Лайма была зарегистрирована во всех штатах из-за инфекций, связанных с поездками, около 99% всех зарегистрированных случаев ограничиваются всего лишь пятью географическими областями (Новая Англия, Центральная Атлантика, Восточно-Северо-Центральная, Южная Атлантика и Западно-Северо-Атлантический регион). Центральный). [83] [246] [247] CDC внедрил национальный надзор за случаями болезни Лайма в 1991 году. С тех пор критерии отчетности менялись несколько раз. [248] В определении эпиднадзора 2022 года случаи классифицируются как подтвержденные, вероятные и подозрительные. [249]
CDC подчеркивает, что, хотя данные эпиднадзора имеют ограничения, они полезны из-за «единообразности, простоты и своевременности». Хотя в районах с высоким уровнем заболеваемости случаи занижаются, в районах с низким уровнем заболеваемости вероятно завышение показателей. Кроме того, случаи эпиднадзора регистрируются по округу проживания, а не по месту обязательного заражения. [250] [83]
Число зарегистрированных случаев заболевания растет, как и эндемичные регионы Северной Америки. Например, ранее считалось, что способность B. burgdorferi sensu lato поддерживаться в энзоотическом цикле в Калифорнии ограничена, поскольку предполагалось, что большая популяция ящериц уменьшит количество людей, пораженных B. burgdorferi, в местных популяциях клещей. ; с тех пор это было поставлено под сомнение, поскольку некоторые данные свидетельствуют о том, что ящерицы могут заразиться. [251]
За исключением одного исследования, проведенного в Европе, [252] большая часть данных о ящерицах основана на обнаружении ДНК спирохет и не продемонстрировала, что ящерицы способны заражать питающихся ими клещей. [251] [253] [254] [255] Поскольку некоторые эксперименты показывают, что ящерицы невосприимчивы к заражению боррелиями , вполне вероятно, что их участие в энзоотическом цикле является более сложным и видоспецифичным. [77]
В то время как B. burgdorferi чаще всего ассоциируется с клещами, переносчиками которых являются белохвостые олени и белоногие мыши , Borrelia afzelii чаще всего выявляется у клещей- переносчиков , питающихся грызунами , а Borrelia garinii и Borrelia valaisiana , по-видимому, связаны с птицами. И грызуны, и птицы являются компетентными резервуарными хозяевами B. burgdorferi sensu stricto . Устойчивость геновида спирохет болезни Лайма к бактериолитической активности альтернативного пути комплемента различных видов-хозяев может определять его ассоциацию с резервуарным хозяином. [252]
Могут существовать несколько схожих, но явно различных состояний, вызванных различными видами или подвидами Borrelia в Северной Америке. Регионально ограниченным заболеванием, которое может быть связано с инфекцией Borrelia , является сыпь, связанная с южными клещами (STARI), также известная как болезнь Мастерса. Amblyomma americanum , широко известная как клещ одинокой звезды, признана основным переносчиком STARI. В некоторых частях географического распространения STARI болезнь Лайма встречается довольно редко (например, в Арканзасе), поэтому людям в этих регионах, у которых наблюдаются симптомы, подобные Лайму, — особенно если они следуют за укусом клеща одинокой звезды, — следует рассматривать STARI как возможность. Обычно это более легкое заболевание, чем заболевание Лайма, и оно обычно хорошо поддается лечению антибиотиками. [256]
В последние годы в Монтане регистрируется от 5 до 10 случаев заболевания, похожего на болезнь Лайма, в год. Встречается в основном в районах вдоль реки Йеллоустоун в центральной Монтане. У людей вокруг укуса клеща появляется красная сыпь в форме «бычьего глаза», за которой следуют недели усталости и лихорадка. [247]
Последствия болезни Лайма сопоставимы среди мужчин и женщин. Заболеванию подвержены самые разные возрастные группы, хотя наибольшее число случаев приходится на детей в возрасте от 10 до 19 лет. По неизвестным причинам болезнь Лайма в семь раз чаще встречается среди азиатов. [257]
В Бразилии выявлена болезнь Лайма, известная как синдром Баджо–Йошинари , вызываемая микроорганизмами, не принадлежащими к комплексу B. burgdorferi sensu lato , и передающаяся клещами родов Amblyomma и Rhipicephalus . [258] Первый зарегистрированный случай BYS в Бразилии был зарегистрирован в 1992 году в Котиа , Сан-Паулу. [259]
Болезнь Лайма была впервые диагностирована как отдельное заболевание в 1975 году в Лайме, штат Коннектикут . [260]
Эволюционная история генетики Borrelia burgdorferi стала предметом недавних исследований. Одно исследование показало, что до лесовосстановления , которое сопровождало постколониальное закрытие ферм в Новой Англии и массовую миграцию на Средний Запад , произошедшую в начале 19-го века, болезнь Лайма присутствовала в Америке на протяжении тысячелетий и распространялась по всей территории Америки. с клещевыми хозяевами от Северо-Востока до Среднего Запада. [261]
Джон Джосселин, посетивший Новую Англию в 1638 году и еще раз с 1663 по 1670 год, писал: «Летом на кустах висит бесконечное количество клещей, которые присасываются к одежде человека, заползают в его штаны и за короткое время поедают себя в очень человеческое тело. Я видел чулки тех, кто ходил по лесу, покрытые ими». [262]
Это также подтверждают труды Питера Кальма , шведского ботаника, которого послал в Америку Линней и который обнаружил, что леса Нью-Йорка «изобилуют» клещами, когда он посетил его в 1749 году. Когда путешествие Кальма было прослежено 100 лет спустя, леса исчезли, и бактерия Лайма, вероятно, изолирована в нескольких очагах вдоль северо-восточного побережья, Висконсина и Миннесоты. [263]
Возможно, первое подробное описание того, что сейчас известно как болезнь Лайма, появилось в трудах Джона Уокера после посещения острова Джура (Олений остров) у западного побережья Шотландии в 1764 году. [264] Он дает хорошее описание и того, и другого. симптомов болезни Лайма (с «сильной болью во внутренних частях конечностей») и самого клеща-переносчика, которого он описывает как «червя» с телом «красноватого цвета и сжатая форма с рядом ножек с каждой стороны», «проникающих в кожу». Многие люди из этой области Великобритании эмигрировали в Северную Америку в период с 1717 года по конец 18 века. [ нужна цитата ]
Исследование сохранившихся музейных образцов выявило ДНК Borrelia у инфицированного клеща Ixodes ricinus из Германии, который датируется 1884 годом, а также у инфицированной мыши из Кейп-Кода, которая умерла в 1894 году . В двухлетней мумии обнаружено наличие последовательности ДНК Borrelia burgdorferi, что сделало его самым ранним известным человеком с болезнью Лайма. [265]
Ранние европейские исследования того, что сейчас известно как болезнь Лайма, описали ее кожные проявления. Первое исследование датируется 1883 годом в Бреслау , Германия (ныне Вроцлав , Польша), где врач Альфред Бухвальд описал человека, который в течение 16 лет страдал дегенеративным заболеванием кожи , теперь известным как хронический атрофический акродерматит . [266]
На исследовательской конференции 1909 года шведский дерматолог Арвид Афцелиус представил исследование расширяющегося кольцевидного поражения, которое он наблюдал у пожилой женщины после укуса овечьего клеща. Он назвал это поражение мигрирующей эритемой . [266] Заболевание кожи, теперь известное как боррелиальная лимфоцитома , было впервые описано в 1911 году. [267]
Современная история медицинского понимания этого заболевания, включая его причину, диагностику и лечение, была сложной. [268]
Неврологические проблемы после укусов клещей были признаны начиная с 1920-х годов. Французские врачи Гарен и Бюжаду описали у фермера болезненный сенсорный радикулит , сопровождавшийся легким менингитом после укуса клеща. Также отмечалась крупная кольцевидная сыпь, хотя врачи не связывали ее с менингорадикулитом. В 1930 году шведский дерматолог Свен Хеллерстрем был первым, кто предположил, что ЭМ и неврологические симптомы после укуса клеща связаны. [269] В 1940-х годах немецкий невролог Альфред Баннварт описал несколько случаев хронического лимфоцитарного менингита и полирадикулоневрита, некоторые из которых сопровождались эритематозными поражениями кожи.
Карл Леннхофф, работавший в Каролинском институте в Швеции, считал, что многие кожные заболевания вызываются спирохетами. В 1948 году он использовал специальное пятно для микроскопического наблюдения того, что, по его мнению, было спирохетами, при различных типах поражений кожи, включая ЭМ. [270] Хотя его выводы позже оказались ошибочными, интерес к изучению спирохет возник. В 1949 году Нильс Тирессон, который также работал в Каролинском институте, первым начал лечить АКА пенициллином. [271] В 1950-х годах взаимосвязь между укусом клеща, лимфоцитомой, ЭМ и синдромом Баннварта была признана во всей Европе, что привело к широкому использованию пенициллина для лечения в Европе. [272] [273]
В 1970 году дерматолог из Висконсина Рудольф Скрименти обнаружил ЭМ-поражение у человека после того, как вспомнил статью Хеллерстрема, которая была перепечатана в американском научном журнале в 1950 году. Это был первый задокументированный случай ЭМ в Соединенных Штатах. Судя по европейской литературе, он лечил человека пенициллином. [274]
Полный синдром, ныне известный как болезнь Лайма, не был распознан до тех пор, пока в 1975 году в трех городах на юго-востоке Коннектикута не была выявлена группа случаев, первоначально считавшихся ювенильным ревматоидным артритом , включая города Лайм и Олд-Лайм , которые и дали этому заболеванию популярное название. [275] Это исследовали врачи Дэвид Снидман и Аллен Стир из Службы эпидемической разведки , а также другие сотрудники Йельского университета , в том числе Стивен Малависта , который считается соавтором открытия этой болезни. [276] Признание того, что люди в Соединенных Штатах страдают ЭМ, привело к признанию того, что «артрит Лайма» был одним из проявлений того же клещевого заболевания, известного в Европе. [277]
До 1976 года элементы инфекции B. burgdorferi sensu lato назывались или были известны как клещевой менингополиневрит, синдром Гарина-Бюжаду, синдром Баннварта, болезнь Афцелиуса, [278] Коленная лихорадка Монтаука или овечья клещевая лихорадка. С 1976 года заболевание чаще всего называют болезнью Лайма, [279] [280] Лайм-боррелиозом или просто боррелиозом. [281] [282]
В 1980 году Стир и др. , начали тестировать схемы лечения антибиотиками у взрослых с болезнью Лайма. [283] В том же году эпидемиолог Департамента здравоохранения штата Нью-Йорк Хорхе Бенах предоставил Вилли Бургдорферу , исследователю биологической лаборатории Роки Маунтин , коллекции I. dammini [ scapularis ] с острова Шелтер, штат Нью-Йорк, известного лайм- эндемичный район в рамках продолжающегося расследования пятнистой лихорадки Скалистых гор. Исследуя клещей на наличие риккетсий, Бургдорфер заметил «плохо окрашенные, довольно длинные, неправильно закрученные спирохеты». Дальнейшее обследование выявило спирохеты у 60% клещей. Бургдорфер считает, что знакомство с европейской литературой помогло ему понять, что спирохеты могут быть «долгожданной причиной внеклеточного матрикса и болезни Лайма». Бенах предоставил ему еще больше клещей с острова Шелтер и сыворотку от людей, у которых диагностирована болезнь Лайма. Исследователь Центра медицинских наук Техасского университета Алан Барбур «предложил свой опыт в области культивирования и иммунохимической характеристики организма». Впоследствии Бургдорфер подтвердил свое открытие, выделив у людей с болезнью Лайма спирохеты, идентичные тем, которые обнаружены у клещей. [284] В июне 1982 года он опубликовал свои открытия в журнале Science , и в его честь спирохета была названа Borrelia burgdorferi . [285]
После идентификации B. burgdorferi как возбудителя болезни Лайма для тестирования были выбраны антибиотики, руководствуясь чувствительностью к антибиотикам in vitro , включая антибиотики тетрациклинового ряда , амоксициллин , цефуроксим аксетил , пенициллин для внутривенного и внутримышечного введения и цефтриаксон для внутривенного введения . [286] [287] Механизм передачи клещей также был предметом многочисленных дискуссий. Спирохеты B. burgdorferi были идентифицированы в слюне клещей в 1987 году, что подтверждает гипотезу о том, что передача происходит через слюнные железы клещей. [288]
Изменения ландшафта и урбанизация
Урбанизация и другие антропогенные факторы могут быть причастны к распространению болезни Лайма среди людей. Во многих районах расширение пригородных кварталов привело к постепенному вырубке окружающих лесных массивов и увеличению пограничных контактов между людьми и районами, густонаселенными клещами. Экспансия человека также привела к сокращению численности хищников, охотящихся на оленей, а также мышей, бурундуков и других мелких грызунов — основных резервуаров болезни Лайма. В результате увеличения числа контактов человека с хозяином и переносчиком вероятность передачи заболевания значительно возросла. [289] [290] Исследователи изучают возможную связь между глобальным потеплением и распространением трансмиссивных болезней, включая болезнь Лайма. [291]
Эффект разбавления
Учитывая эту динамику среды обитания и хозяина, некоторые исследователи начали предполагать, может ли эффект разбавления смягчить распространение болезни Лайма. [289] Эффект разбавления представляет собой гипотезу, которая предсказывает, что увеличение биоразнообразия хозяина приведет к уменьшению числа векторов, инфицированных B. burgdorferi . [289] Научные исследования показали, что распространенность нимфальных инфекций (NIP) снижается по мере увеличения числа видов-хозяев, что подтверждает эффект разбавления. [289] Тем не менее, эти результаты не следует ошибочно интерпретировать, предполагая, что существует прямая связь между снижением уровня NIP и снижением эпидемиологического риска, поскольку это еще не доказано. [289] Кроме того, важно отметить, что до сих пор эффект разбавления поддерживается только на северо-востоке США и был опровергнут в других частях мира, где также наблюдается высокий уровень заболеваемости болезнью Лайма [292]
Хроническая болезнь Лайма
Термин «хроническая болезнь Лайма» является спорным и не признан в медицинской литературе [293] , и большинство медицинских авторитетов не рекомендуют длительное лечение антибиотиками при болезни Лайма. [35] [117] [294] Исследования показали, что большинство людей с диагнозом «хроническая болезнь Лайма» либо не имеют объективных доказательств предыдущей или текущей инфекции B. burgdorferi , либо являются людьми, которых следует классифицировать как больных болезнью Лайма после лечения. синдром (PTLDS), который определяется как продолжающиеся или рецидивирующие неспецифические симптомы (такие как усталость, скелетно-мышечная боль и когнитивные жалобы) у человека, ранее лечившегося от болезни Лайма. [295]
Документальный фильм 2008 года « Под нашей кожей» известен тем, что продвигает противоречивые и непризнанные теории о «хронической болезни Лайма». [296]
Профилактика болезни Лайма является важным шагом в обеспечении безопасности собак в эндемичных районах. Доступны профилактическое образование и ряд профилактических мер. Во-первых, для владельцев собак, которые живут рядом или часто посещают места, зараженные клещами, важным шагом является плановая вакцинация их собак. [297]
Другой важной профилактической мерой является использование стойких акарицидов, таких как репелленты для местного применения или пестициды, содержащие триазапентадиены ( амитраз ), фенилпиразолы ( фипронил ) или перметрин ( пиретроиды ). [298] Эти акарициды нацелены в первую очередь на взрослые стадии клещей, переносящих болезнь Лайма, и уменьшают количество репродуктивно активных клещей в окружающей среде. [297] Составы этих ингредиентов доступны в различных формах для местного применения, включая точечные инъекции, спреи, порошки, пропитанные ошейники, растворы и шампуни. [298]
Осмотр собаки на наличие клещей после пребывания в зоне, зараженной клещами, является важной мерой предосторожности для профилактики болезни Лайма. Ключевые точки для осмотра — голова, шея и уши. [299]
У собак серьезный долгосрочный прогноз может привести к заболеванию клубочков [300] , которое представляет собой категорию поражения почек, которая может вызвать хроническое заболевание почек. [181] У собак также может возникнуть хроническое заболевание суставов, если заболевание не лечить. Однако в большинстве случаев болезни Лайма у собак происходит полное выздоровление при лечении антибиотиками, а иногда и без него. [301] [ необходима проверка ] В редких случаях болезнь Лайма может быть смертельной как для людей, так и для собак. [302]
В отличие от собак, кошки очень редко заражаются болезнью Лайма. Тем не менее, кошки способны заразиться B. burgdorferi после укуса инфицированного клеща. У кошек, инфицированных болезнью Лайма, могут проявляться симптомы, включая, помимо прочего, хромоту, усталость или потерю аппетита. [303] В двух случаях у инфицированных кошек наблюдались нарушения сердечной деятельности, аналогичные симптомам болезни Лайма как у собак, так и у людей. [304] Однако кошки, инфицированные болезнью Лайма, скорее всего, протекают бессимптомно и не проявляют заметных признаков заболевания. [304] [303] Кошек с болезнью Лайма часто лечат антибиотиками, как и других животных. В некоторых случаях может потребоваться дополнительное лечение или терапия. [303]
Хотя болезнь Лайма может возникнуть у лошадей, не каждая инфекция B. burgdorferi сопровождается симптомами. [305] В частности, обнаружения специфических антител только против B. burgdorferi недостаточно для диагностики болезни Лайма у лошадей, и неспецифическое тестирование на антитела не рекомендуется. [306]
Хотя некоторые коммерческие группы предлагают тестирование, в целом оно не рекомендуется.
Центры по контролю и профилактике заболеваний США опубликовали изображение кекса с маком, на котором некоторые из «маковых семян» на самом деле были клещами.
По сравнению с неиммунизированными морскими свинками, у вакцинированных животных, контактировавших с инфицированными клещами, быстро появлялось покраснение в месте укуса клеща. Ни у одного из иммунизированных животных не развилась болезнь Лайма, если клещей удаляли при появлении покраснения. Напротив, около половины контрольной группы заразились B. burgdorferi после удаления клеща. Когда один зараженный клещ был прикреплен к иммунизированным морским свинкам и не удален, ни одно из вакцинированных животных не заразилось по сравнению с 60 процентами контрольных животных. Однако защита иммунизированных морских свинок ослабевала, если на животном оставались три клеща. Клещи у иммунизированных животных не могли агрессивно питаться и вытеснялись быстрее, чем у морских свинок в контрольной группе.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка ){{cite journal}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка )Анализ данных CDC по VoxHealth
![]() В этой статье использованы общедоступные материалы о синдроме Лайма после лечения. Центры по контролю и профилактике заболеваний .
В этой статье использованы общедоступные материалы о синдроме Лайма после лечения. Центры по контролю и профилактике заболеваний .