Пенициллины ( P , PCN или PEN ) представляют собой группу β-лактамных антибиотиков, первоначально полученных из плесневых грибов Penicillium , главным образом P. chrysogenum и P. Rubens . Большинство пенициллинов, используемых в клинической практике, синтезируются P. chrysogenum с помощью глубокой ферментации в резервуарах [2] и затем очищаются. [3] [4] Был обнаружен ряд природных пенициллинов, но в клинической практике используются только два очищенных соединения: пенициллин G ( внутримышечное или внутривенное применение ) и пенициллин V (пероральный). Пенициллины были одними из первых лекарств, эффективных против многих бактериальных инфекций , вызываемых стафилококками и стрептококками . Они до сих пор широко используются при различных бактериальных инфекциях, хотя многие типы бактерий в результате интенсивного использования выработали устойчивость .
Десять процентов населения заявляют об аллергии на пенициллин , но поскольку частота положительных результатов кожных проб снижается на 10% с каждым годом избегания, 90% этих пациентов в конечном итоге могут переносить пенициллин. Кроме того, люди с аллергией на пенициллин обычно могут переносить цефалоспорины (еще одна группа β-лактамов), поскольку перекрестная реактивность иммуноглобулина E (IgE) составляет всего 3%. [5]
Пенициллин был открыт в 1928 году шотландским учёным Александром Флемингом как неочищенный экстракт P. Rubens . [6] Ученик Флеминга Сесил Джордж Пейн был первым, кто успешно применил пенициллин для лечения глазной инфекции ( неонатального конъюнктивита ) в 1930 году. Очищенное соединение (пенициллин F) было выделено в 1940 году исследовательской группой под руководством Говарда Флори и Эрнста Бориса Чейна в Оксфордский университет. Флеминг впервые применил очищенный пенициллин для лечения стрептококкового менингита в 1942 году . [7] Нобелевскую премию по физиологии и медицине 1945 года разделили Чейн, Флеминг и Флори.
Некоторые полусинтетические пенициллины эффективны против более широкого спектра бактерий: к ним относятся антистафилококковые пенициллины , аминопенициллины и антипсевдомонадные пенициллины .
Термин «пенициллин» определяется как натуральный продукт плесени Penicillium , обладающий противомикробной активностью. [8] Он был придуман Александром Флемингом 7 марта 1929 года, когда он обнаружил антибактериальные свойства Penicillium Rubens . [9] Флеминг объяснил в своей статье 1929 года в Британском журнале экспериментальной патологии, что «чтобы избежать повторения довольно громоздкой фразы «Фильтрат плесневого бульона», будет использоваться название «пенициллин». [10] Таким образом, название относится к научному названию формы, описанному Флемингом в его Нобелевской лекции в 1945 году:
Меня часто спрашивали, почему я придумал название «Пенициллин». Я просто следовал совершенно ортодоксальным линиям и придумал слово, которое объясняло, что вещество пенициллин было получено из растения рода Penicillium, точно так же, как много лет назад слово « Дигиталин » было изобретено для вещества, полученного из растения Наперстянка . [11]
В современном использовании термин «пенициллин» используется в более широком смысле для обозначения любого β-лактамного противомикробного препарата, который содержит тиазолидиновое кольцо, слитое с β-лактамным ядром, и может быть, а может и не быть натуральным продуктом. [12] Как и большинство натуральных продуктов, пенициллин присутствует в плесенях Penicillium в виде смеси активных компонентов ( гентамицин – еще один пример натурального продукта, который представляет собой нечеткую смесь активных компонентов). [8] Основные активные компоненты Penicillium перечислены в следующей таблице: [13] [14]
Другие второстепенные активные компоненты Penicillium включают пенициллин O , [20] [21] пенициллин U1 и пенициллин U6. Впоследствии было обнаружено , что другие названные компоненты природного пенициллина , такие как пенициллин А, не обладают антибиотической активностью и химически не связаны с пенициллинами-антибиотиками. [8]
Точный состав экстрагированного пенициллина зависит от вида используемой плесени Penicillium и от питательной среды, используемой для культивирования плесени. [8] Оригинальный штамм Penicillium Rubens , созданный Флемингом , производит в основном пенициллин F, названный в честь Флеминга. Но пенициллин F нестабилен, его трудно выделить, и он вырабатывается плесенью в небольших количествах. [8]
Основной коммерческий штамм Penicillium chrysogenum (штамм Peoria) продуцирует пенициллин G в качестве основного компонента, когда в качестве культуральной среды используется кукурузный отвар. [8] Когда в культуральную среду добавляют феноксиэтанол или феноксиуксусную кислоту, плесень вместо этого вырабатывает пенициллин V в качестве основного пенициллина. [8]
6-Аминопенициллановая кислота (6-АПК) представляет собой соединение, полученное из пенициллина G. 6-АПК содержит бета-лактамное ядро пенициллина G, но с оторванными боковыми цепями; 6-АПК является полезным предшественником для производства других пенициллинов. Существует множество полусинтетических пенициллинов, производных 6-АПК, которые делятся на три группы: антистафилококковые пенициллины, пенициллины широкого спектра действия и антипсевдомонадные пенициллины. Все полусинтетические пенициллины называются пенициллинами, поскольку все они в конечном итоге происходят из пенициллина G.
Использование единиц для назначения пенициллина является исторической случайностью и в значительной степени устарело за пределами США. Поскольку первоначальный пенициллин представлял собой нечеткую смесь активных соединений (аморфный желтый порошок), эффективность каждой партии пенициллина варьировалась от партии к партии. Поэтому было невозможно прописать 1 г пенициллина, поскольку активность 1 г пенициллина из одной серии отличалась бы от активности из другой серии. После производства каждую партию пенициллина необходимо было стандартизировать по известной единице пенициллина: затем каждый стеклянный флакон наполняли необходимым количеством единиц. В 1940-х годах стандартным стандартом был флакон объемом 5000 оксфордских единиц [24] , но в зависимости от партии он мог содержать от 15 до 20 мг пенициллина. Позже стандартом стал флакон в 1 000 000 международных единиц, который мог содержать от 2,5 до 3 г природного пенициллина (смесь пенициллинов I, II, III и IV и природных примесей). С появлением чистых препаратов пенициллина G (белого кристаллического порошка) нет смысла назначать пенициллин в дозах.
«Единица» пенициллина имела три предыдущих определения, и каждое определение было выбрано как примерно эквивалентное предыдущему.
Существует более старая единица пенициллина V, которая не эквивалентна нынешней единице пенициллина V. Причина в том, что FDA США ошибочно предположило, что эффективность пенициллина V такая же, как у пенициллина G. Фактически, пенициллин V менее эффективен, чем пенициллин G, и нынешняя единица пенициллина V отражает этот факт.
Аналогичный стандарт был установлен и для пенициллина К. [32]
Пенициллин G (бензилпенициллин) впервые был получен из гриба пенициллина , встречающегося в природе. Штамм гриба, используемый сегодня для производства пенициллина G, был создан методом генной инженерии для повышения выхода в производственном процессе. Ни один из других природных пенициллинов (F, K, N, X, O, U1 или U6) в настоящее время не используется в клинической практике.
Пенициллин V (феноксиметилпенициллин) получают путем добавления предшественника феноксиуксусной кислоты в среду, в которой культивируется генетически модифицированный штамм [ сомнительно ] грибка пенициллия .
Существуют три основные группы других полусинтетических антибиотиков, родственных пенициллинам. Их синтезируют путем добавления различных боковых цепей к предшественнику 6-АРА , выделенному из пенициллина G. Это антистафилококковые антибиотики, антибиотики широкого спектра действия и антипсевдомонадные антибиотики.
Антистафилококковые антибиотики называются так потому, что они устойчивы к расщеплению стафилококковой пенициллиназой . Поэтому их также называют устойчивыми к пенициллиназе.
Эту группу антибиотиков называют «широкого спектра действия», поскольку они активны в отношении широкого спектра грамотрицательных бактерий, таких как Escherichia coli и Salmonella typhi , для которых пенициллин не подходит. Однако в настоящее время резистентность этих организмов является обычным явлением.
Существует множество предшественников ампициллина. Это неактивные соединения, которые расщепляются в кишечнике с выделением ампициллина. Ни один из этих пролекарств ампициллина в настоящее время не используется:
Эпициллин – это аминопенициллин, который никогда не нашел широкого клинического применения.
Грамотрицательный вид Pseudomonas aeruginosa естественно устойчив ко многим классам антибиотиков. В 1960-е и 1970-е годы предпринималось множество попыток разработать антибиотики, активные против видов Pseudomonas . В группе есть два химических класса: карбоксипенициллины и уреидопенициллины. Все они вводятся инъекционно: ни один препарат нельзя вводить через рот.
Термин «пенициллин», используемый сам по себе, может относиться к любому из двух химических соединений : пенициллину G или пенициллину V.
Пенициллин G разрушается желудочной кислотой, поэтому его нельзя принимать внутрь, но можно назначать дозы до 2,4 г (намного выше, чем у пенициллина V). Его вводят внутривенно или внутримышечно. Его можно приготовить в виде нерастворимой соли, и в настоящее время используются две такие формы: прокаинпенициллин и бензатинбензилпенициллин , которые используются только при лечении сифилиса . Когда необходимо поддерживать высокую концентрацию в крови, пенициллин G необходимо вводить через относительно частые интервалы, поскольку он довольно быстро выводится из кровотока почками.
Пенициллин G лицензирован для лечения септицемии , эмпиемы , пневмонии , перикардита , эндокардита и менингита , вызванных чувствительными штаммами стафилококков и стрептококков. Он также лицензирован для лечения сибирской язвы , актиномикоза , заболеваний шейно-лицевой области, органов грудной клетки и брюшной полости, клостридиальных инфекций , ботулизма , газовой гангрены (с сопутствующей хирургической обработкой и/или хирургическим вмешательством по показаниям), столбняка (в качестве дополнительной терапии к человеческому противостолбнячному иммуноглобулину). ), дифтерия (в качестве дополнительной терапии к антитоксину и для профилактики носительства), рожистый эндокардит, фузоспирохетоз (тяжелые инфекции ротоглотки, нижних дыхательных путей и области половых органов), листериозные инфекции, менингит, эндокардит, пастереллезные инфекции, включая бактериемию. и менингит, лихорадка Хаверхилла ; лихорадка от укуса крыс и диссеминированные гонококковые инфекции , менингококковый менингит и/или септицемия, вызванная чувствительными к пенициллину микроорганизмами, и сифилис. [33]
Пенициллин V можно принимать внутрь, поскольку он относительно устойчив к желудочной кислоте. Дозы выше 500 мг не полностью эффективны из-за плохой абсорбции. Он используется при тех же бактериальных инфекциях, что и пенициллин G, и является наиболее широко используемой формой пенициллина. [34] Однако он не используется при таких заболеваниях, как эндокардит , когда требуется высокий уровень пенициллина в крови.
Поскольку устойчивость к пенициллину сейчас настолько распространена, другие антибиотики теперь являются предпочтительным выбором для лечения. Например, пенициллин раньше был препаратом первой линии при инфекциях, вызванных Neisseria gonorrhoeae и Neisseria meningitidis , но больше не рекомендуется для лечения этих инфекций. Устойчивость к пенициллину в настоящее время очень распространена у Staphylococcus aureus , а это означает, что пенициллин не следует использовать для лечения инфекций, вызванных инфекцией S. aureus , если не известно, что инфекционный штамм восприимчив.
Распространенные (≥ 1% людей) побочные реакции , связанные с применением пенициллинов, включают диарею , гиперчувствительность , тошноту , сыпь , нейротоксичность , крапивницу и суперинфекцию (включая кандидоз ). Нечастые побочные эффекты (0,1–1% людей) включают лихорадку , рвоту , эритему , дерматит , ангионевротический отек , судороги (особенно у людей с эпилепсией ) и псевдомембранозный колит . [35] Пенициллин также может вызывать сывороточную болезнь или реакцию, подобную сывороточной болезни, у некоторых людей. Сывороточная болезнь — это реакция гиперчувствительности III типа , которая возникает через одну-три недели после воздействия лекарств, включая пенициллин. Это не настоящая лекарственная аллергия, поскольку аллергия представляет собой реакцию гиперчувствительности I типа , но повторное воздействие возбудителя может привести к анафилактической реакции. [36] [37] Аллергия возникает у 1–10% людей и проявляется кожной сыпью после воздействия. IgE-опосредованная анафилаксия возникает примерно у 0,01% пациентов. [38] [35]
Боль и воспаление в месте инъекции также характерны для парентерально вводимых бензатинбензилпенициллина, бензилпенициллина и, в меньшей степени, прокаинбензилпенициллина. Это состояние известно как ливедоидный дерматит или синдром Николау. [39] [40]
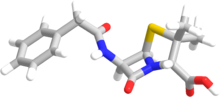
Термин « пенам » используется для описания общего ядра скелета пенициллинов. Это ядро имеет молекулярную формулу RC 9 H 11 N 2 O 4 S, где R — вариабельная боковая цепь, которая отличает пенициллины друг от друга. Ядро пенама имеет молярную массу 243 г/моль, при этом более крупные пенициллины имеют молярную массу около 450 - например, клоксациллин имеет молярную массу 436 г/моль. 6-АПК (C 8 H 12 N 2 O 3 S) образует основную структуру пенициллинов. Он состоит из закрытого дипептида, образующегося в результате конденсации L-цистеина и D-валина. Это приводит к образованию β-лактамных и тиазолидиновых колец. [41]
Ключевой структурной особенностью пенициллинов является четырехчленное β-лактамное кольцо; этот структурный фрагмент необходим для антибактериальной активности пенициллина. Кольцо β-лактама само по себе слито с пятичленным тиазолидиновым кольцом. Слияние этих двух колец приводит к тому, что β-лактамное кольцо становится более реакционноспособным, чем моноциклические β-лактамы, поскольку два слитых кольца искажают амидную связь β-лактама и, следовательно, устраняют резонансную стабилизацию, обычно присущую этим химическим связям. [42] Ацильная боковая цепь, присоединенная к β-лактамному кольцу. [43]
Различные β-лактамные антибиотики были получены после химической модификации структуры 6-АПК в ходе синтеза, в частности, путем химических замен в ацильной боковой цепи. Например, первый химически измененный пенициллин, метициллин, имел замены метоксигруппами в положениях 2' и 6' бензольного кольца 6-АРА пенициллина G. [41] Это отличие делает метициллин устойчивым к активности β-лактамаз , фермент, благодаря которому многие бактерии естественным образом невосприимчивы к пенициллинам. [44]
Пенициллин может легко проникать в бактериальные клетки грамположительных видов . Это связано с тем, что грамположительные бактерии не имеют внешней клеточной мембраны и просто заключены в толстую клеточную стенку . [45] Молекулы пенициллина достаточно малы, чтобы проходить через пространства гликопротеинов в клеточной стенке. По этой причине грамположительные бактерии очень чувствительны к пенициллину (о чем впервые свидетельствует открытие пенициллина в 1928 году [46] ). [47]
Пенициллин или любая другая молекула проникает в грамотрицательные бактерии другим путем. У бактерий более тонкие клеточные стенки, но внешняя поверхность покрыта дополнительной клеточной мембраной, называемой внешней мембраной. Наружная мембрана представляет собой липидный слой ( липополисахаридная цепь), который блокирует прохождение водорастворимых ( гидрофильных ) молекул, таких как пенициллин. Таким образом, он действует как первая линия защиты от любого токсичного вещества, что является причиной относительной устойчивости к антибиотикам по сравнению с грамположительными видами [48]. Но пенициллин все же может проникать в грамотрицательные виды путем диффузии через водные каналы, называемые поринами (внешние мембранные белки), которые рассеяны среди жировых молекул и могут транспортировать питательные вещества и антибиотики в бактерии. [49] Порины достаточно велики, чтобы обеспечить диффузию большинства пенициллинов, но скорость диффузии через них определяется конкретным размером молекул лекарства. Например, пенициллин G имеет большие размеры и медленно проникает через порины; в то время как более мелкие ампициллин и амоксициллин диффундируют гораздо быстрее. [50] Напротив, крупный ванкомицин не может проходить через порины и, следовательно, неэффективен для грамотрицательных бактерий. [51] Размер и количество поринов у разных бактерий различны. В результате действия двух факторов — размера пенициллина и порина — грамотрицательные бактерии могут быть невосприимчивы или иметь различную степень чувствительности к конкретному пенициллину. [52]


Пенициллин убивает бактерии, подавляя завершение синтеза пептидогликанов , структурного компонента бактериальной клеточной стенки . Он специфически ингибирует активность ферментов, которые необходимы для сшивания пептидогликанов на заключительном этапе биосинтеза клеточной стенки. Он делает это путем связывания пенициллинсвязывающих белков с β-лактамным кольцом — структурой, обнаруженной в молекулах пенициллина. [54] [55] Это приводит к ослаблению клеточной стенки из-за меньшего количества поперечных связей и означает, что вода неконтролируемо поступает в клетку, поскольку она не может поддерживать правильный осмотический градиент. Это приводит к лизису и гибели клеток.
Бактерии постоянно реконструируют свои пептидогликановые клеточные стенки, одновременно строя и разрушая части клеточной стенки по мере роста и деления. На последних стадиях биосинтеза пептидогликана образуется пентапептид уридиндифосфат -N -ацетилмурамовой кислоты (UDP-MurNAc), в котором четвертая и пятая аминокислоты представляют собой D -аланил- D -аланин. Перенос D-аланина осуществляется (катализируется) ферментом DD -транспептидазой ( к такому типу относятся пенициллин-связывающие белки ). [50] Структурная целостность бактериальной клеточной стенки зависит от перекрестного связывания UDP-MurNAc и N -ацетилглюкозамина. [56] Пенициллин и другие β-лактамные антибиотики действуют как аналог D -аланина- D -аланина (дипептида) в UDP-MurNAc из-за конформационного сходства. Затем DD-транспептидаза связывает четырехчленное β-лактамное кольцо пенициллина вместо UDP-MurNAc. [50] Как следствие, DD-транспептидаза инактивируется, образование поперечных связей между UDP-MurNAc и N -ацетилглюкозамином блокируется, в результате чего развивается дисбаланс между выработкой и деградацией клеточной стенки, что приводит к быстрой гибели клетки. [57]
Ферменты, которые гидролизуют поперечные связи пептидогликана, продолжают функционировать, даже если те, которые образуют такие поперечные связи, этого не делают. Это ослабляет клеточную стенку бактерии, и осмотическое давление становится все более некомпенсированным, что в конечном итоге приводит к гибели клеток ( цитолизу ). Кроме того, накопление предшественников пептидогликана запускает активацию гидролаз и аутолизинов бактериальной клеточной стенки, которые дополнительно переваривают пептидогликаны клеточной стенки. Небольшой размер пенициллинов увеличивает их эффективность, позволяя им проникать на всю глубину клеточной стенки. Это контрастирует с гликопептидными антибиотиками ванкомицином и тейкопланином , которые намного крупнее пенициллинов. [58]
Грамположительные бактерии называются протопластами , когда они теряют клеточные стенки. Грамотрицательные бактерии после обработки пенициллином не теряют полностью клеточных стенок и называются сферопластами . [53]
Пенициллин демонстрирует синергический эффект с аминогликозидами , поскольку ингибирование синтеза пептидогликанов позволяет аминогликозидам легче проникать через клеточную стенку бактерий, что позволяет им нарушать синтез бактериального белка внутри клетки. Это приводит к снижению MBC для восприимчивых организмов. [59]
Пенициллины, как и другие β -лактамные антибиотики, блокируют не только деление бактерий, в том числе цианобактерий , но и деление цианелл, фотосинтетических органелл глаукофитов , деление хлоропластов мохообразных . Напротив, они не оказывают влияния на пластиды высокоразвитых сосудистых растений . Это подтверждает эндосимбиотическую теорию эволюции пластидного деления у наземных растений. [60]
Некоторые бактерии вырабатывают ферменты, разрушающие β-лактамное кольцо, называемые β-лактамазами , которые делают бактерии устойчивыми к пенициллину. Поэтому некоторые пенициллины модифицируются или назначаются вместе с другими препаратами для использования против устойчивых к антибиотикам бактерий или у пациентов с ослабленным иммунитетом. Применение клавулановой кислоты или тазобактама, ингибиторов β-лактамаз, наряду с пенициллином придает пенициллину активность в отношении бактерий, продуцирующих β-лактамазу. Ингибиторы β-лактамаз необратимо связываются с β-лактамазой, предотвращая разрушение бета-лактамных колец на молекуле антибиотика. Альтернативно, флуклоксациллин представляет собой модифицированный пенициллин, который обладает активностью против бактерий, продуцирующих β-лактамазу, благодаря ацильной боковой цепи, которая защищает бета-лактамное кольцо от β-лактамазы. [38]
Пенициллин имеет низкое связывание с белками плазмы. Биодоступность пенициллина зависит от типа: пенициллин G имеет низкую биодоступность, менее 30%, тогда как пенициллин V имеет более высокую биодоступность, от 60 до 70% . [61]
Пенициллин имеет короткий период полураспада и выводится через почки. [61] Это означает, что его необходимо принимать не менее четырех раз в день, чтобы поддерживать адекватный уровень пенициллина в крови. Поэтому в ранних руководствах по использованию пенициллина рекомендовалось делать инъекции пенициллина каждые три часа, а дозировка пенициллина была описана как попытка наполнить ванну с вынутой пробкой. [8] В этом больше нет необходимости, поскольку гораздо большие дозы пенициллина дешевы и легко доступны; однако некоторые авторитеты рекомендуют по этой причине использовать постоянные инфузии пенициллина. [62]
Когда Александр Флеминг открыл сырой пенициллин в 1928 году, он сделал одно важное наблюдение: на многие бактерии пенициллин не влияет. [46] Это явление было обнаружено Эрнстом Чейном и Эдвардом Абрахамом при попытке точно определить пенициллин. В 1940 году они обнаружили, что невосприимчивые бактерии, такие как Escherichia coli, производят специфические ферменты, которые могут расщеплять молекулы пенициллина, делая их, таким образом, устойчивыми к антибиотику. Они назвали фермент пенициллиназой . [63] Пенициллиназа теперь классифицируется как член ферментов, называемых β-лактамазами. Эти β-лактамазы в природе присутствуют во многих других бактериях, и многие бактерии производят их при постоянном воздействии антибиотиков. У большинства бактерий устойчивость может осуществляться посредством трех различных механизмов: снижения проницаемости бактерий, снижения аффинности связывания пенициллин-связывающих белков (PBP) или разрушения антибиотика за счет экспрессии β-лактамазы. [64] Используя любой из них, бактерии обычно развивают устойчивость к различным антибиотикам - явление, называемое множественной лекарственной устойчивостью .
Реальный процесс механизма сопротивления может быть очень сложным. В случае пониженной проницаемости у бактерий механизмы различны у грамположительных и грамотрицательных бактерий. У грамположительных бактерий блокировка пенициллина обусловлена изменениями клеточной стенки. Например, устойчивость S. aureus к ванкомицину обусловлена дополнительным синтезом пептидогликана, который делает клеточную стенку намного толще, предотвращая эффективное проникновение пенициллина. [47] Устойчивость грамотрицательных бактерий обусловлена мутационными изменениями в структуре и количестве поринов. [52] У таких бактерий, как Pseudomonas aeruginosa , количество поринов уменьшено; тогда как у таких бактерий, как виды Enterobacter , Escherichia coli и Klebsiella pneumoniae , существуют модифицированные порины, такие как неспецифические порины (такие как группы OmpC и OmpF), которые не могут транспортировать пенициллин. [65]
Устойчивость, обусловленная изменениями PBP, весьма разнообразна. Распространенный случай встречается у Streptococcus pneumoniae , где имеется мутация в гене PBP, а мутантные PBP имеют пониженную аффинность связывания с пенициллинами. [66] У S. pneumoniae имеется шесть мутантных PBP , из которых PBP1a, PBP2b, PBP2x и иногда PBP2a ответственны за снижение аффинности связывания. [67] S. aureus может активировать скрытый ген, который продуцирует другой PBP, PBD2, который имеет низкую аффинность связывания с пенициллинами. [68] Существует другой штамм S. aureus , называемый метициллин-резистентным S. aureus (MRSA), который устойчив не только к пенициллину и другим β-лактамам, но и к большинству антибиотиков. Бактериальный штамм появился после введения метициллина в 1959 году. [44] У MRSA мутации в генах ( система mec ) PBP производят вариант белка, называемый PBP2a (также называемый PBP2'), [69] при создании четырех нормальных PBP. PBP2a имеет низкую аффинность связывания с пенициллином, а также не имеет активности гликозилтрансферазы, необходимой для полного синтеза пептидогликана (который осуществляется четырьмя нормальными PBP). [67] У Helicobacter cinaedi имеется множество мутаций в разных генах, которые создают варианты PBP. [70]
Ферментативное разрушение β-лактамазами является наиболее важным механизмом устойчивости к пенициллинам [71] и описывается как «самая большая угроза для использования [пенициллинов]». [72] Это был первый обнаруженный механизм устойчивости к пенициллину. В ходе экспериментов по очистке и проверке биологической активности пенициллина в 1940 году было обнаружено, что E. coli нечувствительна. [73] Причина была обнаружена в выработке фермента пенициллиназы (следовательно, первой известной β-лактамазы) в E. coli , который легко расщепляет пенициллин. [63] Существует более 2000 типов β-лактамаз, каждый из которых имеет уникальную аминокислотную последовательность и, следовательно, ферментативную активность. [72] Все они способны гидролизовать β-лактамные кольца, но их точные целевые сайты различны. [74] Они секретируются на поверхности бактерий в больших количествах у грамположительных бактерий, но в меньшем количестве у грамотрицательных видов. Следовательно, при смешанной бактериальной инфекции грамположительные бактерии могут защищать чувствительные к пенициллину грамотрицательные клетки. [50]
У P. aeruginosa существуют необычные механизмы , при которых может наблюдаться устойчивость, опосредованная биопленками, и образование персистерных клеток, устойчивых к множеству лекарств . [75]
.jpg/440px-Sample_of_penicillin_mould_presented_by_Alexander_Fleming_to_Douglas_Macleod,_1935_(9672239344).jpg)
Начиная с конца 19 века появились сообщения об антибактериальных свойствах плесени Penicillium , но ученые не смогли понять, какой процесс вызывает этот эффект. [76] Шотландский врач Александр Флеминг в больнице Святой Марии в Лондоне (ныне часть Имперского колледжа ) был первым, кто показал, что Penicillium Rubens обладает антибактериальными свойствами. [77] 3 сентября 1928 года он заметил, что грибковое заражение бактериальной культуры ( Staphylococcus aureus ), по-видимому, убивает бактерии. Он подтвердил это наблюдение новым экспериментом 28 сентября 1928 года. [78] Он опубликовал свой эксперимент в 1929 году и назвал антибактериальное вещество (экстракт гриба) пенициллином. [46]
К. Дж. Ла Туш идентифицировал гриб как Penicillium rubrum (позже Чарльз Том реклассифицировал его как P. notatum и P. chrysogenum , но позже исправил как P. Rubens ). [79] Флеминг выразил первоначальный оптимизм по поводу того, что пенициллин будет полезным антисептиком из-за его высокой эффективности и минимальной токсичности по сравнению с другими антисептиками того времени, и отметил его лабораторную ценность при выделении Bacillus influenzae (теперь называемого Haemophilus influenzae ). [80] [81]
Флеминг никого не убедил в важности своего открытия. [80] Во многом это произошло потому, что пенициллин было настолько трудно выделить, что его разработка в качестве лекарственного средства казалась невозможной. Предполагается, что если бы Флемингу удалось больше заинтересовать других ученых своей работой, пенициллин, возможно, был бы разработан несколькими годами раньше. [80]
Важность его работы была признана размещением 19 ноября 1999 года Международного исторического химического памятника в Лабораторном музее Александра Флеминга в Лондоне. [82]

В 1930 году Сесил Джордж Пейн, патолог Королевского лазарета в Шеффилде , 25 ноября 1930 года успешно вылечил офтальмию новорожденных , гонококковую инфекцию у младенцев, с помощью пенициллина (экстракт грибков ) .
В 1940 году австралийский учёный Говард Флори (позже барон Флори) и группа исследователей ( Эрнст Чейн , Эдвард Абрахам , Артур Дункан Гарднер , Норман Хитли , Маргарет Дженнингс , Джин Орр-Юинг и Артур Гордон Сандерс) в Школе сэра Уильяма Данна Патология Оксфордского университета добилась прогресса в создании концентрированного пенициллина из грибкового культурального бульона, который показал бактерицидное действие как in vitro , так и in vivo . [86] [87] В 1941 году они лечили полицейского Альберта Александра с тяжелой инфекцией лица; его состояние улучшилось, но затем закончились запасы пенициллина, и он умер. Впоследствии еще несколько пациентов прошли успешное лечение. [88] В декабре 1942 года выжившие после пожара в Кокоанат-Гроув в Бостоне были первыми ожоговыми пациентами, которых успешно вылечили пенициллином. [89]
Первое успешное использование чистого пенициллина произошло в 1942 году, когда Флеминг вылечил Гарри Ламберта от инфекции нервной системы (стрептококковый менингит ), которая в противном случае была бы смертельной. К тому времени оксфордская команда смогла произвести лишь небольшое количество. Флори охотно отдал Флемингу единственный доступный образец. У Ламберта началось улучшение уже на следующий день лечения, и он полностью вылечился в течение недели. [90] [91] Флеминг опубликовал свое клиническое исследование в журнале The Lancet в 1943 году. [7] После медицинского прорыва британский военный кабинет учредил 5 апреля 1943 года Комитет по пенициллину, что привело к проектам массового производства . [92] [93]
Когда медицинское применение было установлено, команда Оксфорда обнаружила, что невозможно производить пригодные для использования количества в их лаборатории. [88] Не сумев убедить британское правительство, Флори и Хитли в июне 1941 года отправились в США со своими образцами пресс-форм, чтобы заинтересовать правительство США крупномасштабным производством. [94] Они обратились в Северную региональную исследовательскую лабораторию Министерства сельского хозяйства США (NRRL, ныне Национальный центр исследований в области сельскохозяйственного использования ) в Пеории, штат Иллинойс, где были созданы мощности для крупномасштабной ферментации. [95] Немедленно последовала массовая культура плесени и поиск лучших форм. [94]
14 марта 1942 года первого пациента лечили от стрептококкового сепсиса пенициллином американского производства, произведенным компанией Merck & Co. [96] Половина общего количества препарата, произведенного в то время, была использована для лечения одной пациентки, Энн Миллер. [97] К июню 1942 года в США было достаточно пенициллина для лечения десяти пациентов. [98] В июле 1943 года Совет военного производства разработал план массового распределения запасов пенициллина среди войск союзников, сражающихся в Европе. [99] Результаты исследований ферментации кукурузного настоя в NRRL позволили Соединенным Штатам произвести 2,3 миллиона доз ко времени вторжения в Нормандию весной 1944 года. После всемирных поисков в 1943 году в Пеории была обнаружена заплесневелая дыня . Было обнаружено , что на рынке Иллинойса содержится лучший штамм плесени для производства с использованием процесса замачивания кукурузного ликера. [100] Ученый компании Pfizer Джаспер Х. Кейн предложил использовать метод глубокой ферментации для производства больших количеств пенициллина фармацевтического качества. [101] [26] : 109 Крупномасштабное производство стало результатом разработки инженером -химиком Маргарет Хатчинсон Руссо установки для глубокого брожения . [102] Как прямой результат войны и Управления военного производства, к июню 1945 года производилось более 646 миллиардов единиц в год. [99]
Дж. Рэймонд Реттью внес значительный вклад в военные усилия Америки, разработав методы производства пенициллина в коммерческих количествах, при этом он объединил свои знания о грибной икре с функцией сепаратора сливок Sharples. [103] К 1943 году лаборатория Реттью производила большую часть пенициллина в мире. Во время Второй мировой войны пенициллин существенно повлиял на количество смертей и ампутаций, вызванных инфицированными ранами среди союзных войск, спасая примерно 12–15% жизней. [104] Однако доступность была сильно ограничена из-за сложности производства больших количеств пенициллина и быстрого почечного клиренса препарата, что требовало частого приема. Методы массового производства пенициллина были запатентованы Эндрю Джексоном Мойером в 1945 году. [105] [106] [107] Флори не запатентовал пенициллин, поскольку сэр Генри Дейл посоветовал ему сделать это неэтично. [88]
Пенициллин активно выводится из организма, и около 80% дозы пенициллина выводится из организма в течение трех-четырех часов после приема. Действительно, в раннюю эпоху пенициллина этот препарат был настолько дефицитен и так высоко ценился, что стало обычным делом собирать мочу у пациентов, проходящих лечение, чтобы пенициллин в моче можно было изолировать и повторно использовать. [108] Это не было удовлетворительным решением, поэтому исследователи искали способ замедлить выведение пенициллина. Они надеялись найти молекулу, которая могла бы конкурировать с пенициллином за переносчик органической кислоты, ответственный за выведение, так, чтобы переносчик преимущественно выделял конкурирующую молекулу, а пенициллин сохранялся. Подходящим оказался урикозурический препарат пробенецид . При совместном применении пробенецида и пенициллина пробенецид конкурентно ингибирует выведение пенициллина, увеличивая концентрацию пенициллина и продлевая его активность. В конце концов, появление методов массового производства и полусинтетических пенициллинов решило проблемы с поставками, поэтому использование пробенецида сократилось. [108] Пробенецид по-прежнему полезен при некоторых инфекциях, требующих особенно высоких концентраций пенициллинов. [109]
После Второй мировой войны Австралия была первой страной, сделавшей этот препарат доступным для гражданского использования. В США пенициллин стал доступен широкой публике 15 марта 1945 года. [110]
Флеминг, Флори и Чейн разделили Нобелевскую премию по физиологии и медицине 1945 года за разработку пенициллина.
.jpg/440px-Molecular_model_of_Penicillin_by_Dorothy_Hodgkin_(9663803982).jpg)
Химическая структура пенициллина была впервые предложена Эдвардом Абрахамом в 1942 году [86] и позже подтверждена в 1945 году с помощью рентгеновской кристаллографии Дороти Кроуфут Ходжкин , которая также работала в Оксфорде. [111] Позже в 1964 году она получила Нобелевскую премию по химии за это и другие определения структуры.
Химик Джон К. Шиэн из Массачусетского технологического института (MIT) завершил первый химический синтез пенициллина в 1957 году. [112] [113] [114] Шиэн начал свои исследования синтеза пенициллина в 1948 году, и в ходе этих исследований разработал новые методы синтеза пептидов , а также новые защитные группы — группы, маскирующие реакционную способность определенных функциональных групп. [114] [115] Хотя первоначальный синтез, разработанный Шиэном, не подходил для массового производства пенициллинов, одним из промежуточных соединений в синтезе Шиэна была 6-аминопенициллановая кислота (6-АПК), ядро пенициллина. [112] [113] [114] [116]
6-APA был обнаружен исследователями из Beecham Research Laboratories (позже Beecham Group ) в Суррее в 1957 году (опубликовано в 1959 году). [117] Присоединение различных групп к «ядру» 6-АПА пенициллина позволило создать новые формы пенициллинов, которые более универсальны и обладают лучшей активностью. [118]
Узкий диапазон излечимых заболеваний или «спектр активности» пенициллинов, наряду с плохой активностью феноксиметилпенициллина, действующего при пероральном приеме, привели к поиску производных пенициллина, которые могли бы лечить более широкий спектр инфекций. Выделение 6-АРА, ядра пенициллина, позволило получить полусинтетические пенициллины с различными улучшениями по сравнению с бензилпенициллином (биодоступность, спектр, стабильность, переносимость).
Первой крупной разработкой стал ампициллин, появившийся в 1961 году. Он обладал более широким спектром действия, чем любой из оригинальных пенициллинов. Дальнейшая разработка привела к появлению пенициллинов, устойчивых к β-лактамазам, включая флуклоксациллин, диклоксациллин и метициллин. Они были значимы из-за своей активности против видов бактерий, продуцирующих β-лактамазу, но были неэффективны против метициллин-резистентных штаммов Staphylococcus aureus (MRSA), которые появились впоследствии. [119]
Еще одним развитием линии истинных пенициллинов стали антипсевдомонадные пенициллины, такие как карбенициллин, тикарциллин и пиперациллин, полезные благодаря своей активности против грамотрицательных бактерий. Однако полезность β-лактамного кольца была такова, что родственные антибиотики, включая мециллинамы, карбапенемы и, что наиболее важно, цефалоспорины, все еще сохраняют его в центре своей структуры. [120]

Пенициллин получают путем ферментации различных видов сахара грибом Penicillium Rubens . [121] В процессе ферментации образуется пенициллин в качестве вторичного метаболита , когда рост грибка подавляется стрессом. [121] Путь биосинтеза, описанный ниже, подвергается ингибированию по принципу обратной связи с участием побочного продукта l -лизина, ингибирующего фермент гомоцитратсинтазу . [122]
Клетки Penicillium выращивают с использованием метода, называемого периодической культурой с подпиткой, при котором клетки постоянно подвергаются стрессу, необходимому для индукции производства пенициллина. Хотя использование глюкозы в качестве источника углерода подавляет ферменты биосинтеза пенициллина, лактоза не оказывает никакого эффекта, а уровень щелочного pH подавляет эту регуляцию. Избыток фосфатов , доступного кислорода и использование аммония в качестве источника азота подавляют выработку пенициллина, в то время как метионин может действовать как единственный источник азота/серы со стимулирующим эффектом. [123]
Биотехнологический метод направленной эволюции был применен для получения путем мутации большого числа штаммов Penicillium . Эти методы включают подверженную ошибкам ПЦР , перетасовку ДНК , ITCHY и ПЦР с перекрытием цепей .
Полусинтетические пенициллины получают, начиная с ядра пенициллина 6-АРА.

В целом, существует три основных и важных этапа биосинтеза пенициллина G (бензилпенициллина).