Щелочные металлы состоят из химических элементов: литий (Li), натрий (Na), калий (K), [примечание 1] , рубидий (Rb), цезий (Cs), [примечание 2] и франций (Fr). Вместе с водородом они составляют группу 1 , [примечание 3] , лежащую в s-блоке таблицы Менделеева . У всех щелочных металлов самый внешний электрон находится на s-орбитали : эта общая электронная конфигурация приводит к тому, что они имеют очень схожие характеристические свойства. [примечание 4] Действительно, щелочные металлы представляют собой лучший пример групповых тенденций в свойствах в периодической таблице, при этом элементы демонстрируют хорошо охарактеризованное гомологическое поведение. [5] Это семейство элементов также известно как литиевое семейство по имени его ведущего элемента.
Все щелочные металлы являются блестящими, мягкими , высокореактивными металлами при стандартной температуре и давлении и легко теряют свой внешний электрон , образуя катионы с зарядом +1. Все их можно легко разрезать ножом из-за их мягкости, обнажая блестящую поверхность, которая быстро тускнеет на воздухе из-за окисления атмосферной влагой и кислородом (а в случае лития - азотом ). Из-за их высокой реакционной способности их необходимо хранить под маслом, чтобы предотвратить реакцию с воздухом, и в природе они встречаются только в солях и никогда в виде свободных элементов. Цезий, пятый щелочной металл, является наиболее реакционноспособным из всех металлов. Все щелочные металлы реагируют с водой, причем более тяжелые щелочные металлы реагируют более энергично, чем более легкие.
Все открытые щелочные металлы встречаются в природе в виде их соединений: по распространенности наиболее распространен натрий, за ним следуют калий, литий, рубидий, цезий и, наконец, франций, который из-за чрезвычайно высокой радиоактивности встречается очень редко ; Франций встречается в природе лишь в незначительных следах как промежуточный этап в некоторых неясных побочных ветвях цепочек естественного распада . Были проведены эксперименты с целью синтеза элемента 119 , который, вероятно, станет следующим членом группы; ни один из них не увенчался успехом. Однако унунений не может быть щелочным металлом из-за релятивистских эффектов , которые, по прогнозам, окажут большое влияние на химические свойства сверхтяжелых элементов ; даже если он действительно окажется щелочным металлом, по прогнозам, он будет иметь некоторые отличия по физическим и химическим свойствам от своих более легких гомологов.
Большинство щелочных металлов имеют множество различных применений. Одним из наиболее известных применений чистых элементов является использование рубидия и цезия в атомных часах , из которых цезиевые атомные часы составляют основу вторых. Распространенным применением соединений натрия являются натриевые лампы , которые очень эффективно излучают свет. Поваренная соль , или хлорид натрия, использовалась с древности. Литий находит применение в качестве психиатрического лекарства и в качестве анода в литиевых батареях . Натрий, калий и, возможно, литий являются важными элементами , играющими важную биологическую роль в качестве электролитов , и хотя другие щелочные металлы не являются незаменимыми, они также оказывают различное воздействие на организм, как полезное, так и вредное.

Соединения натрия известны с древних времен; соль ( хлорид натрия ) была важным товаром в человеческой деятельности, о чем свидетельствует английское слово « зарплата» , обозначающее «зарплату » — деньги, выплачиваемые римским солдатам за покупку соли. [6] [ нужен лучший источник ] Хотя поташ использовался с древних времен, на протяжении большей части его истории не считалось, что это вещество фундаментально отличается от минеральных солей натрия. Георг Эрнст Шталь получил экспериментальные данные, которые позволили ему предположить фундаментальное различие солей натрия и калия в 1702 году [7] , а Анри-Луи Дюамель дю Монсо смог доказать это различие в 1736 году. [8] Точный химический состав калия и соединения натрия, а также статус химических элементов калия и натрия тогда не был известен, и поэтому Антуан Лавуазье не включил ни одну щелочь в свой список химических элементов в 1789 году. [9] [10]
Чистый калий был впервые выделен в 1807 году в Англии Хамфри Дэви , который получил его из едкого поташа (KOH, гидроксид калия) путем электролиза расплавленной соли с помощью недавно изобретенной гальванической батареи . Предыдущие попытки электролиза водной соли не увенчались успехом из-за чрезвычайной реакционной способности калия. [11] : 68 Калий был первым металлом, который был выделен электролизом. [12] Позже в том же году Дэви сообщил об экстракции натрия из аналогичного вещества каустической соды (NaOH, щелок) с помощью аналогичной техники, продемонстрировав, что элементы и, следовательно, соли различны. [9] [10] [13] [14]

Петалит ( Li Al Si 4 O 10 ) был открыт в 1800 году бразильским химиком Хосе Бонифасио де Андрада в шахте на острове Уто, Швеция . [15] [16] [17] Однако только в 1817 году Йохан Август Арфведсон , работавший тогда в лаборатории химика Йонса Якоба Берцелиуса , обнаружил присутствие нового элемента при анализе петалитовой руды . [18] [19] Он отметил, что этот новый элемент образует соединения, подобные соединениям натрия и калия, хотя его карбонат и гидроксид были менее растворимы в воде и более щелочными , чем другие щелочные металлы. [20] Берцелиус дал неизвестному материалу название литион / литина , от греческого слова λιθoς (транслитерируемого как литос , что означает «камень»), чтобы отразить его открытие в твердом минерале, в отличие от калия, который был обнаружен в растениях. пепел и натрий, который был известен отчасти своим высоким содержанием в крови животных. Он назвал металл внутри материала литием . [21] [16] [19] Литий, натрий и калий были частью открытия периодичности , поскольку они входят в серию триад элементов одной группы , которые были отмечены Иоганном Вольфгангом Дёберейнером в 1850 году как имеющие схожие свойства. . [22]

Рубидий и цезий были первыми элементами, открытыми с помощью спектроскопа , изобретенного в 1859 году Робертом Бунзеном и Густавом Кирхгофом . [23] В следующем году они обнаружили цезий в минеральной воде из Бад-Дюркхайма , Германия. Открытие рубидия произошло в следующем году в Гейдельберге , Германия, в минерале лепидолите . [24] Названия рубидия и цезия происходят от наиболее заметных линий в их спектрах излучения : ярко-красной линии рубидия (от латинского слова Rubidus , что означает темно-красный или ярко-красный) и небесно-голубой линии цезия ( происходит от латинского слова caesius , что означает небесно-голубой). [25] [26]
Примерно в 1865 году Джон Ньюлендс опубликовал серию статей, в которых перечислил элементы в порядке увеличения атомного веса и аналогичных физических и химических свойств, которые повторялись с интервалом в восемь; он сравнил такую периодичность с октавами музыки, где ноты, отстоящие друг от друга на октаву, имеют схожие музыкальные функции. [27] [28] Его версия объединила все известные тогда щелочные металлы (от лития до цезия), а также медь, серебро и таллий (которые демонстрируют степень окисления +1, характерную для щелочных металлов) в одну группу. В его таблице водород помещался рядом с галогенами . [22]
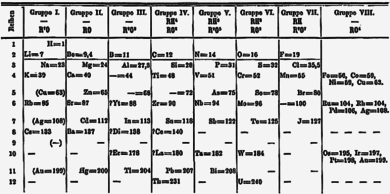
После 1869 года Дмитрий Менделеев предложил свою периодическую таблицу, поместив литий во главе группы с натрием, калием, рубидием, цезием и таллием. [29] Два года спустя Менделеев пересмотрел свою таблицу, поместив водород в группу 1 выше лития, а также переместив таллий в группу бора . В этой версии 1871 года медь, серебро и золото были помещены дважды: один раз как часть группы IB и один раз как часть «группы VIII», охватывающей сегодняшние группы с 8 по 11. [30] [примечание 5] После введения В таблице из 18 столбцов элементы группы IB были перемещены на их текущее положение в d-блоке , а щелочные металлы остались в группе IA . Позже, в 1988 году, название группы было изменено на группу 1. [4] Тривиальное название «щелочные металлы» происходит от того факта, что все гидроксиды элементов группы 1 являются сильными щелочами при растворении в воде. [5]
Было как минимум четыре ошибочных и неполных открытия [31] [32] [33] [34] до того, как Маргарита Перей из Института Кюри в Париже, Франция, открыла франций в 1939 году путем очистки образца актиния-227 , о котором, как сообщалось, имеют энергию распада 220 кэВ . Однако Перей заметил частицы распада с уровнем энергии ниже 80 кэВ. Перей предположил, что эта активность распада могла быть вызвана ранее неопознанным продуктом распада, который был выделен во время очистки, но снова появился из чистого актиния -227. Различные тесты исключили возможность того, что неизвестным элементом является торий , радий , свинец, висмут или таллий . Новый продукт проявлял химические свойства щелочного металла (например, соосаждение с солями цезия), что заставило Перея предположить, что это элемент 87, возникший в результате альфа- распада актиния-227. [35] Затем Перей попытался определить соотношение бета-распада и альфа-распада в актинии-227. Ее первый тест показал, что альфа-ветвление составило 0,6%, но позже она пересмотрела эту цифру до 1%. [36]
Следующим элементом после франция ( эка -франция) в периодической таблице будет унунений (Uue), элемент 119. [37] : 1729–1730 Синтез унунения был впервые предпринят в 1985 году путем бомбардировки мишени эйнштейния -254 кальцием . -48 ионов на ускорителе superHILAC в Национальной лаборатории Лоуренса Беркли в Беркли, Калифорния. Атомы не были идентифицированы, что привело к предельному выходу 300 нб . [38] [39]
Крайне маловероятно [38] , что эта реакция сможет создать какие-либо атомы унуненния в ближайшем будущем, учитывая чрезвычайно трудную задачу получения достаточных количеств эйнштейния-254, который предпочтителен для производства сверхтяжелых элементов из-за его большого размера. масса, относительно длительный период полураспада (270 дней) и наличие в значительных количествах в несколько микрограммов [40] позволяют сделать мишень достаточно крупной для повышения чувствительности эксперимента до необходимого уровня; Эйнштейний не обнаружен в природе и производится только в лабораториях и в количествах, меньших, чем те, которые необходимы для эффективного синтеза сверхтяжелых элементов. Однако, учитывая, что унунений является лишь первым элементом 8-го периода расширенной таблицы Менделеева , он вполне может быть открыт в ближайшем будущем посредством других реакций, и действительно, в настоящее время в Японии предпринимаются попытки его синтеза. [41] В настоящее время ни один из элементов периода 8 еще не обнаружен, и также возможно, что из-за капельной нестабильности физически возможны только элементы нижнего периода 8, примерно до элемента 128. [42] [43] Никаких попыток синтеза более тяжелых щелочных металлов не предпринималось: из-за их чрезвычайно высокого атомного номера для их производства потребуются новые, более мощные методы и технологии. [37] : 1737–1739 гг.

Правило Оддо-Харкинса гласит, что элементы с четными атомными номерами встречаются чаще, чем элементы с нечетными атомными номерами, за исключением водорода. Это правило утверждает, что элементы с нечетными атомными номерами имеют один неспаренный протон и с большей вероятностью захватят другой, тем самым увеличивая свой атомный номер. В элементах с четными атомными номерами протоны спарены, причем каждый член пары компенсирует спин другого, повышая стабильность. [45] [46] [47] Все щелочные металлы имеют нечетные атомные номера, и они не так распространены, как соседние с ними элементы с четными атомными номерами (благородные газы и щелочноземельные металлы ) в Солнечной системе. Более тяжелые щелочные металлы также менее распространены, чем более легкие, поскольку щелочные металлы, начиная с рубидия, могут быть синтезированы только в сверхновых , а не в ходе звездного нуклеосинтеза . Литий также гораздо менее распространен, чем натрий и калий, поскольку он плохо синтезируется как в ходе нуклеосинтеза Большого взрыва , так и в звездах: Большой взрыв мог произвести лишь следовые количества лития, бериллия и бора из-за отсутствия стабильного ядра с 5 или 8 атомами углерода. нуклонов , и звездный нуклеосинтез мог преодолеть это узкое место только с помощью процесса тройного альфа , соединяя три ядра гелия с образованием углерода и пропуская эти три элемента. [44]

Земля образовалась из того же облака материи, из которого образовалось Солнце, но в ходе формирования и эволюции Солнечной системы планеты приобрели разный состав . В свою очередь, естественная история Земли привела к тому, что некоторые части этой планеты имели разную концентрацию элементов. Масса Земли составляет примерно 5,98 × 1024 кг. Он состоит в основном из железа (32,1%), кислорода (30,1%), кремния (15,1%), магния (13,9%), серы (2,9%), никеля (1,8%), кальция (1,5%) и алюминия ( 1,4%); остальные 1,2% состоят из следовых количеств других элементов.что из-за планетарной дифференциации область ядра в основном состоит из железа (88,8%), с меньшим количеством никеля (5,8%), серы (4,5%) и менее 1% микроэлементов. [48]
Щелочные металлы из-за своей высокой реакционной способности не встречаются в природе в чистом виде. Они являются литофилами и поэтому остаются близко к поверхности Земли, поскольку легко соединяются с кислородом и, таким образом, прочно связываются с кремнеземом , образуя минералы относительно низкой плотности, которые не опускаются в ядро Земли. Калий, рубидий и цезий также являются несовместимыми элементами из-за большого ионного радиуса . [49]
Натрий и калий очень распространены на Земле, и оба входят в десятку наиболее распространенных элементов земной коры ; [50] [51] Натрий составляет примерно 2,6% земной коры по весу, что делает его шестым по распространенности элементом в целом [52] и самым распространенным щелочным металлом. Калий составляет примерно 1,5% земной коры и является седьмым по распространенности элементом. [52] Натрий содержится во многих различных минералах, из которых наиболее распространенной является обыкновенная соль (хлорид натрия), которая в огромных количествах растворяется в морской воде. Другие твердые месторождения включают галит , амфибол , криолит , нитратин и цеолит . [52] Многие из этих твердых отложений образуются в результате испарения древних морей, которое до сих пор происходит в таких местах, как Большое Соленое озеро штата Юта и Мертвое море . [11] : 69 Несмотря на почти одинаковое содержание натрия в земной коре, в океане натрий встречается гораздо чаще, чем калий, как потому, что больший размер калия делает его соли менее растворимыми, так и потому, что калий связывается с силикатами в почве и выщелачивает калий. усваивается растениями гораздо легче, чем натрий. [11] : 69
Несмотря на химическое сходство, литий обычно не встречается вместе с натрием или калием из-за его меньшего размера. [11] : 69 Из-за относительно низкой реакционной способности его можно обнаружить в морской воде в больших количествах; По оценкам, концентрация лития в морской воде составляет примерно от 0,14 до 0,25 частей на миллион (ppm) [53] [54] или 25 микромолярных частиц . [55] Его диагональное расположение с магнием часто позволяет ему заменять магний в ферромагниевых минералах, где его концентрация в коре составляет около 18 частей на миллион , что сопоставимо с концентрацией галлия и ниобия . В коммерческом отношении наиболее важным минералом лития является сподумен , который встречается в крупных месторождениях по всему миру. [11] : 69
Рубидий примерно так же распространен, как цинк , и более распространен, чем медь. В природе он встречается в минералах лейците , поллуците , карналлите , циннвальдите и лепидолите , [56] хотя ни один из них не содержит только рубидий и никаких других щелочных металлов. [11] : 70 Цезий более распространен, чем некоторые общеизвестные элементы, такие как сурьма , кадмий , олово и вольфрам , но гораздо менее распространен, чем рубидий. [57]
Франций-223 , единственный природный изотоп франция, [58] [59] является продуктом альфа -распада актиния-227 и может быть обнаружен в следовых количествах в урановых минералах. [60] По оценкам, в данном образце урана на каждые 10 18 атомов урана приходится только один атом франция . [61] [62] Было подсчитано, что в земной коре в любое время содержится не более 30 граммов франция из-за его чрезвычайно короткого периода полураспада, составляющего 22 минуты. [63] [64]
Физические и химические свойства щелочных металлов легко объяснить тем, что они имеют конфигурацию валентных электронов ns 1 , что приводит к слабой металлической связи . Следовательно, все щелочные металлы мягкие и имеют низкие плотности , [5] температуры плавления [5] и кипения , [5] , а также теплоту сублимации , испарения и диссоциации . [11] : 74 Все они кристаллизуются в объемно-центрированную кубическую кристаллическую структуру [11] : 73 и имеют характерные цвета пламени , поскольку их внешний s-электрон очень легко возбуждается. [11] : 75 Действительно, эти цвета для испытаний на пламя являются наиболее распространенным способом их идентификации, поскольку все их соли с общими ионами растворимы. [11] :75 Конфигурация ns 1 также приводит к тому, что щелочные металлы имеют очень большие атомные и ионные радиусы , а также очень высокую тепло- и электропроводность . [11] : 75 В их химическом составе преобладает потеря единственного валентного электрона на самой внешней s-орбитали с образованием степени окисления +1 из-за легкости ионизации этого электрона и очень высокой второй энергии ионизации. [11] : 76 Большая часть химии наблюдалась только у первых пяти членов группы. Химия франция недостаточно изучена из-за его чрезвычайной радиоактивности ; [5] поэтому изложение его свойств здесь ограничено. То немногое, что известно о франции, показывает, что, как и ожидалось, по поведению он очень близок к цезию. Физические свойства франция еще более схематичны, поскольку объемный элемент никогда не наблюдался; следовательно, любые данные, которые можно найти в литературе, безусловно, являются спекулятивными экстраполяциями. [65]
Щелочные металлы более похожи друг на друга, чем элементы любой другой группы . [5] Действительно, сходство настолько велико, что довольно трудно разделить калий, рубидий и цезий из-за их одинаковых ионных радиусов ; литий и натрий более различимы. Например, при движении вниз по таблице все известные щелочные металлы демонстрируют увеличение атомного радиуса , [72] уменьшение электроотрицательности , [72] увеличение реакционной способности , [5] и уменьшение температур плавления и кипения [72] , а также теплоты плавления и испарения. . [11] : 75 В целом их плотность увеличивается при движении вниз по таблице, за исключением того, что калий менее плотен, чем натрий. [72] Одним из очень немногих свойств щелочных металлов, которое не демонстрирует очень плавную тенденцию, является их потенциал восстановления : значение лития аномально и более отрицательно, чем у других. [11] : 75 Это связано с тем, что ион Li + имеет очень высокую энергию гидратации в газовой фазе: хотя ион лития значительно разрушает структуру воды, вызывая более высокое изменение энтропии, этой высокой энергии гидратации достаточно, чтобы Восстановительные потенциалы указывают на то, что это наиболее электроположительный щелочной металл, несмотря на трудность его ионизации в газовой фазе. [11] : 75
К стабильным щелочным металлам относятся все металлы серебристого цвета, за исключением цезия, имеющего бледно-золотистый оттенок: [73] это один из трех ясно окрашенных металлов (два других — медь и золото). [11] : 74 Кроме того, тяжелые щелочноземельные металлы кальций , стронций и барий , а также двухвалентные лантаноиды европий и иттербий имеют бледно-желтый цвет, хотя цвет гораздо менее заметен, чем у цезия. [11] : 74 Их блеск быстро тускнеет на воздухе из-за окисления. [5]
Все щелочные металлы обладают высокой реакционной способностью и никогда не встречаются в природе в элементарных формах. [21] По этой причине их обычно хранят в минеральном масле или керосине (парафиновом масле). [74] Они агрессивно реагируют с галогенами с образованием галогенидов щелочных металлов , которые представляют собой белые ионные кристаллические соединения, все растворимые в воде, за исключением фторида лития (LiF). [5] Щелочные металлы также реагируют с водой с образованием сильнощелочных гидроксидов , поэтому с ними следует обращаться с большой осторожностью. Тяжелые щелочные металлы реагируют более энергично, чем более легкие; например, при попадании в воду цезий вызывает больший взрыв, чем калий, если используется одинаковое количество молей каждого металла. [5] [75] [57] Щелочные металлы имеют самые низкие энергии первой ионизации в соответствующих периодах периодической таблицы [65] из-за их низкого эффективного ядерного заряда [5] и способности достигать конфигурации благородного газа за счет потери всего один электрон . [5] Щелочные металлы реагируют не только с водой, но и с донорами протонов, такими как спирты и фенолы , газообразный аммиак и алкины , причем последние демонстрируют феноменальную степень своей реакционной способности. Их огромная сила в качестве восстановителей делает их очень полезными для освобождения других металлов от их оксидов или галогенидов. [11] : 76
Вторая энергия ионизации всех щелочных металлов очень высока [5] [65] , поскольку она находится в полной оболочке, которая также находится ближе к ядру; [5] таким образом, они почти всегда теряют один электрон, образуя катионы. [11] : 28 Щелочи являются исключением: это нестабильные соединения, которые содержат щелочные металлы в степени окисления -1, что очень необычно , поскольку до открытия щелочей не предполагалось, что щелочные металлы способны образовывать анионы . Считалось, что они могут появляться в солях только в виде катионов. Щелочные анионы заполнили s-подоболочки , что придает им достаточную стабильность для существования. Известно, что все стабильные щелочные металлы, за исключением лития, способны образовывать щелочи, [76] [77] [78] , а щелочи представляют большой теоретический интерес из-за их необычной стехиометрии и низких потенциалов ионизации . Алкалиды химически подобны электридам , которые представляют собой соли с захваченными электронами , действующими как анионы. [79] Особенно ярким примером щелочи является «обратный гидрид натрия » , H + Na- (оба иона образуют комплексы ) , в отличие от обычного гидрида натрия, Na + H- : [80] он нестабилен изолированно, из-за его высокой энергии, возникающей в результате смещения двух электронов от водорода к натрию, хотя прогнозируется, что некоторые производные будут метастабильными или стабильными. [80] [81]
В водном растворе ионы щелочных металлов образуют акваионы формулы [M(H 2 O) n ] + , где n — число сольватации. Их координационные числа и форма хорошо согласуются с ожидаемыми, исходя из их ионных радиусов. Говорят, что в водном растворе молекулы воды, непосредственно связанные с ионом металла, принадлежат первой координационной сфере , также известной как первая или первичная сольватная оболочка. Связь между молекулой воды и ионом металла представляет собой дативную ковалентную связь , при которой атом кислорода отдает на связь оба электрона. Каждая координированная молекула воды может быть присоединена водородными связями к другим молекулам воды. Говорят, что последние находятся во второй координационной сфере. Однако для катионов щелочных металлов вторая координационная сфера не определена четко, поскольку заряд +1 на катионе недостаточно велик, чтобы поляризовать молекулы воды в первичной сольватной оболочке настолько, чтобы они могли образовывать прочные водородные связи с молекулами в первичной сольватной оболочке. вторая координационная сфера, создающая более стабильную сущность. [82] [83] : 25 Число сольватации Li + было экспериментально установлено равным 4, образуя тетраэдр [Li(H 2 O) 4 ] + : в то время как числа сольватации от 3 до 6 были обнаружены для акваионов лития. числа сольватации менее 4 могут быть результатом образования контактных ионных пар , а более высокие числа сольватации можно интерпретировать как молекулы воды, приближающиеся к [Li(H 2 O) 4 ] + через грань тетраэдра, хотя молекулярно-динамическое моделирование может указывать на существование октаэдрического гексааква-иона. В первичной сольватной сфере иона натрия, вероятно, также находится шесть молекул воды, образующих октаэдрический ион [Na(H 2 O) 6 ] + . [66] [83] : 126–127 Хотя ранее считалось, что более тяжелые щелочные металлы также образуют октаэдрические гексааква-ионы, с тех пор было обнаружено, что калий и рубидий, вероятно, образуют [K(H 2 O) 8 ] + и [ Ионы Rb(H 2 O) 8 ] + , имеющие квадратную антипризматическую структуру, и что цезий образует 12-координатный ион [Cs(H 2 O) 12 ] + . [84]
Химия лития демонстрирует несколько отличий от химии остальной части группы, поскольку небольшой катион Li + поляризует анионы и придает его соединениям более ковалентный характер. [5] Литий и магний имеют диагональное соотношение из-за схожего атомного радиуса, [5] так что они демонстрируют некоторое сходство. Например, литий образует стабильный нитрид — свойство, общее для всех щелочноземельных металлов (группы магния), но уникальное для щелочных металлов. [85] Кроме того, среди соответствующих групп только литий и магний образуют металлоорганические соединения со значительным ковалентным характером (например, Li Me и MgMe 2 ). [86]
Фторид лития — единственный галогенид щелочного металла, плохо растворимый в воде [5] , а гидроксид лития — единственный гидроксид щелочного металла, который не расплывается . [5] И наоборот, перхлорат лития и другие соли лития с крупными анионами, которые не могут быть поляризованы, гораздо более стабильны, чем аналогичные соединения других щелочных металлов, вероятно, потому, что Li + имеет высокую энергию сольватации. [11] : 76 Этот эффект также означает, что большинство простых солей лития обычно встречаются в гидратированной форме, поскольку безводные формы чрезвычайно гигроскопичны : это позволяет использовать такие соли, как хлорид лития и бромид лития , в осушителях и кондиционерах воздуха . [11] : 76
Также прогнозируется, что франций будет демонстрировать некоторые различия из-за своего большого атомного веса , заставляющего его электроны двигаться со скоростью, значительной долей скорости света, и, таким образом, делая релятивистские эффекты более заметными. В отличие от тенденции к уменьшению электроотрицательности и энергии ионизации щелочных металлов, электроотрицательность и энергия ионизации франция, по прогнозам, будут выше, чем у цезия, из-за релятивистской стабилизации 7s-электронов; кроме того, ожидается, что его атомный радиус будет аномально низким. Таким образом, вопреки ожиданиям, наиболее реакционноспособным из щелочных металлов является цезий, а не франций. [68] [37] : 1729 [87] Все известные физические свойства франция также отклоняются от четких тенденций, идущих от лития к цезию, такие как первая энергия ионизации, сродство к электрону и поляризуемость анионов, хотя и из-за недостаточности известных данные о франции, многие источники дают экстраполированные значения, игнорируя тот факт, что релятивистские эффекты делают тенденцию от лития к цезию неприменимой к францию. [87] Некоторые из немногих свойств франция, которые были предсказаны с учетом теории относительности, - это сродство к электрону (47,2 кДж/моль) [88] и энтальпия диссоциации молекулы Fr 2 (42,1 кДж/моль). [89] Молекула CsFr поляризована как Cs + Fr - , показывая, что подоболочка 7s франция гораздо сильнее подвержена релятивистским эффектам, чем подоболочка 6s цезия. [87] Кроме того, ожидается, что супероксид франция (FrO 2 ) будет иметь значительный ковалентный характер, в отличие от других супероксидов щелочных металлов, из-за вклада связывания со стороны 6p-электронов франция. [87]
Все щелочные металлы имеют нечетные атомные номера; следовательно, их изотопы должны быть либо нечетно-нечетными (числа протонов и нейтронов нечетные), либо нечетно-четными ( число протонов нечетное, а число нейтронов четное). Нечетно-нечетные ядра имеют четные массовые числа , тогда как нечетно-четные ядра имеют нечетные массовые числа. Первичные нечетно-нечетные нуклиды редки, потому что большинство нечетно-нечетных ядер очень нестабильны по отношению к бета-распаду , поскольку продукты распада четно-четные и, следовательно, более прочно связаны из-за эффектов спаривания ядер . [90]
Из-за большой редкости нечетно-нечетных ядер почти все первичные изотопы щелочных металлов являются нечетно-четными (исключение составляют легкий стабильный изотоп литий-6 и долгоживущий радиоизотоп калий-40). Для данного нечетного массового числа может быть только один бета-стабильный нуклид , поскольку нет разницы в энергии связи между четно-нечетным и нечетно-четным, сравнимой с разницей между четно-четным и нечетно-нечетным, в результате чего другие нуклиды того же массового числа ( изобары ), способные к бета-распаду в сторону нуклида с наименьшей массой. Эффект нестабильности нечетного числа нуклонов любого типа заключается в том, что элементы с нечетными номерами, такие как щелочные металлы, имеют тенденцию иметь меньше стабильных изотопов, чем элементы с четными номерами. Из 26 моноизотопных элементов , имеющих только один стабильный изотоп, все, кроме одного, имеют нечетный атомный номер, а все, кроме одного, также имеют четное количество нейтронов. Бериллий является единственным исключением из обоих правил из-за его низкого атомного номера. [90]
Все щелочные металлы, за исключением лития и цезия, имеют по крайней мере один встречающийся в природе радиоизотоп : натрий-22 и натрий-24 представляют собой следовые радиоизотопы, образующиеся космогенно , [91] калий-40 и рубидий-87 имеют очень длительный период полураспада и, таким образом, встречаются в природе. , [92] и все изотопы франция радиоактивны . [92] В начале 20 века цезий также считался радиоактивным, [93] [94] , хотя он не имеет встречающихся в природе радиоизотопов. [92] (Франций в то время еще не был открыт.) Природный долгоживущий радиоизотоп калия, калий-40, составляет около 0,012% природного калия, [95] и, таким образом, природный калий слабо радиоактивен. Эта естественная радиоактивность стала основой для ошибочного заявления об открытии элемента 87 (следующего щелочного металла после цезия) в 1925 году. [31] [32] Природный рубидий также слабо радиоактивен: 27,83% приходится на долгоживущий радиоизотоп рубидий. -87. [11] : 74
Цезий-137 с периодом полураспада 30,17 лет является одним из двух основных среднеживущих продуктов деления , наряду со стронцием-90 , который отвечает за большую часть радиоактивности отработанного ядерного топлива после нескольких лет охлаждения. до нескольких сотен лет после использования. Он составляет большую часть радиоактивности, оставшейся после чернобыльской аварии . Цезий-137 подвергается высокоэнергетическому бета-распаду и в конечном итоге становится стабильным барием-137 . Это сильный излучатель гамма-излучения. Цезий-137 имеет очень низкую скорость захвата нейтронов, и от него невозможно избавиться таким способом, но ему необходимо дать возможность распасться. [96] Цезий-137 использовался в качестве индикатора в гидрологических исследованиях, аналогично использованию трития . [97] Небольшие количества цезия-134 и цезия-137 попали в окружающую среду почти во время всех испытаний ядерного оружия и некоторых ядерных аварий , в первую очередь аварии в Гойании и чернобыльской катастрофы . По состоянию на 2005 год цезий-137 является основным источником радиации в зоне отчуждения вокруг Чернобыльской АЭС . [98] Его химические свойства как одного из щелочных металлов делают его одним из наиболее проблематичных продуктов деления с коротким и средним сроком жизни, поскольку он легко перемещается и распространяется в природе из-за высокой растворимости его солей в воде и является усваивается организмом, который ошибочно принимает его за свои незаменимые родственные вещества — натрий и калий. [99] : 114
Щелочные металлы более похожи друг на друга, чем элементы любой другой группы . [5] Например, при движении вниз по таблице все известные щелочные металлы демонстрируют увеличение атомного радиуса , [72] уменьшение электроотрицательности , [72] увеличение реакционной способности , [5] и уменьшение температур плавления и кипения [72], а также теплоты плавление и испарение. [11] : 75 В целом их плотность увеличивается при движении вниз по таблице, за исключением того, что калий менее плотен, чем натрий. [72]

Атомные радиусы щелочных металлов увеличиваются по мере спуска по группе. [72] Из-за эффекта экранирования , когда атом имеет более одной электронной оболочки , каждый электрон испытывает электрическое отталкивание от других электронов, а также электрическое притяжение от ядра. [100] В щелочных металлах внешний электрон ощущает только суммарный заряд +1, поскольку некоторая часть заряда ядра (которая равна атомному номеру ) компенсируется внутренними электронами; число внутренних электронов щелочного металла всегда на один меньше заряда ядра. Следовательно, единственным фактором, влияющим на атомный радиус щелочных металлов, является количество электронных оболочек. Поскольку это число увеличивается вниз по группе, атомный радиус также должен увеличиваться вниз по группе. [72]
Ионные радиусы щелочных металлов значительно меньше их атомных радиусов. Это связано с тем, что самый внешний электрон щелочных металлов находится в другой электронной оболочке , чем внутренние электроны, и, таким образом, когда он удаляется, образующийся атом имеет на одну электронную оболочку меньше и становится меньше. Кроме того, эффективный заряд ядра увеличился, и, таким образом, электроны сильнее притягиваются к ядру, а ионный радиус уменьшается. [5]

Первая энергия ионизации элемента или молекулы — это энергия, необходимая для перемещения наиболее свободно удерживаемого электрона из одного моля газообразных атомов элемента или молекул с образованием одного моля газообразных ионов с электрическим зарядом +1. Факторами, влияющими на первую энергию ионизации, являются заряд ядра , степень экранирования внутренними электронами и расстояние от наиболее слабо удерживаемого электрона от ядра, которым всегда является внешний электрон в элементах основной группы . Первые два фактора изменяют эффективный заряд ядра, который ощущает наиболее слабо удерживаемый электрон. Поскольку самый внешний электрон щелочных металлов всегда испытывает один и тот же эффективный заряд ядра (+1), единственным фактором, влияющим на первую энергию ионизации, является расстояние от самого внешнего электрона до ядра. Поскольку это расстояние увеличивается вниз по группе, самый удаленный электрон ощущает меньшее притяжение со стороны ядра, и, таким образом, первая энергия ионизации уменьшается. [72] Эта тенденция нарушается во франции из-за релятивистской стабилизации и сжатия 7s-орбитали, в результате чего валентный электрон франция оказывается ближе к ядру, чем можно было бы ожидать из нерелятивистских расчетов. Это заставляет самый внешний электрон франция чувствовать большее притяжение со стороны ядра, увеличивая его первую энергию ионизации, немного превышающую энергию цезия. [37] : 1729
Вторая энергия ионизации щелочных металлов намного выше, чем первая, поскольку второй наиболее свободно удерживаемый электрон является частью полностью заполненной электронной оболочки , и поэтому его трудно удалить. [5]
Реакционная способность щелочных металлов возрастает при движении вниз по группе. Это результат сочетания двух факторов: энергий первой ионизации и энергий атомизации щелочных металлов. Поскольку первая энергия ионизации щелочных металлов уменьшается вниз по группе, самому внешнему электрону легче удалиться от атома и участвовать в химических реакциях , тем самым увеличивая реакционную способность вниз по группе. Энергия атомизации измеряет прочность металлической связи элемента, которая падает вниз по группе по мере увеличения радиуса атомов , и, таким образом, металлическая связь должна увеличиваться в длине, отдаляя делокализованные электроны от притяжения ядер более тяжелых элементов. щелочные металлы. Сложение энергий атомизации и первой ионизации дает величину, тесно связанную (но не равную) с энергией активации реакции щелочного металла с другим веществом. Эта величина уменьшается по мере спуска по группе, как и энергия активации; таким образом, химические реакции могут протекать быстрее, а реакционная способность увеличивается по группе. [101]

Электроотрицательность — это химическое свойство , которое описывает тенденцию атома или функциональной группы притягивать к себе электроны (или электронную плотность ). [102] Если бы связь между натрием и хлором в хлориде натрия была ковалентной , пара общих электронов притягивалась бы к хлору, поскольку эффективный заряд ядра на внешних электронах составляет +7 в хлоре, но только +1 в натрии. Электронная пара притягивается настолько близко к атому хлора, что практически переносится на атом хлора ( ионная связь ). Однако, если атом натрия был заменен атомом лития, электроны не будут притягиваться так близко к атому хлора, как раньше, потому что атом лития меньше, что приводит к более сильному притяжению электронной пары к более близкому эффективному ядерному заряду лития. Следовательно, более крупные атомы щелочного металла (ниже по группе) будут менее электроотрицательными, поскольку связывающая пара менее сильно притягивается к ним. Как упоминалось ранее, ожидается, что франций станет исключением. [72]
Из-за более высокой электроотрицательности лития некоторые его соединения имеют более ковалентный характер. Например, йодид лития (LiI) растворяется в органических растворителях , что является свойством большинства ковалентных соединений. [72] Фторид лития (LiF) — единственный галогенид щелочного металла , не растворяющийся в воде, [5] а гидроксид лития (LiOH) — единственный гидроксид щелочного металла , который не расплывается . [5]
Точка плавления вещества — это точка, в которой оно меняет состояние из твердого состояния в жидкое, а точка кипения вещества (в жидком состоянии) — это точка, в которой давление паров жидкости равняется давлению окружающей среды, окружающей жидкость [103] [103] [ 103] [103] [103] [103] 104] и вся жидкость переходит в газообразное состояние. Когда металл нагревается до точки плавления, металлические связи , удерживающие атомы на месте, ослабевают, и атомы могут перемещаться, и металлические связи в конечном итоге полностью разрываются при температуре кипения металла. [72] [105] Таким образом, падение температуры плавления и кипения щелочных металлов указывает на то, что прочность металлических связей щелочных металлов снижается вниз по группе. [72] Это происходит потому, что атомы металла удерживаются вместе электромагнитным притяжением положительных ионов к делокализованным электронам. [72] [105] По мере того, как атомы увеличиваются в размерах, спускаясь вниз по группе (поскольку их атомный радиус увеличивается), ядра ионов отодвигаются дальше от делокализованных электронов и, следовательно, металлическая связь становится слабее, так что металлу легче плавить и кипятить, тем самым снижая температуры плавления и кипения. [72] Увеличение ядерного заряда не является значимым фактором из-за экранирующего эффекта. [72]
Все щелочные металлы имеют одинаковую кристаллическую структуру ( объемно-центрированную кубическую ) [11] , и поэтому единственными значимыми факторами являются количество атомов, которые могут поместиться в определенный объем, и масса одного из атомов, поскольку плотность определяется как масса единицы объема. Первый фактор зависит от объема атома и, следовательно, от атомного радиуса, который увеличивается при движении вниз по группе; таким образом, объем атома щелочного металла увеличивается при движении вниз по группе. Масса атома щелочного металла также увеличивается при движении вниз по группе. Таким образом, динамика плотностей щелочных металлов зависит от их атомных масс и атомных радиусов; если известны значения этих двух факторов, можно вычислить соотношения между плотностями щелочных металлов. В результате наблюдается тенденция к увеличению плотности щелочных металлов вниз по таблице, за исключением калия. Из-за наименьшего атомного веса и наибольшего атомного радиуса среди всех элементов в их периодах щелочные металлы являются наименее плотными металлами в таблице Менделеева. [72] Литий, натрий и калий — единственные три металла в периодической таблице, которые менее плотны, чем вода: [5] фактически, литий является наименее плотным известным твердым веществом при комнатной температуре . [11] : 75
Щелочные металлы образуют полный ряд соединений со всеми обычно встречающимися анионами, что хорошо иллюстрирует групповые закономерности. Эти соединения можно охарактеризовать как содержащие щелочные металлы, отдающие электроны акцепторам и образующие моноположительные ионы. [11] : 79 Это описание наиболее точно для галогенидов щелочных металлов и становится все менее и менее точным по мере увеличения катионного и анионного заряда, а также по мере того, как анион становится больше и более поляризуемым. Например, ионная связь сменяется металлической связью по ряду NaCl, Na 2 O, Na 2 S, Na 3 P, Na 3 As, Na 3 Sb, Na 3 Bi, Na. [11] : 81

Все щелочные металлы бурно или взрывоопасно реагируют с холодной водой, образуя водный раствор сильноосновного гидроксида щелочного металла и выделяя газообразный водород. [101] Эта реакция становится более энергичной при движении вниз по группе: литий устойчиво реагирует с шипением , но натрий и калий могут воспламениться, а рубидий и цезий погружаются в воду и выделяют газообразный водород так быстро, что в воде образуются ударные волны, которые могут разбить стекло. контейнеры. [5] Когда щелочной металл падает в воду, происходит взрыв, который состоит из двух отдельных стадий. Металл сначала реагирует с водой, разрывая водородные связи в воде и выделяя газообразный водород; это происходит быстрее для более реакционноспособных тяжелых щелочных металлов. Во-вторых, тепло, выделяемое в первой части реакции, часто воспламеняет газообразный водород, вызывая его взрывное сгорание в окружающем воздухе. Этот вторичный взрыв газообразного водорода вызывает видимое пламя над чашей с водой, озером или другим водоемом, а не начальную реакцию металла с водой (которая обычно происходит в основном под водой). [75] Гидроксиды щелочных металлов являются наиболее основными известными гидроксидами. [11] : 87
Недавние исследования показали, что взрывное поведение щелочных металлов в воде обусловлено кулоновским взрывом , а не только быстрым выделением самого водорода. [106] Все щелочные металлы плавятся в результате реакции с водой. Молекулы воды ионизируют оголенную металлическую поверхность жидкого металла, оставляя положительно заряженную поверхность металла и отрицательно заряженные ионы воды. Притяжение между заряженным металлом и ионами воды быстро увеличит площадь поверхности, вызывая экспоненциальное увеличение ионизации. Когда силы отталкивания внутри поверхности жидкого металла превышают силы поверхностного натяжения, он энергично взрывается. [106]
Сами гидроксиды представляют собой наиболее основные известные гидроксиды, реагирующие с кислотами с образованием солей и со спиртами с образованием олигомерных алкоксидов . Они легко реагируют с диоксидом углерода с образованием карбонатов или бикарбонатов или с сероводородом с образованием сульфидов или бисульфидов и могут использоваться для отделения тиолов от нефти. Они реагируют с амфотерными оксидами: например, оксиды алюминия , цинка , олова , свинца реагируют с гидроксидами щелочных металлов с образованием алюминатов, цинкатов, станнатов и плюмбатов. Диоксид кремния является кислым, поэтому гидроксиды щелочных металлов также могут разрушать силикатное стекло . [11] : 87

Щелочные металлы образуют множество интерметаллических соединений друг с другом и с элементами групп 2–13 периодической таблицы различной стехиометрии, [11] : 81 , например, амальгамы натрия с ртутью , в том числе Na 5 Hg 8 и Na 3 Hg. [107] Некоторые из них имеют ионные характеристики: взяв в качестве примера сплавы с золотом, наиболее электроотрицательным из металлов, NaAu и KAu являются металлическими, а RbAu и CsAu — полупроводниками. [11] : 81 NaK представляет собой сплав натрия и калия, который очень полезен, поскольку он является жидким при комнатной температуре, хотя необходимо принимать меры предосторожности из-за его чрезвычайной реакционной способности по отношению к воде и воздуху. Эвтектическая смесь плавится при температуре -12,6 °С. [108] Сплав, содержащий 41% цезия, 47% натрия и 12% калия, имеет самую низкую известную температуру плавления среди всех металлов или сплавов -78 °C. [23]
Интерметаллические соединения щелочных металлов с более тяжелыми элементами 13-й группы (алюминий, галлий , индий и таллий ), такие как NaTl, являются плохими проводниками или полупроводниками , в отличие от обычных сплавов с предыдущими элементами, что означает, что используемый щелочной металл имеет потерял электрон из-за вовлеченных анионов Цинтла . [109] Тем не менее, в то время как элементы в группе 14 и за ее пределами имеют тенденцию образовывать дискретные анионные кластеры, элементы группы 13 имеют тенденцию образовывать полимерные ионы с катионами щелочных металлов, расположенными между гигантской ионной решеткой. Например, NaTl состоит из полимерного аниона (—Tl − —) n с ковалентной алмазной кубической структурой с ионами Na + , расположенными между анионной решеткой. Более крупные щелочные металлы не могут аналогичным образом вписаться в анионную решетку и имеют тенденцию заставлять более тяжелые элементы 13 группы образовывать анионные кластеры. [110]
Бор представляет собой особый случай, поскольку он является единственным неметаллом в группе 13. Бориды щелочных металлов имеют тенденцию быть богатыми бором, включая заметные связи бор-бор с участием дельтаэдрических структур, [11] : 147–8 , и термически нестабильны из-за щелочи. металлы, имеющие очень высокое давление паров при повышенных температурах. Это делает прямой синтез проблематичным, поскольку щелочные металлы не реагируют с бором при температуре ниже 700 ° C, и поэтому это должно осуществляться в герметичных контейнерах с избытком щелочного металла. Кроме того, исключительно в этой группе, реакционная способность с бором снижается вниз по группе: литий реагирует полностью при 700 °С, но натрий при 900 °С, а калий - не до 1200 °С, причем реакция для лития протекает мгновенно, а для калия занимает несколько часов. Бориды рубидия и цезия даже не охарактеризованы. Известны различные фазы, такие как LiB 10 , NaB 6 , NaB 15 и KB 6 . [111] [112] Под высоким давлением связь бор-бор в боридах лития меняется от следования правилам Уэйда к образованию анионов Цинтла, как и остальная часть группы 13. [113]
Литий и натрий реагируют с углеродом с образованием ацетилидов Li 2 C 2 и Na 2 C 2 , которые также можно получить реакцией металла с ацетиленом . Калий, рубидий и цезий реагируют с графитом ; их атомы интеркалируются между гексагональными слоями графита, образуя интеркаляционные соединения графита формул MC 60 (темно-серый, почти черный), MC 48 (темно-серый, почти черный), MC 36 (синий), MC 24 (стальной синий) и MC 8 (бронза) (M = K, Rb или Cs). Эти соединения более чем в 200 раз более электропроводны, чем чистый графит, что позволяет предположить, что валентный электрон щелочного металла переносится в слои графита (например, M + C−8). [66] При нагревании KC 8 удаление атомов калия приводит к последовательному преобразованию в KC 24 , KC 36 , KC 48 и наконец KC 60 . KC 8 является очень сильным восстановителем , пирофорен и взрывается при контакте с водой. [114] [115] В то время как более крупные щелочные металлы (K, Rb и Cs) первоначально образуют MC 8 , более мелкие первоначально образуют MC 6 , и действительно, для их образования требуется реакция металлов с графитом при высоких температурах около 500 °C. форма. [116] Помимо этого, щелочные металлы являются настолько сильными восстановителями, что могут даже восстанавливать бакминстерфуллерен с образованием твердых фуллеридов M n C 60 ; натрий, калий, рубидий и цезий могут образовывать фуллериды, где n = 2, 3, 4 или 6, а рубидий и цезий дополнительно могут достигать n = 1. [11] : 285
При реакции щелочных металлов с более тяжелыми элементами углеродной группы ( кремнием , германием , оловом , свинцом) образуются ионные вещества с клеточной структурой, например силициды M 4 Si 4 ( M = K, Rb или Cs), который содержит М + и тетраэдрический Si4-4ионы. [66] Химия германидов щелочных металлов , включающая германид-ион Ge 4- и другие кластерные ионы ( Zintl ), такие как Ge.2-4, Ге4-9, Ге2-9, и [(Ge 9 ) 2 ] 6− , во многом аналогична реакции соответствующих силицидов. [11] : 393 Станниды щелочных металлов в основном ионные, иногда с ионом станнида ( Sn 4- ), [110] и иногда с более сложными ионами Цинтла, такими как Sn4-9, который появляется в нонастанниде тетракалия (K 4 Sn 9 ). [117] Одноатомный ион плюмбида ( Pb 4- ) неизвестен, и, по прогнозам, его образование будет энергетически невыгодным; Плюмбиды щелочных металлов содержат сложные ионы Цинтла, такие как Pb4-9. Эти германиды, станниды и плюмбиды щелочных металлов могут быть получены восстановлением германия, олова и свинца металлическим натрием в жидком аммиаке. [11] : 394

Литий, самый легкий из щелочных металлов, — единственный щелочной металл, который реагирует с азотом при стандартных условиях , а его нитрид — единственный стабильный нитрид щелочного металла. Азот — инертный газ, поскольку разрыв прочной тройной связи в молекуле динитрога (N 2 ) требует больших затрат энергии. На образование нитрида щелочного металла потребовалась бы энергия ионизации щелочного металла (с образованием ионов М + ), энергия, необходимая для разрыва тройной связи в N 2 и образования ионов N 3- , а также вся энергия, выделяющаяся из образование нитрида щелочного металла происходит за счет энергии решетки нитрида щелочного металла. Энергия решетки максимизируется при использовании небольших, сильно заряженных ионов; Щелочные металлы не образуют сильно заряженные ионы, а образуют только ионы с зарядом +1, поэтому только литий, самый маленький щелочной металл, может высвободить достаточно энергии решетки, чтобы сделать реакцию с азотом экзотермической , образуя нитрид лития . Реакции других щелочных металлов с азотом не выделяют достаточно энергии решетки и, таким образом, будут эндотермическими , поэтому они не образуют нитриды при стандартных условиях. [85] Нитрид натрия (Na 3 N) и нитрид калия (K 3 N), хотя и существуют, крайне нестабильны, склонны обратно разлагаться на составляющие их элементы и не могут быть получены путем взаимодействия элементов друг с другом при стандартных условиях. . [119] [120] Стерические препятствия запрещают существование нитрида рубидия или цезия. [11] : 417 Однако натрий и калий образуют бесцветные азидные соли с участием линейного N−3анион; из-за большого размера катионов щелочных металлов они достаточно термически стабильны, чтобы плавиться перед разложением. [11] : 417
Все щелочные металлы легко реагируют с фосфором и мышьяком с образованием фосфидов и арсенидов с формулой M 3 Pn (где M представляет собой щелочной металл, а Pn представляет собой пниктоген — фосфор, мышьяк, сурьму или висмут ). Это происходит из-за большего размера ионов P 3- и As 3- , поэтому для образования солей необходимо высвободить меньше энергии решетки. [66] Это не единственные фосфиды и арсениды щелочных металлов: например, калий имеет девять различных известных фосфидов с формулами K 3 P, K 4 P 3 , K 5 P 4 , KP, K 4 P 6 , K 3 П 7 , К 3 П 11 , КП 10.3 и КП 15 . [121] Хотя большинство металлов образуют арсениды, только щелочные и щелочноземельные металлы образуют в основном ионные арсениды. Структура Na 3 As сложна с необычно короткими расстояниями Na–Na (328–330 пм), которые короче, чем у металлического натрия, и это указывает на то, что даже с этими электроположительными металлами связь не может быть прямо ионной. [11] Другие арсениды щелочных металлов, не соответствующие формуле M 3 As, известны, например, LiAs, который имеет металлический блеск и электропроводность, что указывает на наличие некоторой металлической связи . [11] Антимониды нестабильны и реакционноспособны, поскольку ион Sb 3- является сильным восстановителем; реакция их с кислотами образует токсичный и нестабильный газ стибин (SbH 3 ). [122] Действительно, они обладают некоторыми металлическими свойствами, а антимониды щелочных металлов стехиометрии MSb включают атомы сурьмы, связанные в спиральную структуру Цинтла. [123] Висмутиды даже не являются полностью ионными; это интерметаллические соединения , содержащие частично металлические и частично ионные связи. [124]
Все щелочные металлы бурно реагируют с кислородом при стандартных условиях. Они образуют различные типы оксидов, такие как простые оксиды (содержащие ион O 2− ), пероксиды (содержащие ион O2-2ион, где между двумя атомами кислорода существует одинарная связь ), супероксиды (содержащие O−2ион) и многие другие. Литий сгорает на воздухе с образованием оксида лития , а натрий реагирует с кислородом с образованием смеси оксида натрия и пероксида натрия . Калий образует смесь пероксида калия и супероксида калия , тогда как рубидий и цезий образуют исключительно супероксид. Спускаясь по группе, их реакционная способность возрастает: если литий, натрий и калий просто горят на воздухе, то рубидий и цезий пирофорны (самопроизвольно загораются на воздухе). [85]
Щелочные металлы меньшего размера имеют тенденцию поляризовать более крупные анионы (пероксид и супероксид) из-за их небольшого размера. Это притягивает электроны более сложных анионов к одному из составляющих его атомов кислорода, образуя оксидный ион и атом кислорода. Это заставляет литий образовывать оксид исключительно при реакции с кислородом при комнатной температуре. Этот эффект становится значительно слабее для более крупных натрия и калия, позволяя им образовывать менее стабильные пероксиды. Рубидий и цезий, находящиеся в нижней части группы, настолько велики, что могут образовываться даже наименее стабильные супероксиды. Поскольку супероксид при образовании выделяет больше всего энергии, он предпочтительно образуется для более крупных щелочных металлов, где более сложные анионы не поляризованы. Оксиды и пероксиды этих щелочных металлов существуют, но не образуются при прямой реакции металла с кислородом в стандартных условиях. [85] Кроме того, малый размер ионов Li + и O 2− способствует формированию ими устойчивой ионной структуры решетки. Однако известно, что в контролируемых условиях все щелочные металлы, за исключением франция, образуют оксиды, пероксиды и супероксиды. Пероксиды и супероксиды щелочных металлов являются сильными окислителями . Пероксид натрия и супероксид калия вступают в реакцию с диоксидом углерода с образованием карбоната щелочного металла и газообразного кислорода, что позволяет использовать их в очистителях воздуха для подводных лодок ; присутствие водяного пара , естественно присутствующего в дыхании, делает удаление углекислого газа супероксидом калия еще более эффективным. [66] [125] Все стабильные щелочные металлы, за исключением лития, могут образовывать красные озониды (MO 3 ) посредством низкотемпературной реакции порошкообразного безводного гидроксида с озоном : озониды можно затем экстрагировать с использованием жидкого аммиака . Они медленно разлагаются при стандартных условиях на супероксиды и кислород и немедленно гидролизуются до гидроксидов при контакте с водой. [11] : 85 Калий, рубидий и цезий также образуют полуторные оксиды M 2 O 3 , которые лучше считать пероксиддисупероксидами, [(M + ) 4 (O2-2)(О−2) 2 ] . [11] : 85
Рубидий и цезий могут образовывать множество субоксидов с металлами в формальных степенях окисления ниже +1. [11] : 85 Рубидий может образовывать Rb 6 O и Rb 9 O 2 (медного цвета) при окислении на воздухе, тогда как цезий образует огромное разнообразие оксидов, таких как озонид CsO 3 [126] [127] и несколько ярких цветные субоксиды , [128] такие как Cs 7 O (бронзовый), Cs 4 O (красно-фиолетовый), Cs 11 O 3 (фиолетовый), Cs 3 O (темно-зеленый), [129] CsO, Cs 3 O 2 , [130] , а также Cs 7 O 2 . [131] [132] Последний из них можно нагреть в вакууме для получения Cs 2 O. [57]
Аналогично могут реагировать щелочные металлы и с более тяжелыми халькогенами ( серой , селеном , теллуром и полонием ), известны все халькогениды щелочных металлов (за исключением франция). Реакция с избытком халькогена может аналогичным образом привести к образованию низших халькогенидов, в которых ионы халькогена содержат цепочки рассматриваемых атомов халькогена. Например, натрий может реагировать с серой с образованием сульфида ( Na 2 S ) и различных полисульфидов с формулой Na 2 S x ( x от 2 до 6), содержащих S2−
хионы. [66] Из-за основности ионов Se 2- и Te 2- селениды и теллуриды щелочных металлов являются щелочными в растворе; при непосредственной реакции с селеном и теллуром наряду с селенидами и теллуридами с Se образуются полиселениды и полителлуриды щелочных металлов .2−
хи Те2−
хионы. [133] Их можно получить непосредственно из элементов в жидком аммиаке или в отсутствие воздуха и представляют собой бесцветные водорастворимые соединения, которые на воздухе быстро окисляются обратно до селена или теллура. [11] : 766 Все полониды щелочных металлов представляют собой ионные соединения, содержащие ион Po 2- ; они очень химически стабильны и могут быть получены путем прямой реакции элементов при температуре около 300–400 ° C. [11] : 766 [134] [135]
Щелочные металлы являются одними из наиболее электроположительных элементов таблицы Менделеева и поэтому имеют тенденцию ионно связываться с наиболее электроотрицательными элементами таблицы Менделеева, галогенами ( фтором , хлором , бромом , йодом и астатом ), образуя соли, известные как щелочи. галогениды металлов. Реакция очень бурная и иногда может приводить к взрывам. [11] : 76 Известны все двадцать стабильных галогенидов щелочных металлов; нестабильные неизвестны, за исключением астатида натрия, из-за большой нестабильности и редкости астата и франция. Самым известным из двадцати, безусловно, является хлорид натрия , также известный как поваренная соль. Все стабильные галогениды щелочных металлов имеют формулу MX, где M — щелочной металл, а X — галоген. Все они представляют собой белые ионные кристаллические вещества с высокими температурами плавления. [5] [85] Все галогениды щелочных металлов растворимы в воде, за исключением фторида лития (LiF), который нерастворим в воде из-за очень высокой энтальпии решетки . Высокая энтальпия решетки фторида лития обусловлена малыми размерами ионов Li + и F − , что приводит к сильным электростатическим взаимодействиям между ними: [5] аналогичный эффект имеет место для фторида магния , что согласуется с диагональной зависимостью между литием и магний. [11] : 76
Щелочные металлы также аналогичным образом реагируют с водородом с образованием ионных гидридов щелочных металлов, где анион гидрида действует как псевдогалогенид : их часто используют в качестве восстановителей, производя гидриды, комплексные гидриды металлов или газообразный водород. [11] : 83 [66] Другие псевдогалогениды также известны, особенно цианиды . Они изоструктурны соответствующим галогенидам, за исключением цианида лития , что указывает на то, что ионы цианида могут свободно вращаться. [11] : 322 Тройные галоидоксиды щелочных металлов, такие как Na 3 ClO, K 3 BrO (желтый), Na 4 Br 2 O, Na 4 I 2 O и K 4 Br 2 O, также известны. [11] : 83 Полигалогениды довольно нестабильны, хотя полигалогениды рубидия и цезия в значительной степени стабилизированы благодаря слабой поляризующей способности этих чрезвычайно крупных катионов. [11] : 835
Катионы щелочных металлов обычно не образуют координационные комплексы с простыми основаниями Льюиса из-за их низкого заряда всего +1 и относительно большого размера; таким образом, ион Li + образует большинство комплексов, а более тяжелые ионы щелочных металлов образуют все меньше и меньше (хотя для слабых комплексов случаются исключения). [11] : Литий 90, в частности, имеет очень богатую координационную химию, в которой он демонстрирует координационные числа от 1 до 12, хотя октаэдрическая гексакоординация является его предпочтительным способом. [11] : 90–1 В водном растворе ионы щелочных металлов существуют в виде октаэдрических гексагидратных комплексов [M(H 2 O) 6 ] + , за исключением иона лития, который из-за своего малого размера образует тетраэдрические тетрагидратные комплексы [11] : 90–1. Li(H 2 O) 4 ] + ; щелочные металлы образуют эти комплексы, поскольку их ионы притягиваются электростатическими силами притяжения к полярным молекулам воды. По этой причине в качестве осушителей часто используют безводные соли, содержащие катионы щелочных металлов . [66] Щелочные металлы также легко образуют комплексы с краун-эфирами (например , 12-краун-4 для Li + , 15-краун-5 для Na + , 18-краун-6 для K + и 21-краун-7 для Rb +). ) и криптанды за счет электростатического притяжения. [66]
Щелочные металлы медленно растворяются в жидком аммиаке , образуя аммиачные растворы сольватированного катиона металла M + и сольватированного электрона e - , которые реагируют с образованием газообразного водорода и амида щелочного металла (MNH 2 , где M представляет собой щелочной металл): это было впервые отмечен Хамфри Дэви в 1809 г. и вновь открыт У. Вейлем в 1864 г. Процесс можно ускорить с помощью катализатора . Аналогичные растворы образуют тяжелые двухвалентные щелочноземельные металлы кальций , стронций , барий , а также двухвалентные лантаноиды , европий и иттербий . Амидная соль совершенно нерастворима и легко выпадает в осадок из раствора, оставляя интенсивно окрашенные аммиачные растворы щелочных металлов. В 1907 году Чарльз А. Краус определил, что цвет обусловлен наличием сольватированных электронов , которые способствуют высокой электропроводности этих растворов. При низких концентрациях (ниже 3 М) раствор имеет темно-синий цвет и имеет проводимость в десять раз большую, чем водный раствор хлорида натрия ; при более высоких концентрациях (свыше 3 М) раствор имеет медный цвет и имеет проводимость примерно как у жидких металлов, таких как ртуть . [11] [66] [137] Помимо амидной соли щелочного металла и сольватированных электронов, такие растворы аммиака также содержат катион щелочного металла (М + ), нейтральный атом щелочного металла (М), двухатомные молекулы щелочного металла (М 2 ) и анионы щелочных металлов (M − ). Они нестабильны и в конечном итоге становятся более термодинамически стабильными амидом щелочного металла и газообразным водородом. Сольватированные электроны являются мощными восстановителями и часто используются в химическом синтезе. [66]


Будучи самым маленьким щелочным металлом, литий образует самое большое разнообразие и наиболее стабильные металлоорганические соединения , связанные ковалентной связью. Литийорганические соединения представляют собой электрически непроводящие летучие твердые вещества или жидкости, которые плавятся при низких температурах и имеют тенденцию образовывать олигомеры со структурой (RLi) x , где R — органическая группа. Поскольку электроположительная природа лития передает большую часть плотности заряда связи на атом углерода, эффективно создавая карбанион , литийорганические соединения являются чрезвычайно мощными основаниями и нуклеофилами . В качестве оснований часто используют бутиллитий , который имеется в продаже. Примером литийорганического соединения является метиллитий ((CH 3 Li) x ), который существует в тетрамерной ( x = 4, тетраэдрическая) и гексамерной ( x = 6, октаэдрическая) формах. [66] [141] Литийорганические соединения, особенно н -бутиллитий, являются полезными реагентами в органическом синтезе, как и следовало ожидать, учитывая диагональное соотношение лития с магнием, которое играет важную роль в реакции Гриньяра . [11] : 102 Например, алкиллитии и ариллитии можно использовать для синтеза альдегидов и кетонов путем реакции с карбонилами металлов . Реакция с тетракарбонилом никеля , например, протекает через нестабильный ацилкарбонильный комплекс никеля, который затем подвергается электрофильному замещению с образованием желаемого альдегида (с использованием H + в качестве электрофила) или кетона (с использованием алкилгалогенида). [11] : 105
Алкиллитии и ариллитии могут также реагировать с N , N -дизамещенными амидами с образованием альдегидов и кетонов, а также симметричных кетонов при взаимодействии с окисью углерода . Они термически разлагаются с выделением β-водорода с образованием алкенов и гидрида лития : другой путь — реакция простых эфиров с алкил- и ариллитием, которые действуют как сильные основания. [11] : 105 В неполярных растворителях ариллитий реагирует как карбанионы, которыми они фактически являются, превращая диоксид углерода в ароматические карбоновые кислоты (ArCO 2 H), а арилкетоны - в третичные карбинолы (Ar' 2 C(Ar)OH). Наконец, их можно использовать для синтеза других металлоорганических соединений путем обмена металл-галоген. [11] : 106
В отличие от литийорганических соединений, металлоорганические соединения более тяжелых щелочных металлов являются преимущественно ионными. Применение натрийорганических соединений в химии ограничено отчасти из-за конкуренции со стороны литийорганических соединений , которые коммерчески доступны и проявляют более удобную реакционную способность. Основным натрийорганическим соединением, имеющим коммерческое значение, является циклопентадиенид натрия . Тетрафенилборат натрия также можно отнести к натрийорганическим соединениям, поскольку в твердом состоянии натрий связан с арильными группами. Металлоорганические соединения высших щелочных металлов еще более реакционноспособны, чем натрийорганические соединения, и имеют ограниченное применение. Примечательным реагентом является основание Шлоссера , смесь н -бутиллития и трет -бутоксида калия . Этот реагент реагирует с пропеном с образованием соединения аллилкалий (KCH 2 CHCH 2 ). Цис -2-бутен и транс -2-бутен уравновешиваются при контакте с щелочными металлами. В то время как изомеризация лития и натрия протекает быстро, с более тяжелыми щелочными металлами она протекает медленно. Более тяжелые щелочные металлы также благоприятствуют стерически перегруженной конформации. [142] Сообщалось о нескольких кристаллических структурах калийорганических соединений, устанавливающих, что они, как и соединения натрия, являются полимерными. [143] Натрий-, калий-органические, рубидий- и цезиорганические соединения являются в основном ионными и нерастворимы (или почти нерастворимы) в неполярных растворителях. [66]
Алкильные и арильные производные натрия и калия склонны вступать в реакцию с воздухом. Они вызывают расщепление простых эфиров с образованием алкоксидов. В отличие от соединений алкиллития, алкилнатрий и алкилкалий не могут быть получены путем реакции металлов с алкилгалогенидами, поскольку происходит сочетание Вюрца : [123] : 265
По существу, их необходимо получать путем взаимодействия соединений алкилртути с металлическим натрием или калием в инертных углеводородных растворителях. В то время как метилнатрий образует тетрамеры, такие как метиллитий, метилкалий более ионный и имеет структуру арсенида никеля с дискретными метил-анионами и катионами калия. [123] : 265
Щелочные металлы и их гидриды реагируют с кислыми углеводородами, например циклопентадиенами и терминальными алкинами, с образованием солей. Используются жидкий аммиак, эфир или углеводородные растворители, наиболее распространенным из которых является тетрагидрофуран . Наиболее важным из этих соединений является циклопентадиенид натрия NaC 5 H 5 , важный предшественник многих циклопентадиенильных производных переходных металлов. [123] :265 Аналогичным образом щелочные металлы реагируют с циклооктатетраеном в тетрагидрофуране с образованием циклооктатетраенидов щелочных металлов ; например, циклооктатетраенид дикалия (K 2 C 8 H 8 ) является важным предшественником многих производных циклооктатетраенила металлов, таких как ураноцен . [123] : 266 Крупные и очень слабо поляризующиеся катионы щелочных металлов могут стабилизировать крупные ароматические поляризуемые анион-радикалы, такие как темно-зеленый нафталинид натрия Na + [C 10 H 8 •] - , сильный восстановитель. [123] : 266
Щелочные металлы при взаимодействии с кислородом образуют оксиды , пероксиды , супероксиды и субоксиды . Однако первые три встречаются чаще. В таблице ниже [144] показаны типы соединений, образующихся при реакции с кислородом. Соединение в скобках представляет собой второстепенный продукт сгорания.
Пероксиды щелочных металлов представляют собой ионные соединения, нестабильные в воде. Пероксидный анион слабо связан с катионом и гидролизуется, образуя более прочные ковалентные связи.
Остальные соединения кислорода также нестабильны в воде.
С серой они образуют сульфиды и полисульфиды . [146]
Поскольку сульфиды щелочных металлов представляют собой по существу соли слабой кислоты и сильного основания, они образуют основные растворы.
Литий — единственный металл, который напрямую соединяется с азотом при комнатной температуре.
Li 3 N может реагировать с водой с выделением аммиака.
С водородом щелочные металлы образуют солевые гидриды , которые гидролизуются в воде.
Литий — единственный металл, который непосредственно реагирует с углеродом с образованием ацетилида дилития . Na и K могут реагировать с ацетиленом с образованием ацетилидов . [147]
При реакции с водой они генерируют гидроксид- ионы и газообразный водород. Эта реакция является энергичной и сильно экзотермической, и образующийся водород может воспламениться на воздухе или даже взорваться в случае Rb и Cs. [144]
Щелочные металлы являются очень хорошими восстановителями. Они могут восстанавливать катионы металлов, которые менее электроположительны. Титан получают в промышленных масштабах восстановлением тетрахлорида титана Na при 400 °C ( процесс Ван Аркеля-де Бура ).
Щелочные металлы реагируют с производными галогенов с образованием углеводорода посредством реакции Вюрца .
Щелочные металлы растворяются в жидком аммиаке или других растворителях-донорах, таких как алифатические амины или гексаметилфосфорамид, с образованием растворов синего цвета. Считается, что эти растворы содержат свободные электроны. [144]
Благодаря наличию сольватированных электронов эти растворы являются очень мощными восстановителями, используемыми в органическом синтезе.

Реакция 1) известна как редукция Берча . Другими сокращениями [144] , которые можно осуществить с помощью этих решений, являются:

Хотя франций является самым тяжелым из когда-либо обнаруженных щелочных металлов, были проведены некоторые теоретические работы, предсказывающие физические и химические характеристики гипотетических более тяжелых щелочных металлов. Будучи первым элементом 8-го периода , неоткрытый элемент унунний (элемент 119), по прогнозам, станет следующим щелочным металлом после франция и будет вести себя так же, как и его более легкие родственники ; однако прогнозируется, что он будет отличаться от более легких щелочных металлов некоторыми свойствами. [37] : 1729–1730. По прогнозам, его химический состав будет ближе к калию [42] или рубидию [37] : 1729–1730 вместо цезия или франция. Это необычно, поскольку периодические тенденции , игнорирующие релятивистские эффекты, предсказывают, что унунений будет даже более реакционноспособным, чем цезий и франций. Эта пониженная реакционная способность происходит из-за релятивистской стабилизации валентного электрона унуненния, увеличения первой энергии ионизации унунения и уменьшения металлического и ионного радиусов ; [42] этот эффект уже наблюдается для франция. [37] : 1729–1730 Это предполагает, что унунений будет вести себя химически как щелочной металл, что, хотя и вероятно, может быть неверным из-за релятивистских эффектов. [149] Релятивистская стабилизация 8s-орбитали также увеличивает сродство унунния к электрону, намного превосходящее сродство цезия и франция; действительно, ожидается, что унунений будет иметь сродство к электрону выше, чем все более легкие щелочные металлы, чем он. Релятивистские эффекты также вызывают очень сильное падение поляризуемости унунения . [37] : 1729–1730 С другой стороны, прогнозируется, что унунений продолжит тенденцию снижения температуры плавления по мере спуска по группе, поскольку ожидается, что температура плавления будет находиться в диапазоне от 0 ° C до 30 ° C. [37] : 1724

Стабилизация валентного электрона унунения и, таким образом, сжатие 8s-орбитали приводит к уменьшению его атомного радиуса до 240 пм , [37] : 1729–1730, что очень близко к радиусу рубидия (247 пм), [5] , так что химия Унуненний в степени окисления +1 должен быть больше похож по химическому составу на рубидий, чем на франций. С другой стороны, прогнозируется, что ионный радиус иона Uue + будет больше, чем у Rb + , поскольку 7p-орбитали дестабилизированы и, следовательно, больше, чем p-орбитали нижних оболочек. Унуненний может также проявлять степени окисления +3 [37] : 1729–1730 и +5 , [150] которые не наблюдаются ни в одном другом щелочном металле, [11] : 28 в дополнение к степени окисления +1, которая характерна для другие щелочные металлы, а также является основной степенью окисления всех известных щелочных металлов: это происходит из-за дестабилизации и расширения спинора 7p 3/2 , в результате чего его крайние электроны имеют более низкую энергию ионизации, чем можно было бы ожидать в противном случае. . [11] : 28 [37] : 1729–1730 Действительно, ожидается, что многие соединения унунения будут иметь сильный ковалентный характер из-за участия электронов 7p 3/2 в связи. [87]
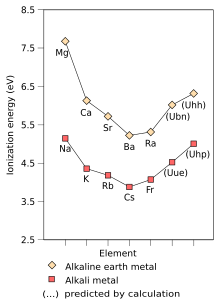
Не так много работы было сделано для предсказания свойств щелочных металлов за пределами унунния. Хотя простая экстраполяция таблицы Менделеева (по принципу Ауфбау ) поместила бы элемент 169, унгексенний, под унунений, расчеты Дирака-Фока предсказывают, что следующим элементом после унунения со свойствами, подобными щелочному металлу, может быть элемент 165, унгексенний, который по прогнозам, будет иметь электронную конфигурацию [Og] 5g 18 6f 14 7d 10 8s 2 8p 1/2 2 9s 1 . [37] : 1729–1730 [148] Этот элемент будет занимать промежуточное положение по свойствам между щелочным металлом и элементом 11-й группы , и хотя его физические и атомные свойства будут ближе к первому, его химический состав может быть ближе к химическому составу последний. Дальнейшие расчеты показывают, что унгексентий будет следовать тенденции увеличения энергии ионизации по сравнению с цезием, имея энергию ионизации, сравнимую с энергией ионизации натрия, и что он также должен продолжать тенденцию уменьшения атомных радиусов за пределами цезия, имея атомный радиус, сравнимый с атомным радиусом калия. . [37] : 1729–1730 Однако 7d-электроны унгекспентия также могут участвовать в химических реакциях вместе с 9s-электроном, возможно, допуская состояния окисления выше +1, откуда вероятное поведение унгекспентия в качестве переходного металла. [37] : 1732–1733 [151] Поскольку щелочные и щелочноземельные металлы оба являются элементами s-блока , эти предсказания тенденций и свойств унунения и унгексентия также в основном справедливы для соответствующих щелочноземельных металлов унбинилия (Ubn ) и унгексексий (Ухх). [37] : 1729–1733 Унсепттрий, элемент 173, может быть еще лучшим более тяжелым гомологом унунения; с предсказанной электронной конфигурацией [Usb] 6g 1 , он возвращается к ситуации, подобной щелочному металлу, когда один легко удаляемый электрон находится намного выше закрытой p-оболочки по энергии, и, как ожидается, будет даже более реакционноспособным, чем цезий. [152] [153]
Вероятные свойства других щелочных металлов, помимо ансептрия, по состоянию на 2019 год еще не исследованы, и они могут существовать, а могут и не существовать. [148] В периодах 8 и выше периодической таблицы релятивистские эффекты и эффекты оболочечной структуры становятся настолько сильными, что экстраполяции от более легких родственных соединений становятся совершенно неточными. Кроме того, релятивистские эффекты и эффекты оболочечной структуры (которые стабилизируют s-орбитали и дестабилизируют и расширяют d-, f- и g-орбитали более высоких оболочек) имеют противоположные эффекты, вызывая еще большую разницу между релятивистскими и нерелятивистскими орбиталями. расчеты свойств элементов с такими высокими атомными номерами. [37] : 1732–1733 Интерес к химическим свойствам унунения, унекспентия и унсептрия обусловлен тем, что они расположены вблизи ожидаемых мест расположения островов стабильности с центрами элементов 122 ( 306 Ubb) и 164 ( 482 Uhq) . ). [154] [155] [156]
Многие другие вещества сходны с щелочными металлами по своей склонности к образованию моноположительных катионов. По аналогии с псевдогалогенами их иногда называют «псевдощелочными металлами». Эти вещества включают в себя некоторые элементы и еще много многоатомных ионов ; многоатомные ионы особенно похожи на щелочные металлы своим большим размером и слабой поляризующей способностью. [157]
Элемент водород с одним электроном на нейтральный атом обычно помещается в верхнюю часть первой группы периодической таблицы из-за его электронной конфигурации. Но водород обычно не считается щелочным металлом. [158] Металлический водород , который существует только при очень высоких давлениях, известен своими электрическими и магнитными свойствами, а не химическими свойствами. [159] В типичных условиях чистый водород существует в виде двухатомного газа, состоящего из двух атомов на молекулу (H 2 ); [160] Однако щелочные металлы образуют двухатомные молекулы (например, дилитий , Li 2 ) только при высоких температурах, когда они находятся в газообразном состоянии. [161]
Водород, как и щелочные металлы, имеет один валентный электрон [123] и легко реагирует с галогенами [123] , но на этом сходство в основном заканчивается из-за малого размера голого протона H + по сравнению с катионами щелочных металлов. [123] Его расположение над литием обусловлено, прежде всего, его электронной конфигурацией . [158] Иногда его ставят выше фтора из-за схожих химических свойств, хотя сходство также не является абсолютным. [162]
Первая энергия ионизации водорода (1312,0 кДж/моль ) значительно выше, чем у щелочных металлов. [163] [164] Поскольку для заполнения внешней оболочки атома водорода требуется только один дополнительный электрон, водород часто ведет себя как галоген, образуя отрицательный гидрид- ион, и на этом основании очень иногда считается галогеном. (Щелочные металлы также могут образовывать отрицательные ионы, известные как алкалиды , но это не более чем лабораторные диковинки, поскольку они нестабильны.) [80] [81] Аргументом против такого размещения является то, что образование гидрида из водорода является эндотермическим процессом, в отличие от экзотермическое образование галогенидов из галогенов. Радиус аниона H - также не соответствует тенденции увеличения размера вниз по галогенам: действительно, H - очень размыт, потому что его единственный протон не может легко контролировать оба электрона. [123] : 15–6 Некоторое время ожидалось, что жидкий водород проявит металлические свойства; [162] хотя было показано, что это не так, при чрезвычайно высоких давлениях , например, в ядрах Юпитера и Сатурна , водород действительно становится металлическим и ведет себя как щелочной металл; на этой стадии он известен как металлический водород . [165] Электросопротивление жидкого металлического водорода при 3000 К примерно равно удельному сопротивлению жидких рубидия и цезия при 2000 К при соответствующих давлениях, когда они претерпевают переход неметалл-металл. [166]
Электронная конфигурация водорода 1s 1 , хотя и аналогична конфигурации щелочных металлов (ns 1 ), уникальна, поскольку в ней нет подоболочки 1p. Следовательно, он может потерять электрон с образованием гидрона H + или получить его с образованием гидрид- иона H - . [11] : 43 В первом случае он внешне напоминает щелочные металлы; в последнем случае это галогены, но различия, связанные с отсутствием подоболочки 1p, настолько важны, что ни одна из групп не соответствует свойствам водорода. [11] : 43 Группа 14 также хорошо подходит с точки зрения термодинамических свойств, таких как энергия ионизации и сродство к электрону , но водород не может быть четырехвалентным. Таким образом, ни одно из трех положений не является полностью удовлетворительным, хотя группа 1 является наиболее распространенным размещением (если оно выбрано) из-за электронной конфигурации и того факта, что гидрон, безусловно, является наиболее важным из всех одноатомных видов водорода, являясь основой кислотно-щелочной химии. [162] В качестве примера нестандартных свойств водорода, обусловленных его необычной электронной конфигурацией и небольшим размером, ион водорода очень мал (радиус около 150 фм по сравнению с размером 50–220 пм большинства других атомов и ионов) и поэтому не существует. в конденсированных системах, за исключением ассоциации с другими атомами или молекулами. Действительно, перенос протонов между химическими веществами является основой кислотно-щелочной химии . [11] : 43 Также уникальной является способность водорода образовывать водородные связи , которые являются результатом явлений переноса заряда, электростатических и электронных корреляций. [162] Хотя аналогичные связи лития также известны, они в основном электростатические. [162] Тем не менее, водород может брать на себя ту же структурную роль, что и щелочные металлы в некоторых молекулярных кристаллах, и имеет тесную связь с легчайшими щелочными металлами (особенно с литием). [167]

Ион аммония ( NH+4) имеет очень схожие свойства с более тяжелыми щелочными металлами, действует как промежуточный щелочной металл между калием и рубидием [157] [168] и часто считается близким родственником. [169] [170] [ 171 ] Например, большинство солей щелочных металлов растворимы в воде, и это свойство присуще солям аммония. [172] Ожидается, что аммоний будет вести себя стабильно как металл ( NH+4ионы в море делокализованных электронов) при очень высоких давлениях (хотя и меньших, чем обычное давление, при котором происходят переходы от изолирующего к металлическому поведению, около 100 ГПа ), и, возможно, могут возникать внутри ледяных гигантов Урана и Нептуна , что может иметь значительные последствия. на их внутренние магнитные поля. [170] [171] Было подсчитано, что переход от смеси молекул аммиака и диводорода к металлическому аммонию может происходить при давлениях чуть ниже 25 ГПа. [170] В стандартных условиях аммоний может образовывать металлическую амальгаму с ртутью. [173]
Другие «псевдощелочные металлы» включают катионы алкиламмония , в которых некоторые атомы водорода в катионе аммония заменены алкильными или арильными группами. В частности, катионы четвертичного аммония ( NR+4) очень полезны, поскольку они постоянно заряжены, и их часто используют в качестве альтернативы дорогому Cs + для стабилизации очень крупных и очень легко поляризуемых анионов, таких как HI .−2. [11] : 812–9 Гидроксиды тетраалкиламмония, как и гидроксиды щелочных металлов, являются очень сильными основаниями, которые реагируют с углекислым газом воздуха с образованием карбонатов. [123] : 256 Кроме того, атом азота может быть заменен атомом фосфора, мышьяка или сурьмы (более тяжелые неметаллические пниктогены ), образуя фосфоний ( PH+4) или арсоний ( AsH+4) катион, который сам может быть замещен аналогичным образом; в то время как стибоний ( SbH+4) сам по себе не известен, охарактеризованы некоторые его органические производные. [157]
Кобальтоцен , Co(C 5 H 5 ) 2 , представляет собой металлоцен , кобальтовый аналог ферроцена . Это темно-фиолетовое твердое вещество. Кобальтоцен имеет 19 валентных электронов, что на один больше, чем обычно встречается в комплексах органопереходных металлов, таких как его очень стабильный родственник ферроцен, в соответствии с правилом 18 электронов . Этот дополнительный электрон занимает орбиталь, разрыхляющую по отношению к связям Co–C. Следовательно, многие химические реакции Co(C 5 H 5 ) 2 характеризуются его тенденцией терять этот «лишний» электрон, образуя очень стабильный 18-электронный катион, известный как кобальтоцений. Многие соли кобальтоцения соосаждаются с солями цезия, а гидроксид кобальтоцения является сильным основанием, которое поглощает углекислый газ из воздуха с образованием карбоната кобальтоцения. [123] : 256 Как и щелочные металлы, кобальтоцен является сильным восстановителем, а декаметилкобальтоцен еще сильнее из-за совместного индуктивного эффекта десяти метильных групп. [174] Кобальт может быть заменен его более тяжелым родственным родием , чтобы получить родоцен , еще более сильный восстановитель. [175] Иридоцен (с участием иридия ), по-видимому, еще более эффективен, но он не очень хорошо изучен из-за своей нестабильности. [176]

Таллий — самый тяжелый стабильный элемент 13-й группы таблицы Менделеева. В нижней части таблицы Менделеева эффект инертной пары довольно силен из-за релятивистской стабилизации 6s-орбитали и уменьшения энергии связи по мере увеличения размера атомов, так что количество энергии, высвобождаемой при образовании еще двух связей, равно не стоит высоких энергий ионизации 6s-электронов. [11] : 226–7 Он демонстрирует степень окисления +1 [11] : 28 , которую проявляют все известные щелочные металлы, [11] : 28 и соединения таллия с таллием в степени окисления +1 очень напоминают соответствующие калий или серебро. соединения стехиометрически обусловлены близкими ионными радиусами ионов Tl + (164 пм ), K + (152 пм) и Ag + (129 пм). [177] [178] Иногда его считали щелочным металлом в континентальной Европе (но не в Англии) в первые годы после его открытия, [178] : 126 , и он был помещен сразу после цезия как шестой щелочной металл в книге Дмитрия Менделеева . периодическая таблица 1869 года и периодическая таблица Юлиуса Лотара Мейера 1868 года. [22] В периодической таблице Менделеева 1871 года и периодической таблице Мейера 1870 года таллий помещен в его нынешнее положение в группе бора , а пространство под цезием оставлено пустым. [22] Однако таллий также имеет степень окисления +3, [11] : 28 , которую не проявляет ни один известный щелочной металл [11] : 28 (хотя прогнозируется, что унунний, неоткрытый седьмой щелочной металл, возможно, будет иметь степень окисления +3). ). [37] : 1729–1730 Шестым щелочным металлом сейчас считается франций. [179] Хотя Tl + стабилизируется эффектом инертной пары, эта инертная пара 6s-электронов все еще способна участвовать в химическом процессе, так что эти электроны стереохимически активны в водном растворе. Кроме того, галогениды таллия (кроме TlF ) совершенно нерастворимы в воде, а TlI имеет необычную структуру из-за присутствия в таллии стереохимически активной инертной пары. [180]
Металлы группы 11 (или металлы чеканки), медь, серебро и золото, обычно относят к категории переходных металлов, поскольку они могут образовывать ионы с неполными d-оболочками. Физически они имеют относительно низкие температуры плавления и высокие значения электроотрицательности, присущие постпереходным металлам . «Заполненная d- подоболочка и свободный s- электрон Cu, Ag и Au способствуют их высокой электро- и теплопроводности. Переходные металлы слева от группы 11 испытывают взаимодействия между s- электронами и частично заполненной d- подоболочкой, что снижает подвижность электронов». [181] Химически металлы группы 11 ведут себя как металлы основной группы в своих валентных состояниях +1 и, следовательно, в некоторой степени связаны с щелочными металлами: это одна из причин, по которой их ранее называли «группой IB», параллельно щелочным металлам. металлы «группы IA». Иногда их относят к постпереходным металлам. [182] Их спектры аналогичны спектрам щелочных металлов. [30] Их моноположительные ионы парамагнитны и не придают окраски их солям, как ионы щелочных металлов. [183]
В периодической таблице Менделеева 1871 года медь, серебро и золото указаны дважды: один раз в группе VIII (с триадой железа и металлами платиновой группы ) и один раз в группе IB. Группа IB, тем не менее, была заключена в скобки, чтобы отметить, что она носит предварительный характер. Основным критерием отнесения к группе Менделеева была максимальная степень окисления элемента: на этом основании элементы 11 группы не могли быть отнесены к группе IB из-за существования в то время известных соединений меди(II) и золота(III). время. [30] Однако исключение группы IB сделало бы группу I единственной основной группой (группа VIII была названа переходной группой), в которой отсутствует бифуркация A-B. [30] Вскоре после этого большинство химиков решили отнести эти элементы к группе IB и исключить их из группы VIII из-за полученной симметрии: это была преобладающая классификация до появления современной таблицы Менделеева средней длины с 18 столбцами, которая разделили щелочные металлы и металлы 11 группы. [30]
Металлы для чеканки традиционно рассматривались как подразделение группы щелочных металлов, поскольку они имеют характерную электронную конфигурацию s 1 щелочных металлов (группа 1: p 6 s 1 ; группа 11: d 10 s 1 ). Однако сходство во многом ограничивается стехиометрией +1 соединений обеих групп, а не их химическими свойствами. [11] : 1177 Это связано с тем, что заполненная подоболочка d обеспечивает гораздо более слабый экранирующий эффект на самый внешний s-электрон, чем заполненная подоболочка p, так что металлы чеканки имеют гораздо более высокие энергии первой ионизации и меньшие ионные радиусы, чем соответствующие щелочные металлы. . [11] : 1177 Кроме того, они имеют более высокие температуры плавления, твердость и плотность, а также более низкую реакционную способность и растворимость в жидком аммиаке , а также имеют более ковалентный характер в своих соединениях. [11] : 1177 Наконец, щелочные металлы находятся на вершине электрохимического ряда , тогда как металлы чеканки находятся почти в самом низу. [11] : 1177 Заполненная d-оболочка чеканных металлов гораздо легче разрушается, чем заполненная p-оболочка щелочных металлов, так что вторая и третья энергии ионизации ниже, что обеспечивает более высокие степени окисления, чем +1, и более богатую координационную химию, тем самым придавая металлам 11 группы явный характер переходных металлов . [11] : 1177 Особого внимания заслуживает образование ионных соединений золота с рубидием и цезием, в которых оно образует аурид-ион (Au − ), который также встречается в сольватированной форме в растворе жидкого аммиака: здесь золото ведет себя как псевдогалоген , поскольку его 5d 10 6s Конфигурация 1 имеет на один электрон меньше, чем конфигурация квазизамкнутой оболочки 5d 10 6s 2 ртути . [11] : 1177
Производство чистых щелочных металлов несколько затруднено из-за их чрезвычайной реакционной способности с обычно используемыми веществами, такими как вода. [5] [66] Из силикатных руд все стабильные щелочные металлы могут быть получены одним и тем же способом: сначала используется серная кислота для растворения желаемого иона щелочного металла и ионов алюминия (III) из руды (выщелачивание), после чего основное осаждение удаляет ионы алюминия из смеси, осаждая их в виде гидроксида . Оставшийся нерастворимый карбонат щелочного металла затем селективно осаждают; затем соль растворяют в соляной кислоте с получением хлорида. Затем результат оставляют испаряться и затем можно выделить щелочной металл. [66] Литий и натрий обычно выделяют электролизом из их жидких хлоридов, при этом обычно добавляют хлорид кальция для снижения температуры плавления смеси. Однако более тяжелые щелочные металлы чаще всего выделяют другим способом, когда для восстановления хлорида щелочного металла используется восстановитель (обычно натрий для калия и магния или кальций для самых тяжелых щелочных металлов). Жидкий или газообразный продукт (щелочной металл) затем подвергается фракционной перегонке для очистки. [66] Большинство способов получения чистых щелочных металлов требуют использования электролиза из-за их высокой реакционной способности; одним из немногих, который этого не делает, является пиролиз соответствующего азида щелочного металла , в результате которого образуются металлы натрия, калия, рубидия и цезия и нитрид лития. [123] : 77
Соли лития приходится добывать из воды минеральных источников , рассолов и месторождений рапы. Металл получают электролитическим способом из смеси плавленых хлоридов лития и хлоридов калия . [184]
Натрий встречается в основном в морской воде и на высушенном морском дне , [5] , но в настоящее время производится электролизом хлорида натрия путем снижения температуры плавления вещества до уровня ниже 700 °C с помощью ячейки Даунса . [185] [186] Чрезвычайно чистый натрий можно получить путем термического разложения азида натрия . [187] Калий встречается во многих минералах, таких как сильвит ( хлорид калия ). [5] Раньше калий обычно получали электролизом хлорида калия или гидроксида калия , [188] широко встречавшегося в таких местах, как Канада, Россия, Беларусь, Германия, Израиль, США и Иордания, методом, аналогичным тому, как натрий производился в конце 1800-х - начале 1900-х годов. [189] Его также можно производить из морской воды . [5] Однако эти методы проблематичны, поскольку металлический калий имеет тенденцию растворяться в расплавленном хлориде и значительно испаряется при рабочих температурах, потенциально образуя взрывоопасный супероксид. В результате чистый металлический калий теперь производится путем восстановления расплавленного хлорида калия металлическим натрием при 850 °C. [11] : 74
Хотя натрий менее реакционноспособен, чем калий, этот процесс работает, потому что при таких высоких температурах калий более летуч, чем натрий, и его легко отогнать, так что равновесие смещается вправо, образуя больше газообразного калия, и продолжается почти до завершения. [11] : 74
Металлы, подобные натрию, получают электролизом расплавленных солей. Rb и Cs получают в основном как продукты переработки лития. Чтобы получить чистый цезий, руды цезия и рубидия измельчаются и нагреваются до 650 °C с металлическим натрием, образуя сплав, который затем можно разделить с помощью метода фракционной перегонки . Поскольку металлический цезий слишком реакционноспособен, его обычно предлагают в виде азида цезия (CsN3). Гидроксид цезия образуется при агрессивном взаимодействии цезия с водой и льдом (CsOH). [190]
Рубидий — 16-й по распространенности элемент в земной коре; однако это довольно редко. Некоторые минералы, найденные в Северной Америке, Южной Африке, России и Канаде, содержат рубидий. Некоторые калийные минералы ( лепидолиты , биотиты , полевые шпаты , карналлит ) содержат его вместе с цезием. Поллуцит , карналлит , лейцит и лепидолит — минералы, содержащие рубидий. В качестве побочного продукта экстракции лития его коммерчески получают из лепидолита . Рубидий также содержится в калиевых породах и рассолах , которые имеются в продаже. Большую часть рубидия сейчас получают как побочный продукт переработки лития. Рубидий используется в электронных лампах в качестве геттера — материала, который соединяется с газовыми примесями и удаляет их из электронных ламп. [191] [192]

В течение нескольких лет, в 1950-х и 1960-х годах, побочный продукт производства калия под названием Алкарб был основным источником рубидия. Алкарб содержал 21% рубидия, остальное — калий и небольшую долю цезия. [193] Сегодня крупнейшие производители цезия, например, шахта Танко в Манитобе, Канада, производят рубидий в качестве побочного продукта из поллуцита . [194] Сегодня распространенным методом отделения рубидия от калия и цезия является фракционная кристаллизация рубидиево-цезиевых квасцов ( Cs , Rb ) Al ( SO 4 ) 2 ·12 H 2 O , которая дает чистые рубидиево-алюмовые квасцы примерно через 30 рекристаллизации. [194] [195] Ограниченное применение и отсутствие минерала, богатого рубидием, ограничивают производство соединений рубидия до 2–4 тонн в год. [194] Цезий, однако, не образуется в результате вышеуказанной реакции. Вместо этого добыча поллуцитовой руды является основным методом получения чистого цезия, извлекаемого из руды в основном тремя методами: кислотным разложением, щелочным разложением и прямым восстановлением. [194] [196] Оба металла производятся как побочные продукты производства лития: после 1958 года, когда интерес к термоядерным свойствам лития резко возрос, производство рубидия и цезия также увеличилось соответственно. [11] : 71 Чистые металлические рубидий и цезий получают восстановлением их хлоридов металлическим кальцием при 750 °C и низком давлении. [11] : 74
Вследствие крайней редкости в природе [63] большая часть франция синтезируется в ядерной реакции 197 Au + 18 O → 210 Fr + 5 n с образованием франция-209 , франция-210 и франция-211 . [197] Наибольшее количество франция, когда-либо собранное на сегодняшний день, составляет около 300 000 нейтральных атомов, [198] которые были синтезированы с использованием приведенной выше ядерной реакции. [198] Когда особенно необходим единственный природный изотоп франций-223, его производят как альфа-дочернюю группу актиния-227, который сам получается синтетическим путем нейтронного облучения природного радия-226, одного из дочерних элементов природного урана-238. [199]
Литий, натрий и калий имеют множество применений, тогда как рубидий и цезий очень полезны в академических целях, но пока не имеют широкого применения. [11] : 68 Литий часто используется в литий-ионных батареях , а оксид лития помогает перерабатывать кремнезем. Стеарат лития является загустителем и может использоваться для изготовления смазок; он производится из гидроксида лития, который также используется для поглощения углекислого газа в космических капсулах и подводных лодках. [11] : Хлорид лития 70 используется в качестве припоя для алюминиевых деталей. [200] Металлический литий используется в сплавах с магнием и алюминием для получения очень прочных и легких сплавов. [11] : 70
Соединения натрия имеют множество применений, наиболее известным из которых является хлорид натрия в виде поваренной соли . В качестве мыла используют натриевые соли жирных кислот . [201] Чистый металлический натрий также имеет множество применений, в том числе использование в натриевых лампах , которые производят очень эффективный свет по сравнению с другими типами освещения, [202] [203] и могут помочь сгладить поверхность других металлов. [204] [205] Будучи сильным восстановителем, он часто используется для восстановления многих других металлов, таких как титан и цирконий , из их хлоридов. Кроме того, он очень полезен в качестве теплообменной жидкости в ядерных реакторах на быстрых нейтронах из-за его низкой температуры плавления, вязкости и способности поглощать нейтроны. [11] : 74
Соединения калия часто используют в качестве удобрений [11] : 73 [206] , поскольку калий является важным элементом питания растений. Гидроксид калия является очень сильным основанием и используется для контроля pH различных веществ. [207] [208] Нитрат калия и перманганат калия часто используются в качестве сильных окислителей. [11] : 73 Супероксид калия используется в дыхательных масках, так как он вступает в реакцию с углекислым газом с образованием карбоната калия и газообразного кислорода. Чистый металлический калий используется нечасто, но его сплавы с натрием могут заменить чистый натрий в ядерных реакторах на быстрых нейтронах. [11] : 74
Рубидий и цезий часто используются в атомных часах . [209] Атомные часы цезия чрезвычайно точны; если бы часы были созданы во времена динозавров, они бы отставали менее чем на четыре секунды (через 80 миллионов лет). [57] По этой причине атомы цезия используются в качестве определения второго. [210] Ионы рубидия часто используются в фиолетовых фейерверках , [211] а цезий часто используется в буровых растворах в нефтяной промышленности. [57] [212]
Франций не имеет коммерческого применения, [61] [62] [213] , но из-за относительно простой атомной структуры франция , среди прочего, он использовался в экспериментах по спектроскопии , что привело к получению большего количества информации об энергетических уровнях и константах связи между субатомными частицами. . [214] Исследования света, излучаемого ионами франция-210, захваченными лазером, предоставили точные данные о переходах между уровнями атомной энергии, аналогичные тем, которые предсказываются квантовой теорией . [215]
Чистые щелочные металлы опасно реагируют с воздухом и водой, и их следует хранить вдали от источников тепла, огня, окислителей, кислот, большинства органических соединений, галогенуглеродов , пластмасс и влаги. Они также реагируют с диоксидом углерода и четыреххлористым углеродом, поэтому обычные огнетушители контрпродуктивны при тушении пожаров щелочных металлов. [216] Некоторые порошковые огнетушители класса D , предназначенные для пожаров металлов, эффективны, лишая огонь кислорода и охлаждая щелочной металл. [217]
Эксперименты обычно проводятся с использованием лишь небольших количеств (несколько граммов) в вытяжном шкафу . Небольшие количества лития можно удалить путем реакции с холодной водой, но более тяжелые щелочные металлы следует растворить в менее реакционноспособном изопропаноле . [216] [218] Щелочные металлы следует хранить под минеральным маслом или в инертной атмосфере. В качестве инертной атмосферы может использоваться аргон или газообразный азот, за исключением лития, который реагирует с азотом. [216] Рубидий и цезий необходимо хранить вдали от воздуха, даже под маслом, потому что даже небольшое количество воздуха, диффундировавшего в масло, может вызвать образование взрывоопасного перекиси; по этой же причине нельзя хранить калий под маслом в кислородсодержащей атмосфере дольше 6 месяцев. [219] [220]

Бионеорганическая химия ионов щелочных металлов широко изучена. [221] Твердотельные кристаллические структуры были определены для многих комплексов ионов щелочных металлов в небольших пептидах, компонентах нуклеиновых кислот, углеводах и ионофорных комплексах. [222]
Литий в природе встречается только в следовых количествах в биологических системах и не имеет известной биологической роли, но оказывает воздействие на организм при попадании в организм. [223] Карбонат лития используется в качестве стабилизатора настроения в психиатрии для лечения биполярного расстройства ( маниакально-депрессивного расстройства ) в ежедневных дозах от 0,5 до 2 граммов, хотя есть и побочные эффекты. [223] Чрезмерное употребление лития вызывает среди других симптомов сонливость, невнятную речь и рвоту, [223] и отравляет центральную нервную систему , [223] что опасно, поскольку необходимая доза лития для лечения биполярного расстройства лишь немного ниже, чем токсическая дозировка. [223] [224] Его биохимия, то, как он обрабатывается человеческим организмом, а также исследования на крысах и козах позволяют предположить, что это важный микроэлемент , хотя естественная биологическая функция лития в организме человека еще не определена. [225] [226]
Натрий и калий встречаются во всех известных биологических системах и обычно функционируют как электролиты внутри и снаружи клеток . [227] [228] Натрий является важным питательным веществом, которое регулирует объем крови, кровяное давление, осмотическое равновесие и pH ; минимальная физиологическая потребность в натрии составляет 500 миллиграмм в сутки. [229] Хлорид натрия (также известный как поваренная соль) является основным источником натрия в рационе и используется в качестве приправы и консерванта, например, для маринования и вяленого мяса ; большая часть его поступает из обработанных пищевых продуктов. [230] Рекомендуемая норма потребления натрия с пищей составляет 1,5 грамма в день, [231] но большинство людей в Соединенных Штатах потребляют более 2,3 грамма в день, [232] минимальное количество, способствующее гипертонии; [233] это, в свою очередь, является причиной 7,6 миллионов преждевременных смертей во всем мире. [234]
Калий является основным катионом (положительным ионом) внутри клеток животных , [227] тогда как натрий является основным катионом вне клеток животных. [227] [228] Разница в концентрации этих заряженных частиц вызывает разницу в электрическом потенциале между внутренней и внешней частью клеток, известную как мембранный потенциал . Баланс между калием и натрием поддерживается белками -переносчиками ионов в клеточной мембране . [235] Потенциал клеточной мембраны, создаваемый ионами калия и натрия, позволяет клетке генерировать потенциал действия — «всплеск» электрического разряда. Способность клеток производить электрический разряд имеет решающее значение для таких функций организма, как нейротрансмиссия , сокращение мышц и функция сердца. [235] Таким образом, нарушение этого баланса может быть фатальным: например, прием больших количеств соединений калия может привести к гиперкалиемии , оказывающей сильное влияние на сердечно-сосудистую систему. [236] [237] Хлорид калия используется в США для казней с помощью смертельных инъекций . [236]

Из-за схожего атомного радиуса рубидий и цезий в организме имитируют калий и усваиваются одинаково. Рубидий не имеет известной биологической роли, но может способствовать стимуляции метаболизма [ 238] [239] [240] и, как и цезий, [238] [241] заменять калий в организме, вызывая дефицит калия . [238] [240] Частичная замена вполне возможна и достаточно нетоксична: человек массой 70 кг содержит в среднем 0,36 г рубидия, а увеличение этого значения в 50–100 раз не выявило у испытуемых отрицательных эффектов. [242] Крысы могут пережить до 50% замены калия рубидием. [240] [243] Рубидий (и в гораздо меньшей степени цезий) может действовать как временное лекарство от гипокалиемии; в то время как рубидий может адекватно физиологически заменить калий в некоторых системах, цезий никогда не сможет этого сделать. [239] Имеются лишь очень ограниченные доказательства в виде симптомов дефицита рубидия, который, возможно, необходим козам; даже если это правда, следовых количеств, обычно присутствующих в пище, более чем достаточно. [244] [245]
Соединения цезия редко встречаются у большинства людей, но большинство соединений цезия умеренно токсичны. Как и рубидий, цезий имеет тенденцию замещать калий в организме, но его размер значительно больше, и поэтому он является худшим заменителем. [241] Избыток цезия может привести к гипокалиемии , аритмии и острой остановке сердца, [246] но такие количества обычно не встречаются в природных источниках. [247] Таким образом, цезий не является основным химическим загрязнителем окружающей среды. [247] Среднее значение летальной дозы (LD 50 ) хлорида цезия для мышей составляет 2,3 г на килограмм, что сопоставимо со значениями LD 50 хлорида калия и хлорида натрия . [248] Хлорид цезия рекламировался как альтернативное лечение рака, [249] но был связан со смертью более 50 пациентов, у которых он использовался как часть научно необоснованного лечения рака. [250]
Радиоизотопы цезия требуют особых мер предосторожности: неправильное обращение с источниками гамма-излучения цезия-137 может привести к выбросу этого радиоизотопа и радиационным поражениям. Пожалуй, самым известным случаем является авария в Гоянии в 1987 году, когда неправильно утилизированная система лучевой терапии из заброшенной клиники в городе Гояния , Бразилия, была найдена на свалке, а светящаяся соль цезия продана любопытным людям. , необразованные покупатели. Это привело к четырем смертельным случаям и серьезным травмам в результате радиационного воздействия. Вместе с цезием-134 , йодом-131 и стронцием-90 цезий-137 вошел в число изотопов, распределенных в результате чернобыльской катастрофы и представляющих наибольший риск для здоровья. [98] Радиоизотопы франция, по-видимому, также могут быть опасны из-за их высокой энергии распада и короткого периода полураспада, но ни один из них не был произведен в достаточно больших количествах, чтобы представлять какой-либо серьезный риск. [199]
{{cite journal}}: CS1 maint: numeric names: authors list (link)