Глюкоза – это сахар с молекулярной формулой C 6 H 12 O 6 . Глюкоза в целом является наиболее распространенным моносахаридом , [4] подкатегорией углеводов . Глюкоза в основном вырабатывается растениями и большинством водорослей в ходе фотосинтеза из воды и углекислого газа с использованием энергии солнечного света, где она используется для производства целлюлозы в клеточных стенках , самого распространенного углевода в мире. [5]
В энергетическом обмене глюкоза является важнейшим источником энергии во всех организмах . Глюкоза для метаболизма запасается в виде полимера , у растений главным образом в виде крахмала и амилопектина , а у животных - в виде гликогена . Глюкоза циркулирует в крови животных в виде сахара в крови . Природной формой глюкозы является d -глюкоза, тогда как ее стереоизомер l -глюкоза производится синтетически в сравнительно небольших количествах и менее биологически активен. [6] Глюкоза представляет собой моносахарид, содержащий шесть атомов углерода и альдегидную группу, и, следовательно, является альдогексозой . Молекула глюкозы может существовать как в открытой (ациклической), так и в кольцевой (циклической) форме. Глюкоза встречается в природе и в свободном состоянии содержится во фруктах и других частях растений. У животных глюкоза высвобождается в результате распада гликогена в процессе, известном как гликогенолиз .
Глюкоза в виде раствора сахара для внутривенного введения включена в Список основных лекарственных средств Всемирной организации здравоохранения . [7] Он также находится в списке в сочетании с хлоридом натрия (поваренной солью). [7]
Название глюкозы происходит от древнегреческого γλεῦκος ( gleûkos , «вино, сусло»), от γλυκύς ( glykýs , «сладкое»). [8] [9] Суффикс « -оза » представляет собой химический классификатор, обозначающий сахар.
Глюкозу впервые выделил из изюма в 1747 году немецкий химик Андреас Маргграф . [10] [11] Глюкоза была обнаружена в винограде другим немецким химиком – Иоганном Тобиасом Ловицем – в 1792 году и отличалась от тростникового сахара ( сахарозы ). Глюкоза — это термин, введенный Жаном Батистом Дюма в 1838 году и преобладающий в химической литературе. Фридрих Август Кекуле предложил термин декстроза (от латинского dexter , что означает «правый»), поскольку в водном растворе глюкозы плоскость линейно поляризованного света повернута вправо. Напротив, l-фруктоза (обычно называемая d -фруктозой) (кетогексоза) и l-глюкоза ( l -глюкоза) поворачивают линейно поляризованный свет влево. От более ранних обозначений, соответствующих вращению плоскости линейно поляризованного света ( d- и l -номенклатура), позже отказались в пользу d- и l -нотации , которая относится к абсолютной конфигурации асимметричного центра, наиболее удаленного от карбонильной группы. , и в соответствии с конфигурацией d- или l -глицеральдегида. [12] [13]
Поскольку глюкоза является основной потребностью многих организмов, правильное понимание ее химического состава и структуры во многом способствовало общему прогрессу органической химии . Это понимание возникло во многом в результате исследований Эмиля Фишера , немецкого химика, получившего Нобелевскую премию по химии 1902 года за свои открытия. [14] Синтез глюкозы установил структуру органического материала и, следовательно, стал первым окончательным подтверждением теорий Якобуса Хенрикуса ван 'т Хоффа о химической кинетике и расположении химических связей в углеродсодержащих молекулах. [15] Между 1891 и 1894 годами Фишер установил стереохимическую конфигурацию всех известных сахаров и правильно предсказал возможные изомеры , применив теорию Вант-Гоффа об асимметричных атомах углерода. Названия изначально относились к природным веществам. Их энантиомерам были присвоены одинаковые названия с введением систематических номенклатур с учетом абсолютной стереохимии (например, номенклатура Фишера, номенклатура д / л ).
За открытие метаболизма глюкозы Отто Мейерхоф получил Нобелевскую премию по физиологии и медицине в 1922 году. [16] Ганс фон Эйлер-Хельпин был удостоен Нобелевской премии по химии вместе с Артуром Харденом в 1929 году за «исследования ферментации глюкозы». сахара и их доля ферментов в этом процессе». [17] [18] В 1947 году Бернардо Уссей (за открытие роли гипофиза в метаболизме глюкозы и производных углеводов), а также Карл и Герти Кори (за открытие превращения гликогена из глюкозы) ) получил Нобелевскую премию по физиологии и медицине. [19] [20] [21] В 1970 году Луис Лелуар был удостоен Нобелевской премии по химии за открытие сахарных нуклеотидов, полученных из глюкозы, в биосинтезе углеводов. [22]
Глюкоза образует белые или бесцветные твердые вещества, хорошо растворимые в воде и уксусной кислоте , но плохо растворимые в метаноле и этаноле . Они плавятся при 146 °C (295 °F) ( α ) и 150 °C (302 °F) ( бета ), разлагаются, начиная с 188 °C (370 °F) с выделением различных летучих продуктов, в конечном итоге оставляя остаток углерод . [23] Значение pKa глюкозы составляет 12,16 при температуре 25 °C (77 °F) в воде. [24]
Имея шесть атомов углерода, он классифицируется как гексоза , подкатегория моносахаридов . d -Глюкоза — один из шестнадцати стереоизомеров альдогексозы . D - изомер , d -глюкоза, также известный как декстроза , широко встречается в природе, а L -изомер, l - глюкоза , — нет. Глюкозу можно получить путем гидролиза углеводов, таких как молочный сахар ( лактоза ), тростниковый сахар (сахароза), мальтоза , целлюлоза , гликоген и т. д. Декстрозу обычно производят из кукурузного крахмала в США и Японии, из картофельного и пшеничного крахмала в Европе. и из крахмала тапиоки в тропических регионах. [25] В производственном процессе используется гидролиз посредством обработки паром под давлением при контролируемом pH в струе с последующей ферментативной деполимеризацией. [26] Несвязанная глюкоза является одним из основных ингредиентов меда .

Глюкоза обычно присутствует в твердой форме в виде моногидрата с замкнутым пирановым кольцом (моногидрат α-глюкопиранозы, иногда менее точно известный как гидрат декстрозы). С другой стороны, в водном растворе он в небольшой степени имеет открытую цепь и присутствует преимущественно в виде α- или β- пиранозы , которые взаимно превращаются. Из водных растворов можно кристаллизовать три известные формы: α-глюкопиранозу, β-глюкопиранозу и моногидрат α-глюкопиранозы. [27] Глюкоза является строительным блоком дисахаридов лактозы и сахарозы (тростниковый или свекловичный сахар), олигосахаридов, таких как раффиноза , и полисахаридов, таких как крахмал , амилопектин , гликоген и целлюлоза . Температура стеклования глюкозы составляет 31 °C (88 °F), а константа Гордона–Тейлора (экспериментально определенная константа для прогнозирования температуры стеклования для различных массовых долей смеси двух веществ) [28] равна 4,5. . [29]

Форма глюкозы с открытой цепью составляет менее 0,02% молекул глюкозы в водном растворе в равновесии. [30] Остальное представляет собой одну из двух циклических полуацетальных форм. В форме с открытой цепью молекула глюкозы имеет открытую (в отличие от циклической ) неразветвленную основную цепь из шести атомов углерода, где C-1 является частью альдегидной группы H(C=O)- . Поэтому глюкозу также классифицируют как альдозу или альдогексозу . Альдегидная группа делает глюкозу редуцирующим сахаром , что дает положительную реакцию в тесте Фелинга .
В растворах форма глюкозы с открытой цепью (либо « D- », либо « L- ») существует в равновесии с несколькими циклическими изомерами , каждый из которых содержит кольцо атомов углерода, замкнутое одним атомом кислорода. Однако в водном растворе более 99% молекул глюкозы существуют в форме пиранозы . Форма с открытой цепью ограничена примерно 0,25%, а формы фуранозы существуют в незначительных количествах. Термины «глюкоза» и « D -глюкоза» обычно также используются для этих циклических форм. Кольцо возникает из формы с открытой цепью в результате внутримолекулярной реакции нуклеофильного присоединения между альдегидной группой (при C-1) и гидроксильной группой C-4 или C-5, образуя полуацетальную связь, -C(OH)H- О- .
Реакция между C-1 и C-5 дает шестичленную гетероциклическую систему, называемую пиранозой, которая представляет собой моносахаридный сахар (отсюда и «-оза»), содержащий производное пиранового скелета. (Намного более редкая) реакция между C-1 и C-4 дает пятичленное фуранозное кольцо, названное в честь циклического эфира фурана . В любом случае к каждому углероду в кольце присоединен один водород и один гидроксил, за исключением последнего углерода (C-4 или C-5), где гидроксил заменен остатком открытой молекулы (то есть -(C( CH 2 OH)HOH)-H или -(CHOH)-H соответственно).
Реакция замыкания цикла может дать два продукта, обозначенных «α-» и «β-». Когда молекула глюкопиранозы нарисована в проекции Хаворта , обозначение «α-» означает, что гидроксильная группа, присоединенная к C-1, и группа -CH 2 OH при C-5 лежат на противоположных сторонах плоскости кольца ( транс- расположение ), а «β-» означает, что они находятся на одной стороне плоскости ( цис- расположение). Следовательно, изомер D -глюкозы с открытой цепью дает четыре различных циклических изомера: α- D -глюкопиранозу, β- D -глюкопиранозу, α- D -глюкофуранозу и β- D -глюкофуранозу. Эти пять структур существуют в равновесии и взаимопревращаются, причем взаимное превращение происходит гораздо быстрее при кислотном катализе .

Другой изомер L -глюкозы с открытой цепью аналогичным образом дает начало четырем различным циклическим формам L -глюкозы, каждая из которых является зеркальным отражением соответствующей D -глюкозы.
Глюкопиранозное кольцо (α или β) может принимать несколько неплоских форм, аналогичных конформациям «кресло» и «лодочка» циклогексана . Точно так же глюкофуранозное кольцо может принимать несколько форм, аналогичных конформациям «конверта» циклопентана .
В твердом состоянии наблюдаются только формы глюкопиранозы.
Некоторые производные глюкофуранозы, такие как 1,2-O-изопропилиден-D-глюкофураноза, стабильны и могут быть получены в чистом виде в виде кристаллических твердых веществ. [31] [32] Например, реакция α-D-глюкозы с пара-толилбороновой кислотой H 3 C-(C 6 H 4 )-B(OH) 2 преобразует нормальное пиранозное кольцо с образованием 4-кратного сложного эфира α. -D-глюкофураноза-1,2:3,5-бис( п -толилборонат). [33]

Мутаротация состоит из временного изменения направления реакции образования кольца, что приводит к образованию открытой цепи с последующим реформированием кольца. На этапе замыкания кольца может использоваться группа -OH, отличная от той, которая воссоздана на этапе раскрытия (таким образом, переключение между формами пиранозы и фуранозы), или новая полуацетальная группа, созданная на C-1, может иметь ту же или противоположную направленность, что и исходная. (таким образом переключаясь между формами α и β). Таким образом, хотя форма с открытой цепью едва обнаруживается в растворе, она является важным компонентом равновесия.
Форма с открытой цепью термодинамически нестабильна и спонтанно изомеризуется в циклические формы. (Хотя реакция замыкания кольца теоретически может создавать четырех- или трехатомные кольца, они будут сильно напряжены и не наблюдаются на практике.) В растворах при комнатной температуре четыре циклических изомера взаимопревращаются в течение часов, в процессе, называемом мутаротацией . [34] Начиная с любых пропорций, смесь сходится к стабильному соотношению α:β 36:64. Соотношение α:β было бы 11:89, если бы не влияние аномерного эффекта . [35] Мутаротация происходит значительно медленнее при температуре, близкой к 0 ° C (32 ° F).
Будь то в воде или в твердой форме, d -(+)-глюкоза является правовращающей , то есть она будет вращать направление поляризованного света по часовой стрелке, если смотреть в сторону источника света. Эффект обусловлен хиральностью молекул, и действительно, зеркальный изомер, l -(-)-глюкоза, является левовращающим (вращает поляризованный свет против часовой стрелки) на такую же величину. Сила эффекта различна для каждого из пяти таутомеров .
Обратите внимание, что префикс d – не относится непосредственно к оптическим свойствам соединения. Это указывает на то, что хиральный центр C-5 имеет ту же направленность, что и у d -глицеральдегида (который был помечен так, потому что он правовращающий). Тот факт, что d -глюкоза обладает правовращающим действием, является совместным действием ее четырех хиральных центров, а не только С-5; и действительно, некоторые другие d -альдогексозы обладают левовращающими свойствами.
Превращение между двумя аномерами можно наблюдать в поляриметре, поскольку чистая α- d -глюкоза имеет удельный угол вращения +112,2° мл/(дм·г), чистая β- d -глюкоза +17,5° мл/(дм·г). ·г). [36] Когда равновесие достигается через определенное время за счет мутаротации, угол поворота составляет +52,7° мл/(дм·г). [36] При добавлении кислоты или основания это превращение значительно ускоряется. Уравновешивание происходит через альдегидную форму с открытой цепью.
В разбавленном гидроксиде натрия или других разбавленных основаниях моносахариды манноза , глюкоза и фруктоза взаимно превращаются (посредством превращения Лобри де Брюйна-Альберды-Ван Экенштейна ), так что формируется баланс между этими изомерами. Эта реакция протекает через эндиол :
Глюкоза – самый распространенный моносахарид. Глюкоза также является наиболее широко используемой альдогексозой в большинстве живых организмов. Одним из возможных объяснений этого является то, что глюкоза имеет меньшую склонность, чем другие альдогексозы, к неспецифической реакции с аминогруппами белков . [37] Эта реакция — гликирование — ухудшает или разрушает функцию многих белков, [37] например, гликированного гемоглобина . Низкую скорость гликирования глюкозы можно объяснить тем, что она имеет более стабильную циклическую форму по сравнению с другими альдогексозами, что означает, что она тратит меньше времени, чем в ее реакционноспособной форме с открытой цепью. [37] Причина того, что глюкоза имеет наиболее стабильную циклическую форму из всех альдогексоз, заключается в том, что ее гидроксильные группы (за исключением гидроксигруппы на аномерном углероде d -глюкозы) находятся в экваториальном положении . Предположительно, глюкоза является наиболее распространенным природным моносахаридом, поскольку она менее гликируется с белками, чем другие моносахариды. [37] [38] Другая гипотеза состоит в том, что глюкоза, являющаяся единственной d -альдогексозой, имеющей все пять гидрокси-заместителей в экваториальном положении в форме β- d -глюкозы, более доступна для химических реакций, [39] : 194, 199 , например, для этерификации [40] : 363 или образования ацеталя . [41] По этой причине d -глюкоза также является весьма предпочтительным строительным блоком природных полисахаридов (гликанов). Полисахариды, состоящие исключительно из глюкозы, называются глюканами .
Глюкоза вырабатывается растениями посредством фотосинтеза с использованием солнечного света, воды и углекислого газа и может использоваться всеми живыми организмами в качестве источника энергии и углерода. Однако большая часть глюкозы встречается не в свободной форме, а в виде ее полимеров, т.е. лактозы, сахарозы, крахмала и других, которые являются запасными энергетическими веществами, а также целлюлозы и хитина , которые являются компонентами клеточной стенки растений или грибов. и членистоногих соответственно. Эти полимеры, потребляемые животными, грибами и бактериями, разлагаются до глюкозы с помощью ферментов. Все животные также способны сами производить глюкозу из определенных предшественников по мере возникновения необходимости. Нейроны , клетки мозгового слоя почек и эритроциты зависят от глюкозы для производства энергии. [42] У взрослых людей содержится около 18 г (0,63 унции) глюкозы, [43] из которых около 4 г (0,14 унции) присутствует в крови. [44] Примерно 180–220 г (6,3–7,8 унций) глюкозы вырабатывается в печени взрослого человека за 24 часа. [43]
Многие из долгосрочных осложнений диабета (например, слепота , почечная недостаточность и периферическая нейропатия ), вероятно, обусловлены гликированием белков или липидов . [45] Напротив, регулируемое ферментами добавление сахаров к белку называется гликозилированием и имеет важное значение для функционирования многих белков. [46]
Поступившая в организм глюкоза первоначально связывается с рецептором сладкого вкуса на языке человека. Этот комплекс белков T1R2 и T1R3 позволяет идентифицировать глюкозосодержащие источники пищи. Глюкоза в основном поступает с пищей — около 300 г (11 унций) в день производится путем преобразования пищи [47] , но она также синтезируется из других метаболитов в клетках организма. У человека расщепление глюкозосодержащих полисахаридов происходит частично уже во время жевания посредством амилазы , содержащейся в слюне , а также мальтазы , лактазы и сахаразы на щеточной кайме тонкой кишки . Глюкоза является строительным блоком многих углеводов и может быть отделена от них с помощью определенных ферментов. Глюкозидазы , подгруппа гликозидаз, сначала катализируют гидролиз длинноцепочечных глюкозосодержащих полисахаридов, удаляя концевую глюкозу. В свою очередь, дисахариды в основном расщепляются специфическими гликозидазами до глюкозы. Названия разлагающих ферментов часто происходят от конкретных поли- и дисахаридов; в частности, для деградации полисахаридных цепей используются амилазы (названные в честь амилозы, компонента крахмала), целлюлазы (названные в честь целлюлозы), хитиназы (названные в честь хитина) и другие. Кроме того, для расщепления дисахаридов используются мальтаза, лактаза, сахараза, трегалаза и другие. У человека известно около 70 генов, кодирующих гликозидазы. Они участвуют в переваривании и расщеплении гликогена, сфинголипидов , мукополисахаридов и поли( АДФ-рибозы ). Люди не производят целлюлазы, хитиназы или трегалазы, но это делают бактерии в микробиоте кишечника .
Чтобы проникнуть в клеточные мембраны клеток и мембраны клеточных компартментов или выйти из них, глюкозе необходимы специальные транспортные белки из суперсемейства основных фасилитаторов . В тонком кишечнике (точнее, в тощей кишке ) [48] глюкоза попадает в кишечный эпителий с помощью транспортеров глюкозы [49] посредством вторичного активного механизма транспорта, называемого симпортом ионов натрия и глюкозы через котранспортер натрия/глюкозы. 1 (СГЛТ1). [50] Дальнейший перенос происходит на базолатеральной стороне эпителиальных клеток кишечника через транспортер глюкозы GLUT2 , [50] а также поглощение клетками печени , клетками почек, клетками островков Лангерганса , нейронами , астроцитами и таницитами . [51] Глюкоза поступает в печень через воротную вену и сохраняется там в виде клеточного гликогена. [52] В клетках печени он фосфорилируется глюкокиназой в положении 6 с образованием глюкозо -6-фосфата , который не может покинуть клетку. Глюкозо-6-фосфатаза может превращать глюкозо-6-фосфат обратно в глюкозу исключительно в печени, поэтому организм может поддерживать достаточную концентрацию глюкозы в крови. В других клетках поглощение происходит путем пассивного транспорта через один из 14 белков GLUT. [50] В других типах клеток фосфорилирование происходит посредством гексокиназы , после чего глюкоза больше не может диффундировать из клетки.
Переносчик глюкозы GLUT1 вырабатывается большинством типов клеток и имеет особое значение для нервных клеток и β-клеток поджелудочной железы . [50] GLUT3 высоко экспрессируется в нервных клетках. [50] Глюкоза из кровотока поглощается GLUT4 из мышечных клеток (скелетных мышц [53] и сердечной мышцы ) и жировых клеток . [54] GLUT14 экспрессируется исключительно в яичках . [55] Избыточная глюкоза расщепляется и превращается в жирные кислоты, которые сохраняются в виде триглицеридов . В почках глюкоза в моче абсорбируется через SGLT1 и SGLT2 в апикальных клеточных мембранах и передается через GLUT2 в базолатеральных клеточных мембранах. [56] Около 90% реабсорбции глюкозы в почках происходит через SGLT2 и около 3% через SGLT1. [57]
У растений и некоторых прокариот глюкоза — продукт фотосинтеза . [58] Глюкоза также образуется в результате распада полимерных форм глюкозы, таких как гликоген (у животных и грибов ) или крахмал (у растений). Расщепление гликогена называется гликогенолизом, расщепление крахмала — деградацией крахмала. [59]
Метаболический путь, который начинается с молекул, содержащих от двух до четырех атомов углерода (С), и заканчивается молекулой глюкозы, содержащей шесть атомов углерода, называется глюконеогенезом и встречается во всех живых организмах. Меньшие исходные материалы являются результатом других метаболических путей. В конечном счете почти все биомолекулы образуются в результате ассимиляции углекислого газа растениями и микробами в ходе фотосинтеза. [40] : 359 Свободная энергия образования α- d -глюкозы составляет 917,2 кДж/моль. [40] : 59 У человека глюконеогенез происходит в печени и почках, [60] а также в других типах клеток. В печени хранится около 150 г (5,3 унции) гликогена, в скелетных мышцах — около 250 г (8,8 унции). [61] Однако глюкоза, высвобождаемая в мышечных клетках при расщеплении гликогена, не может быть доставлена в кровоток, поскольку глюкоза фосфорилируется гексокиназой, а глюкозо-6-фосфатаза не экспрессируется для удаления фосфатной группы. В отличие от глюкозы, для глюкозо-6-фосфата нет транспортного белка . Глюконеогенез позволяет организму накапливать глюкозу из других метаболитов, включая лактат или определенные аминокислоты , потребляя при этом энергию. Клетки почечных канальцев также могут производить глюкозу.
Глюкозу также можно найти вне живых организмов в окружающей среде. Концентрация глюкозы в атмосфере определяется путем сбора проб с самолета и, как известно, варьируется от места к месту. Например, концентрации глюкозы в атмосферном воздухе внутреннего Китая колеблются от 0,8 до 20,1 пг/л, тогда как концентрации глюкозы в восточном прибрежном Китае колеблются от 10,3 до 142 пг/л. [62]
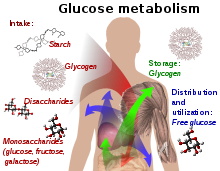
У человека глюкоза метаболизируется путем гликолиза [63] и пентозофосфатного пути. [64] Гликолиз используется всеми живыми организмами, [39] : 551 [65] с небольшими вариациями, и все организмы генерируют энергию за счет распада моносахаридов. [65] В дальнейшем ходе метаболизма он может полностью разлагаться посредством окислительного декарбоксилирования , цикла лимонной кислоты (синоним цикл Кребса ) и дыхательной цепи до воды и углекислого газа. Если для этого недостаточно кислорода, разложение глюкозы у животных происходит анаэробно до лактата посредством ферментации молочной кислоты и выделяется гораздо меньше энергии. Мышечный лактат попадает в печень через кровоток у млекопитающих, где происходит глюконеогенез ( цикл Кори ). При высоком запасе глюкозы метаболит ацетил-КоА из цикла Кребса также может использоваться для синтеза жирных кислот . [66] Глюкоза также используется для пополнения запасов гликогена в организме, который в основном содержится в печени и скелетных мышцах. Эти процессы регулируются гормонально .
У других живых организмов могут возникать и другие формы ферментации. Бактерия Escherichia coli может расти на питательных средах, содержащих глюкозу в качестве единственного источника углерода. [40] : 59 У некоторых бактерий, а в модифицированной форме также у архей, глюкоза расщепляется по пути Энтнера-Дудорова . [67]
Использование глюкозы в качестве источника энергии в клетках осуществляется посредством аэробного дыхания, анаэробного дыхания или ферментации. Первым этапом гликолиза является фосфорилирование глюкозы гексокиназой с образованием глюкозо-6-фосфата . Основная причина немедленного фосфорилирования глюкозы заключается в предотвращении ее диффузии из клетки, поскольку заряженная фосфатная группа предотвращает легкое прохождение глюкозо-6-фосфата через клеточную мембрану . [68] Кроме того, добавление высокоэнергетической фосфатной группы активирует глюкозу для последующего расщепления на более поздних стадиях гликолиза. В физиологических условиях эта первоначальная реакция необратима.
При анаэробном дыхании одна молекула глюкозы дает чистый прирост в размере двух молекул АТФ (четыре молекулы АТФ образуются во время гликолиза посредством фосфорилирования на уровне субстрата, но две требуются ферментам, используемым в этом процессе). [69] При аэробном дыхании молекула глюкозы гораздо более выгодна, поскольку генерируется максимальная чистая продукция 30 или 32 молекул АТФ (в зависимости от организма). [70]
Нажмите на гены, белки и метаболиты ниже, чтобы перейти к соответствующим статьям. [§ 1]
Опухолевые клетки часто растут сравнительно быстро и потребляют количество глюкозы, превышающее среднее, путем гликолиза [71] , что приводит к образованию лактата, конечного продукта ферментации у млекопитающих, даже в присутствии кислорода. Это называется эффектом Варбурга . Для повышенного поглощения глюкозы опухолями чрезмерно вырабатываются различные SGLT и GLUT. [72] [73]
В дрожжах этанол ферментируется при высоких концентрациях глюкозы, даже в присутствии кислорода (что обычно приводит к дыханию, а не к брожению). Это называется эффектом Крэбтри .
Глюкоза также может разлагаться с образованием углекислого газа абиотическим путем. Экспериментально было показано, что это происходит посредством окисления и гидролиза при 22 ° C и pH 2,5. [74]
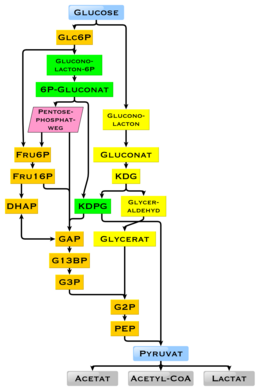
Глюкоза – повсеместное топливо в биологии . Он используется в качестве источника энергии в организмах, от бактерий до человека, посредством аэробного дыхания , анаэробного дыхания (у бактерий) или ферментации . Глюкоза является ключевым источником энергии человеческого организма посредством аэробного дыхания, обеспечивая около 3,75 килокалорий (16 килоджоулей ) пищевой энергии на грамм. [75] Расщепление углеводов (например, крахмала) приводит к образованию моно- и дисахаридов , большую часть которых составляет глюкоза. В результате гликолиза , а затем в реакциях цикла лимонной кислоты и окислительного фосфорилирования глюкоза окисляется с образованием углекислого газа и воды, выделяя энергию главным образом в форме АТФ . Реакция инсулина и другие механизмы регулируют концентрацию глюкозы в крови. Физиологическая калорийность глюкозы в зависимости от источника составляет 16,2 кДж/г [76] или 15,7 кДж/г (3,74 ккал/г). [77] Высокая доступность углеводов из биомассы растений привела к появлению в ходе эволюции, особенно у микроорганизмов, различных методов использования глюкозы для получения энергии и хранения углерода. Существуют различия, при которых конечный продукт больше не может использоваться для производства энергии. Наличие отдельных генов и их генных продуктов — ферментов — определяет возможные реакции. Метаболический путь гликолиза используется практически всеми живыми существами. Существенным отличием использования гликолиза является восстановление НАДФН в качестве восстановителя анаболизма , который в противном случае пришлось бы генерировать косвенно. [78]
Глюкоза и кислород снабжают мозг почти всей энергией [79] , поэтому их доступность влияет на психологические процессы. При низком уровне глюкозы нарушаются психологические процессы, требующие умственных усилий (например, самоконтроль , принятие решений, требующих усилий). [80] [81] [82] [83] В мозге, который зависит от глюкозы и кислорода как основных источников энергии, концентрация глюкозы обычно составляет от 4 до 6 мМ (5 мМ соответствует 90 мг/дл), [ 43] , но снижается до 2–3 мМ натощак. [84] Спутанность сознания возникает при концентрациях ниже 1 мМ и кома при более низких уровнях. [84]
Глюкоза в крови называется сахаром крови . Уровень сахара в крови регулируется глюкозосвязывающими нервными клетками гипоталамуса . [85] Кроме того, глюкоза в мозге связывается с рецепторами глюкозы системы вознаграждения в прилежащем ядре . [85] Связывание глюкозы с рецептором сладкого на языке вызывает высвобождение различных гормонов энергетического обмена либо через глюкозу, либо через другие сахара, что приводит к увеличению клеточного поглощения и снижению уровня сахара в крови. [86] Искусственные подсластители не снижают уровень сахара в крови. [86]
Содержание сахара в крови здорового человека в состоянии кратковременного голодания, например, после ночного голодания, составляет примерно от 70 до 100 мг/дл крови (от 4 до 5,5 мМ). В плазме крови измеренные значения примерно на 10–15% выше. Кроме того, значения в артериальной крови выше, чем концентрации в венозной крови, поскольку глюкоза всасывается в ткани при прохождении по капиллярному руслу . Также в капиллярной крови, которую часто используют для определения сахара в крови, значения иногда выше, чем в венозной крови. Содержание глюкозы в крови регулируется гормонами инсулином , инкретином и глюкагоном . [85] [87] Инсулин снижает уровень глюкозы, глюкагон повышает его. [43] Кроме того, гормоны адреналин , тироксин , глюкокортикоиды , соматотропин и адренокортикотропин приводят к повышению уровня глюкозы. [43] Существует также гормононезависимая регуляция, которая называется ауторегуляцией глюкозы. [88] После приема пищи концентрация сахара в крови увеличивается. Значения выше 180 мг/дл в венозной цельной крови являются патологическими и называются гипергликемией , значения ниже 40 мг/дл называются гипогликемией . [89] При необходимости глюкоза высвобождается в кровоток под действием глюкозо-6-фосфатазы из глюкозо-6-фосфата, происходящего из гликогена печени и почек, тем самым регулируя гомеостаз концентрации глюкозы в крови. [60] [42] У жвачных животных концентрация глюкозы в крови ниже (60 мг/дл у крупного рогатого скота и 40 мг/дл у овец ), поскольку углеводы в большей степени преобразуются микробиотой кишечника в короткоцепочечные жирные кислоты . [90]
Некоторое количество глюкозы преобразуется астроцитами в молочную кислоту , которая затем используется в качестве источника энергии клетками мозга ; некоторая часть глюкозы используется клетками кишечника и эритроцитами , а остальная часть достигает печени , жировой ткани и мышечных клеток, где всасывается и сохраняется в виде гликогена (под влиянием инсулина ). Гликоген клеток печени может превращаться в глюкозу и возвращаться в кровь при низком уровне инсулина или его отсутствии; Гликоген мышечных клеток не возвращается в кровь из-за недостатка ферментов. В жировых клетках глюкоза используется для запуска реакций, которые синтезируют некоторые типы жиров и имеют другие цели. Гликоген — это механизм «накопления энергии глюкозы» в организме, поскольку он гораздо более «экономичен по пространству» и менее реактивен, чем сама глюкоза.
Из-за своей важности для здоровья человека глюкоза является аналитом в тестах на глюкозу , которые являются обычными медицинскими анализами крови . [91] Прием пищи или голодание перед взятием образца крови влияет на анализ глюкозы в крови; Высокий уровень глюкозы в крови натощак может быть признаком предиабета или сахарного диабета . [92]
Гликемический индекс — это показатель скорости резорбции и преобразования в уровень глюкозы в крови из принятых углеводов, измеряемый как площадь под кривой уровня глюкозы в крови после потребления по сравнению с глюкозой (глюкоза определяется как 100). [93] Клиническое значение гликемического индекса является спорным, [93] [94] поскольку продукты с высоким содержанием жиров замедляют всасывание углеводов и снижают гликемический индекс, например мороженое. [94] Альтернативным показателем является инсулиновый индекс , [95] измеряемый как влияние потребления углеводов на уровень инсулина в крови. Гликемическая нагрузка — это показатель количества глюкозы, добавленной к уровню глюкозы в крови после потребления, основанный на гликемическом индексе и количестве потребляемой пищи.
Организмы используют глюкозу в качестве предшественника для синтеза ряда важных веществ. Крахмал, целлюлоза и гликоген («животный крахмал») представляют собой распространенные полимеры глюкозы (полисахариды). Некоторые из этих полимеров (крахмал или гликоген) служат запасами энергии, тогда как другие (целлюлоза и хитин , который производится из производного глюкозы) играют структурную роль. Олигосахариды глюкозы в сочетании с другими сахарами служат важными запасами энергии. К ним относятся лактоза, преобладающий сахар в молоке, который представляет собой дисахарид глюкозы-галактозы, и сахароза, еще один дисахарид, состоящий из глюкозы и фруктозы. Глюкоза также добавляется к определенным белкам и липидам в процессе, называемом гликозилированием . Зачастую это имеет решающее значение для их функционирования. Ферменты, которые соединяют глюкозу с другими молекулами, обычно используют фосфорилированную глюкозу для формирования новой связи путем ее соединения с разрывом глюкозо-фосфатной связи.
Помимо прямого использования в качестве мономера, глюкоза может расщепляться с целью синтеза множества других биомолекул. Это важно, поскольку глюкоза служит одновременно основным хранилищем энергии и источником органического углерода. Глюкоза может расщепляться и превращаться в липиды . Он также является предшественником синтеза других важных молекул, таких как витамин С (аскорбиновая кислота). В живых организмах глюкоза превращается в несколько других химических соединений, которые являются исходным материалом для различных метаболических путей . Среди них все другие моносахариды [96] , такие как фруктоза (по полиольному пути ), [50] манноза (эпимер глюкозы в положении 2), галактоза (эпимер в положении 4), фукоза, различные уроновые кислоты и аминокислоты. сахара производятся из глюкозы. [52] Помимо фосфорилирования до глюкозо-6-фосфата, которое является частью гликолиза, глюкоза может окисляться во время ее распада до глюконо-1,5-лактона. Глюкоза используется у некоторых бактерий в качестве строительного блока при биосинтезе трегалозы или декстрана , а у животных — как строительный блок гликогена. Глюкоза также может превращаться из бактериальной ксилозоизомеразы во фруктозу. Кроме того, метаболиты глюкозы производят все заменимые аминокислоты, сахарные спирты , такие как маннит и сорбит , жирные кислоты , холестерин и нуклеиновые кислоты . [96] Наконец, глюкоза используется в качестве строительного блока при гликозилировании белков до гликопротеинов , гликолипидов , пептидогликанов , гликозидов и других веществ (катализируемого гликозилтрансферазами ) и может быть отщеплена от них гликозидазами .
Диабет — это нарушение обмена веществ, при котором организм не может регулировать уровень глюкозы в крови либо из-за недостатка инсулина в организме, либо из-за неспособности клеток организма должным образом реагировать на инсулин. Каждая из этих ситуаций может быть вызвана устойчиво высоким уровнем глюкозы в крови вследствие истощения поджелудочной железы и резистентности к инсулину . Поджелудочная железа – орган, ответственный за секрецию гормонов инсулина и глюкагона. [97] Инсулин — это гормон, который регулирует уровень глюкозы, позволяя клеткам организма поглощать и использовать глюкозу. Без него глюкоза не может попасть в клетку и, следовательно, не может использоваться в качестве топлива для функций организма. [98] Если поджелудочная железа подвергается постоянному повышению уровня глюкозы в крови, инсулин-продуцирующие клетки поджелудочной железы могут быть повреждены, что приведет к нехватке инсулина в организме. Инсулинорезистентность возникает, когда поджелудочная железа пытается вырабатывать все больше и больше инсулина в ответ на постоянно повышенный уровень глюкозы в крови. В конце концов, остальная часть тела становится резистентной к инсулину, который вырабатывает поджелудочная железа, что требует большего количества инсулина для достижения того же эффекта снижения уровня глюкозы в крови и вынуждает поджелудочную железу вырабатывать еще больше инсулина, чтобы конкурировать с резистентностью. Эта негативная спираль способствует выгоранию поджелудочной железы и прогрессированию диабета.
Чтобы контролировать реакцию организма на сахароснижающую терапию, можно измерить уровень глюкозы. Мониторинг уровня глюкозы в крови может осуществляться несколькими методами, например, с помощью теста на глюкозу натощак, который измеряет уровень глюкозы в крови после 8 часов голодания. Другой тест — это 2-часовой тест на толерантность к глюкозе (GTT). Для этого теста человек проходит тест на глюкозу натощак, затем выпивает 75-граммовый напиток с глюкозой и проходит повторное тестирование. Этот тест измеряет способность организма человека перерабатывать глюкозу. Со временем уровень глюкозы в крови должен снизиться, поскольку инсулин позволяет ему поглощаться клетками и выходить из кровотока.

Люди с диабетом или другими заболеваниями, которые приводят к низкому уровню сахара в крови, часто имеют при себе небольшое количество сахара в различных формах. Одним из наиболее часто используемых видов сахара является глюкоза, часто в форме таблеток глюкозы (глюкоза, спрессованная в форму таблетки, иногда с одним или несколькими другими ингредиентами в качестве связующего вещества), леденца или пакета сахара .

Большинство пищевых углеводов содержат глюкозу либо в качестве единственного строительного блока (как в полисахаридах, крахмале и гликогене), либо вместе с другим моносахаридом (как в гетерополисахаридах, сахарозе и лактозе). [99] Несвязанная глюкоза является одним из основных ингредиентов меда. Глюкоза чрезвычайно распространена и была выделена из различных природных источников по всему миру, включая мужские шишки хвойного дерева Wollemia nobilis в Риме, [100] корни растений Ilex asprella в Китае, [101] и соломинки риса в Китае. Калифорния. [102]
Глюкозу производят в промышленности из крахмала путем ферментативного гидролиза с помощью глюкозамилазы или с использованием кислот . Ферментативный гидролиз в значительной степени вытеснил реакции гидролиза, катализируемые кислотами. [104] В результате получается глюкозный сироп (ферментативно с содержанием глюкозы более 90% в сухом веществе) [104] с годовым объемом производства во всем мире 20 миллионов тонн (по состоянию на 2011 год). [105] Это причина бывшего общего названия «крахмальный сахар». Амилазы чаще всего происходят из Bacillus licheniformis [106] или Bacillus subtilis (штамм MN-385) [106] , которые более термостабильны, чем первоначально используемые ферменты. [106] [107] Начиная с 1982 года пуллуланазы Aspergillus niger использовались в производстве глюкозного сиропа для превращения амилопектина в крахмал (амилозу), тем самым увеличивая выход глюкозы. [108] Реакцию проводят при pH = 4,6–5,2 и температуре 55–60 °C. [10] Кукурузный сироп содержит от 20% до 95% глюкозы в сухом веществе. [109] [110] Японская форма глюкозного сиропа « Мизуаме » изготавливается из сладкого картофеля или рисового крахмала. [111] Мальтодекстрин содержит около 20% глюкозы.
Многие сельскохозяйственные культуры могут использоваться в качестве источника крахмала. Кукуруза , [104] рис, [ 104 ] пшеница , [104] маниока , [104] картофель , [104] ячмень , [104] сладкий картофель, [112] кукурузная шелуха и саго — все они используются в различных частях мира. В Соединенных Штатах почти исключительно используется кукурузный крахмал (из кукурузы). Некоторая коммерческая глюкоза встречается в составе инвертного сахара — смеси глюкозы и фруктозы в соотношении примерно 1:1, получаемой из сахарозы. В принципе, целлюлозу можно гидролизовать до глюкозы, но этот процесс пока коммерчески непрактичен. [27]
В США в качестве источника глюкозы для производства изоглюкозы , представляющей собой смесь глюкозы и фруктозы, используется почти исключительно кукуруза (точнее, кукурузный сироп) , поскольку фруктоза обладает более высокой подслащивающей способностью – при той же физиологической калорийности в 374 килокалории. за 100 г. Ежегодное мировое производство изоглюкозы составляет 8 миллионов тонн (по состоянию на 2011 год). [105] При изготовлении кукурузного сиропа конечным продуктом является кукурузный сироп с высоким содержанием фруктозы (HFCS).

Глюкоза в основном используется для производства фруктозы и глюкозосодержащих продуктов. В пищевых продуктах он используется в качестве подсластителя и увлажнителя для увеличения объема и создания более мягкого вкуса . [104] Различные источники глюкозы, такие как виноградный сок (для вина) или солод (для пива), используются для ферментации до этанола при производстве алкогольных напитков . В большинстве безалкогольных напитков в США используется HFCS-55 (с содержанием фруктозы 55% в сухой массе), тогда как в большинстве других подслащенных HFCS продуктов питания в США используется HFCS-42 (с содержанием фруктозы 42% в сухой массе). ). [114] В Мексике, с другой стороны, безалкогольные напитки подслащиваются тростниковым сахаром, который обладает более высокой подслащивающей способностью. [115] Кроме того, сироп глюкозы используется, в частности, при производстве кондитерских изделий , таких как конфеты , ириски и помадка . [116] Типичными химическими реакциями глюкозы при нагревании в безводных условиях являются карамелизация и, в присутствии аминокислот, реакция Майяра .
Кроме того, различные органические кислоты могут быть получены биотехнологическим путем из глюкозы, например, путем ферментации с Clostridium thermoaceticum для получения уксусной кислоты , с Penicillium notatum для производства арабоаскорбиновой кислоты, с Rhizopus delemar для производства фумаровой кислоты , с Aspergillus niger для производства фумаровой кислоты. производство глюконовой кислоты , Candida brumptii для производства изолимонной кислоты , Aspergillus terreus для производства итаконовой кислоты , Pseudomonas fluorescens для производства 2-кетоглюконовой кислоты, Gluconobacter suboxydans для производства 5-кетоглюконовой кислоты, Aspergillus oryzae для производства койевой кислоты , с Lactobacillus delbrueckii для производства молочной кислоты , с Lactobacillus brevis для производства яблочной кислоты , с Propionibacter shermanii для производства пропионовой кислоты , с Pseudomonas aeruginosa для производства пировиноградной кислоты и с Gluconobacter suboxydans для производства винной кислоты . [117] [ необходимы дополнительные ссылки ] Недавно сообщалось о мощных биоактивных натуральных продуктах, таких как триптолид, которые ингибируют транскрипцию млекопитающих посредством ингибирования субъединицы XPB общего транскрипционного фактора TFIIH в качестве конъюгата глюкозы для воздействия на гипоксические раковые клетки с повышенным содержанием глюкозы. транспортное выражение. [118] В последнее время глюкоза получила коммерческое применение в качестве ключевого компонента «наборов», содержащих молочную кислоту и инсулин, предназначенных для индукции гипогликемии и гиперлактатемии для борьбы с различными видами рака и инфекциями. [119]
Когда молекулу глюкозы необходимо обнаружить в определенном положении в более крупной молекуле, проводят спектроскопию ядерного магнитного резонанса , рентгеноструктурный анализ или иммуноокрашивание лектина с использованием конъюгата репортерного фермента конканавалина А , который связывает только глюкозу или маннозу.
Эти реакции имеют лишь историческое значение:
Проба Фелинга – классический метод выявления альдоз. [120] Из-за мутаротации глюкоза всегда присутствует в небольшой степени в виде альдегида с открытой цепью. При добавлении реагентов Фелинга (раствора Фелинга (I) и раствора Фелинга (II)) альдегидная группа окисляется до карбоновой кислоты , а тартратный комплекс Cu 2+ восстанавливается до Cu + и образует осадок кирпично-красного цвета (Cu 2 О).
В тесте Толленса после добавления к раствору образца аммиачного AgNO 3 глюкоза восстанавливает Ag + до элементарного серебра . [121]
В тесте Барфоеда [122] к раствору испытуемого сахара добавляют раствор растворенного ацетата меди , ацетата натрия и уксусной кислоты и затем нагревают на водяной бане в течение нескольких минут. Глюкоза и другие моносахариды быстро окрашиваются в красноватый цвет и образуют красновато-коричневый оксид меди(I) (Cu 2 O).
Глюкоза, являясь редуцирующим сахаром, реагирует в тесте Нюландера . [123]
При нагревании разбавленного раствора гидроксида калия с глюкозой до 100°С появляется сильное красновато-коричневое окрашивание и карамельный запах. [124] Концентрированная серная кислота растворяет сухую глюкозу без почернения при комнатной температуре, образуя сахарную серную кислоту. [124] [ необходима проверка ] В дрожжевом растворе алкогольное брожение производит углекислый газ в соотношении 2,0454 молекулы глюкозы на одну молекулу CO 2 . [124] Глюкоза образует черную массу с хлоридом олова . [124] В аммиачном растворе серебра глюкоза (а также лактоза и декстрин) приводит к отложению серебра. В аммиачном растворе ацетата свинца в присутствии глюкозы образуются гликозиды свинца, которые при варке становятся менее растворимыми и становятся коричневыми. [124] В аммиачном растворе меди желтый гидрат оксида меди образуется с глюкозой при комнатной температуре, а красный оксид меди образуется при кипячении (то же самое с декстрином, за исключением аммиачного раствора ацетата меди). [124] При использовании реактива Хагера глюкоза при кипячении образует оксид ртути . [124] Щелочной раствор висмута используется для осаждения элементарного черно-коричневого висмута глюкозой. [124] Глюкоза, кипяченная в растворе молибдата аммония, окрашивает раствор в синий цвет. Раствор с индигокармином и карбонатом натрия окрашивается при кипячении с глюкозой. [124]
В концентрированных растворах глюкозы с низкой долей других углеводов ее концентрацию можно определить поляриметром. Для сахарных смесей концентрацию можно определить с помощью рефрактометра , например, при определении Охсле в процессе производства вина.
Фермент глюкозооксидаза (GOx) превращает глюкозу в глюконовую кислоту и перекись водорода, потребляя при этом кислород. Другой фермент, пероксидаза, катализирует хромогенную реакцию (реакцию Триндера) [125] фенола с 4 -аминоантипирином с образованием пурпурного красителя.
Метод тест-полосок использует вышеупомянутое ферментативное превращение глюкозы в глюконовую кислоту с образованием перекиси водорода. Реагенты иммобилизуются на полимерной матрице, так называемой тест-полоске, которая принимает более или менее интенсивный цвет. Это можно измерить рефлектометрически при длине волны 510 нм с помощью портативного фотометра на основе светодиодов. Это позволяет обычным специалистам определять уровень сахара в крови. Помимо реакции фенола с 4-аминоантипирином разработаны новые хромогенные реакции, позволяющие проводить фотометрию при более высоких длинах волн (550 нм, 750 нм). [126]
Электроанализ глюкозы также основан на упомянутой выше ферментативной реакции. Полученную перекись водорода можно количественно определить амперометрически путем анодного окисления при потенциале 600 мВ. [127] GOx иммобилизуют на поверхности электрода или в мембране, расположенной рядом с электродом. В электродах используются драгоценные металлы, такие как платина или золото, а также электроды из углеродных нанотрубок, которые, например, легированы бором. [128] Нанопроволоки Cu–CuO также используются в качестве безэнзимных амперометрических электродов, предел обнаружения которых достигает 50 мкмоль/л. [129] Особенно многообещающим методом является так называемая «ферментатная проводка», при которой электрон, текущий во время окисления, переносится по молекулярной проволоке непосредственно от фермента к электроду. [130]
Существует множество других химических сенсоров для измерения глюкозы. [131] [132] Учитывая важность анализа глюкозы в науках о жизни, также были разработаны многочисленные оптические зонды для сахаридов на основе использования бороновых кислот, [133] которые особенно полезны для внутриклеточных сенсорных применений, где другие (оптические) методы не применимы или могут использоваться лишь условно. Помимо органических производных бороновой кислоты, которые часто высокоспецифично связываются с 1,2-диольными группами сахаров, существуют также другие концепции зондов, классифицированные по функциональным механизмам, которые используют селективные глюкозосвязывающие белки (например, конканавалин А) в качестве рецептора. . Кроме того, были разработаны методы, которые косвенно определяют концентрацию глюкозы через концентрацию продуктов метаболизма, например, путем потребления кислорода с использованием флуоресцентно-оптических датчиков. [134] Наконец, существуют концепции, основанные на ферментах, которые используют собственное поглощение или флуоресценцию (флуоресцентно-меченных) ферментов в качестве репортеров. [131]
Глюкозу можно определить количественно с помощью йодометрии меди. [135]
В частности, для анализа сложных смесей, содержащих глюкозу, например в меде, часто используются хроматографические методы, такие как высокоэффективная жидкостная хроматография и газовая хроматография [135] в сочетании с масс-спектрометрией . [136] [137] Принимая во внимание соотношение изотопов, с помощью этих методов также можно надежно обнаружить фальсификацию меда добавлением сахара. [138] Обычно используется дериватизация с использованием реагентов силилирования. [139] Кроме того, можно количественно определить пропорции ди- и трисахаридов.
Поглощение глюкозы клетками организмов измеряют с помощью 2-дезокси-D-глюкозы или фтордезоксиглюкозы . [84] ( 18 F)фтордезоксиглюкоза используется в качестве индикатора в позитронно-эмиссионной томографии в онкологии и неврологии, [140] где она является, безусловно, наиболее часто используемым диагностическим агентом. [141]
{{cite book}}: |journal=игнорируется ( помощь )