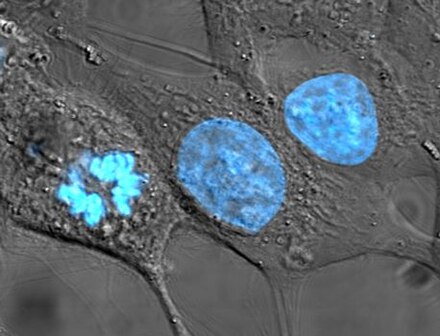
Ядро клетки (от лат. nucleus или nuculeus 'ядро, семя'; мн. ч .: nuclei ) — это связанная с мембраной органелла, обнаруженная в эукариотических клетках . Эукариотические клетки обычно имеют одно ядро, но некоторые типы клеток, такие как эритроциты млекопитающих , не имеют ядер, а некоторые другие, включая остеокласты, имеют много ядер . Основными структурами, составляющими ядро, являются ядерная оболочка , двойная мембрана, которая охватывает всю органеллу и изолирует ее содержимое от клеточной цитоплазмы ; и ядерный матрикс , сеть внутри ядра, которая добавляет механическую поддержку.
Ядро клетки содержит почти весь геном клетки . Ядерная ДНК часто организована в несколько хромосом — длинных цепей ДНК, усеянных различными белками , такими как гистоны , которые защищают и организуют ДНК. Гены в этих хромосомах структурированы таким образом, чтобы способствовать клеточной функции. Ядро поддерживает целостность генов и контролирует деятельность клетки, регулируя экспрессию генов .
Поскольку ядерная оболочка непроницаема для крупных молекул , ядерные поры необходимы для регулирования ядерного транспорта молекул через оболочку. Поры пересекают обе ядерные мембраны, обеспечивая канал , по которому более крупные молекулы должны активно транспортироваться белками-переносчиками, обеспечивая при этом свободное перемещение малых молекул и ионов . Перемещение крупных молекул, таких как белки и РНК, через поры необходимо как для экспрессии генов, так и для поддержания хромосом. Хотя внутренняя часть ядра не содержит никаких связанных с мембраной субкомпартментов, существует ряд ядерных телец , состоящих из уникальных белков, молекул РНК и определенных частей хромосом. Самым известным из них является ядрышко , участвующее в сборке рибосом .

Ядро клетки содержит большую часть генетического материала клетки в форме множественных линейных молекул ДНК, организованных в структуры, называемые хромосомами . Каждая клетка человека содержит примерно два метра ДНК. [1] : 405 В течение большей части клеточного цикла они организованы в комплекс ДНК-белок, известный как хроматин , и во время деления клетки можно увидеть, как хроматин образует четко определенные хромосомы, знакомые по кариотипу . Небольшая часть генов клетки находится вместо этого в митохондриях . [1] : 438
Существует два типа хроматина. Эухроматин — это менее компактная форма ДНК, содержащая гены, которые часто экспрессируются клеткой. [2] Другой тип, гетерохроматин , представляет собой более компактную форму и содержит ДНК, которая редко транскрибируется. Эта структура далее подразделяется на факультативный гетерохроматин , состоящий из генов, которые организованы как гетерохроматин только в определенных типах клеток или на определенных стадиях развития, и конститутивный гетерохроматин , состоящий из структурных компонентов хромосом, таких как теломеры и центромеры . [3] Во время интерфазы хроматин организуется в отдельные дискретные участки, [4] называемые территориями хромосом . [5] Активные гены, которые обычно находятся в эухроматиновой области хромосомы, как правило, располагаются по направлению к границе территории хромосомы. [6]
Антитела к определенным типам организации хроматина, в частности, нуклеосомам , были связаны с рядом аутоиммунных заболеваний , таких как системная красная волчанка . [7] Они известны как антинуклеарные антитела (ANA) и также наблюдались совместно с рассеянным склерозом как часть общей дисфункции иммунной системы. [8]
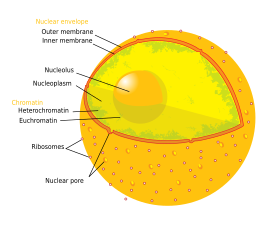
Ядро содержит почти всю ДНК клетки , окруженное сетью волокнистых промежуточных нитей , называемых ядерным матриксом , и окутано двойной мембраной, называемой ядерной оболочкой . Ядерная оболочка отделяет жидкость внутри ядра, называемую нуклеоплазмой , от остальной части клетки. Размер ядра коррелирует с размером клетки, и это соотношение наблюдается для ряда типов и видов клеток. [9] У эукариот ядро во многих клетках обычно занимает 10% объема клетки. [10] : 178 Ядро является самой большой органеллой в клетках животных. [11] : 12 В клетках человека диаметр ядра составляет приблизительно шесть микрометров (мкм). [10] : 179

Ядерная оболочка состоит из двух мембран , внутренней и внешней ядерной мембраны , перфорированных ядерными порами . [10] : 649 Вместе эти мембраны служат для отделения генетического материала клетки от остального содержимого клетки и позволяют ядру поддерживать среду, отличную от остальной части клетки. Несмотря на их близкое расположение вокруг большей части ядра, две мембраны существенно различаются по форме и содержимому. Внутренняя мембрана окружает ядерное содержимое, обеспечивая его определяющий край. [11] : 14 Встроенные во внутреннюю мембрану различные белки связывают промежуточные филаменты, которые придают ядру его структуру. [10] : 649 Внешняя мембрана охватывает внутреннюю мембрану и является продолжением соседней мембраны эндоплазматического ретикулума . [10] : 649 Как часть мембраны эндоплазматического ретикулума, внешняя ядерная мембрана усеяна рибосомами , которые активно транслируют белки через мембрану. [10] : 649 Пространство между двумя мембранами называется перинуклеарным пространством и является продолжением просвета эндоплазматического ретикулума . [10] : 649
В ядерной оболочке млекопитающих имеется от 3000 до 4000 комплексов ядерных пор (NPC), пронизывающих оболочку. [10] : 650 Каждый NPC содержит восьмикратно симметричную кольцевую структуру в месте слияния внутренней и внешней мембран. [12] Количество NPC может значительно различаться в зависимости от типа клеток; в небольших глиальных клетках их всего около нескольких сотен, а в крупных клетках Пуркинье — около 20 000. [10] : 650 NPC обеспечивает избирательный транспорт молекул между нуклеоплазмой и цитозолем . [13] Комплекс ядерных пор состоит примерно из тридцати различных белков, известных как нуклеопорины . [10] : 649 Молекулярная масса пор составляет около 60–80 миллионов дальтон , и они состоят примерно из 50 (у дрожжей ) до нескольких сотен белков (у позвоночных ). [11] : 622–4 Поры имеют общий диаметр 100 нм; однако зазор, через который свободно диффундируют молекулы, составляет всего около 9 нм в ширину из-за наличия регуляторных систем в центре поры. Этот размер избирательно позволяет проходить небольшим водорастворимым молекулам, предотвращая при этом ненадлежащее проникновение или выход из ядра более крупных молекул, таких как нуклеиновые кислоты и более крупные белки. Вместо этого эти крупные молекулы должны активно транспортироваться в ядро. К кольцу прикреплена структура, называемая ядерной корзиной , которая простирается в нуклеоплазму, и ряд нитевидных расширений, которые достигают цитоплазмы. Обе структуры служат для опосредования связывания с ядерными транспортными белками. [1] : 509–10
Большинство белков, рибосомальных субъединиц и некоторые РНК транспортируются через поровые комплексы в процессе, опосредованном семейством транспортных факторов, известных как кариоферины . Те кариоферины, которые опосредуют движение в ядро, также называются импортинами, тогда как те, которые опосредуют движение из ядра, называются экспортинами. Большинство кариоферинов напрямую взаимодействуют со своим грузом, хотя некоторые используют адаптерные белки . [14] Стероидные гормоны, такие как кортизол и альдостерон , а также другие небольшие жирорастворимые молекулы, участвующие в межклеточной сигнализации , могут диффундировать через клеточную мембрану в цитоплазму, где они связывают ядерные рецепторные белки, которые транспортируются в ядро. Там они служат факторами транскрипции , когда связаны со своим лигандом ; в отсутствие лиганда многие такие рецепторы функционируют как гистондеацетилазы , которые подавляют экспрессию генов. [1] : 488
В клетках животных две сети промежуточных филаментов обеспечивают ядру механическую поддержку: ядерная пластинка образует организованную сетку на внутренней поверхности оболочки, в то время как менее организованная поддержка обеспечивается на цитозольной поверхности оболочки. Обе системы обеспечивают структурную поддержку ядерной оболочки и места крепления для хромосом и ядерных пор. [15]
Ядерная пластинка в основном состоит из белков ламинов . Как и все белки, ламины синтезируются в цитоплазме и затем транспортируются внутрь ядра, где они собираются перед включением в существующую сеть ядерной пластинки. [16] [17] Ламины, обнаруженные на цитозольной поверхности мембраны, такие как эмерин и несприн , связываются с цитоскелетом, обеспечивая структурную поддержку. Ламины также обнаруживаются внутри нуклеоплазмы, где они образуют другую регулярную структуру, известную как нуклеоплазматическая вуаль , [18] [19], которая видна с помощью флуоресцентной микроскопии . Фактическая функция вуали не ясна, хотя она исключена из ядрышка и присутствует во время интерфазы . [20] Структуры ламинов, которые составляют вуаль, такие как LEM3 , связывают хроматин, и нарушение их структуры подавляет транскрипцию генов, кодирующих белки. [21]
Как и компоненты других промежуточных нитей, мономер ламина содержит альфа-спиральный домен, используемый двумя мономерами для скручивания друг вокруг друга, образуя димерную структуру, называемую спиральной спиралью . Две из этих димерных структур затем соединяются бок о бок в антипараллельном расположении, образуя тетрамер , называемый протофиламентом . Восемь из этих протофиламентов образуют боковое расположение, которое скручивается, образуя веревкообразную нить . Эти нити могут собираться или разбираться динамическим образом, что означает, что изменения длины нити зависят от конкурирующих скоростей добавления и удаления нити. [15]
Мутации в генах ламина, приводящие к дефектам в сборке филаментов, вызывают группу редких генетических расстройств, известных как ламинопатии . Наиболее известная ламинопатия — это семейство заболеваний, известных как прогерия , которое вызывает преждевременное старение у людей с этим заболеванием. Точный механизм, посредством которого связанные биохимические изменения приводят к старческому фенотипу, не совсем понятен. [22]
Ядрышко является самой большой из дискретных, густо окрашенных, безмембранных структур, известных как ядерные тельца, обнаруженные в ядре. Оно формируется вокруг тандемных повторов рДНК , ДНК, кодирующей рибосомальную РНК (рРНК). Эти области называются ядрышковыми организаторскими областями (ЯОР). Основные роли ядрышка заключаются в синтезе рРНК и сборке рибосом . Структурная сплоченность ядрышка зависит от его активности, поскольку сборка рибосом в ядрышке приводит к временной ассоциации ядрышковых компонентов, облегчая дальнейшую сборку рибосом и, следовательно, дальнейшую ассоциацию. Эта модель подтверждается наблюдениями, что инактивация рДНК приводит к смешиванию ядрышковых структур. [23]
На первом этапе сборки рибосомы белок, называемый РНК-полимеразой I, транскрибирует рДНК, которая образует большой предшественник пре-рРНК. Он расщепляется на две большие субъединицы рРНК – 5.8S и 28S и небольшую субъединицу рРНК 18S . [10] : 328 [24] Транскрипция, посттранскрипционная обработка и сборка рРНК происходят в ядрышке с помощью малых молекул ядрышковой РНК (snoRNA), некоторые из которых получены из сплайсированных интронов из матричных РНК, кодирующих гены, связанные с функцией рибосомы. Собранные рибосомные субъединицы являются крупнейшими структурами, проходящими через ядерные поры . [1] : 526
При наблюдении под электронным микроскопом можно увидеть, что ядрышко состоит из трех различимых областей: самые внутренние фибриллярные центры (FC), окруженные плотным фибриллярным компонентом (DFC) (содержащим фибрилларин и нуклеолин ), который, в свою очередь, граничит с гранулярным компонентом (GC) (содержащим белок нуклеофосмин ). Транскрипция рДНК происходит либо в FC, либо на границе FC-DFC, и, следовательно, когда транскрипция рДНК в клетке увеличивается, обнаруживается больше FC. Большая часть расщепления и модификации рРНК происходит в DFC, в то время как последние этапы, включающие сборку белка на рибосомных субъединицах, происходят в GC. [24]
Спеклы — это субъядерные структуры, обогащенные факторами сплайсинга премессенджерной РНК и расположенные в интерхроматиновых областях нуклеоплазмы клеток млекопитающих. [25] На уровне флуоресцентного микроскопа они выглядят как нерегулярные, точечные структуры, которые различаются по размеру и форме, а при исследовании с помощью электронного микроскопа они видны как кластеры интерхроматиновых гранул . Спеклы — это динамические структуры, и как их белковые, так и РНК-белковые компоненты могут непрерывно циклически перемещаться между спеклами и другими ядерными локациями, включая активные сайты транскрипции. Спеклы могут работать с p53 как усилители активности генов для непосредственного усиления активности определенных генов. Более того, ассоциированные со спеклами и неассоциированные с генами p53 мишени функционально различны. [26]
Исследования состава, структуры и поведения спеклов предоставили модель для понимания функциональной компартментализации ядра и организации аппарата экспрессии генов [27], сплайсинга snRNPs [28] [29] и других белков сплайсинга, необходимых для обработки пре-мРНК. [27] Из-за меняющихся потребностей клетки состав и расположение этих телец изменяются в соответствии с транскрипцией и регуляцией мРНК посредством фосфорилирования специфических белков. [30] Сплайсинговые спеклы также известны как ядерные спеклы (ядерные спеклы), отсеки факторов сплайсинга (отделения SF), кластеры интерхроматиновых гранул (IGC) и B-снурпосомы . [31] B-снурпосомы обнаружены в ядрах ооцитов амфибий и в эмбрионах Drosophila melanogaster . B-снурпосомы появляются отдельно или прикрепленными к тельцам Кахаля на электронных микрофотографиях ядер амфибий. [32] Первоначально считалось, что ядерные спеклы являются местами хранения факторов сплайсинга [33] , однако более позднее исследование показало, что организация генов и субстратов пре-мРНК вблизи спеклов увеличивает кинетическую эффективность сплайсинга пре-мРНК, в конечном итоге повышая уровни белка за счет модуляции сплайсинга [34] .

Ядро обычно содержит от одной до десяти компактных структур, называемых тельцами Кахаля или спиральными тельцами (СТ), диаметр которых составляет от 0,2 мкм до 2,0 мкм в зависимости от типа и вида клеток. [35] При рассмотрении под электронным микроскопом они напоминают клубки спутанных нитей [36] и представляют собой плотные очаги распределения белка коилина . [37] СТ участвуют в ряде различных ролей, связанных с процессингом РНК, в частности, в созревании малой ядрышковой РНК (мякРНК) и малой ядерной РНК (мяРНК), а также в модификации мРНК гистонов. [35]
Похожие на тельца Кахаля, Близнецы телец Кахаля, или драгоценные камни, чье название происходит от созвездия Близнецов в связи с их близкими «близнецовыми» отношениями с CB. Драгоценные камни похожи по размеру и форме на CB, и фактически практически неразличимы под микроскопом. [37] В отличие от CB, драгоценные камни не содержат малых ядерных рибонуклеопротеинов (snRNP), но содержат белок, называемый выживанием двигательного нейрона (SMN), функция которого связана с биогенезом snRNP. Считается, что драгоценные камни помогают CB в биогенезе snRNP, [38] хотя также было высказано предположение на основании микроскопических данных, что CB и драгоценные камни являются различными проявлениями одной и той же структуры. [37] Более поздние ультраструктурные исследования показали, что драгоценные камни являются близнецами телец Кахаля с разницей в компоненте коилина; тельца Кахаля SMN-положительны и коилин-положительны, а драгоценные камни SMN-положительны и коилин-отрицательны. [39]
Помимо ядерных телец, впервые описанных Сантьяго Рамоном-и-Кахалем выше (например, ядрышко, ядерные спеклы, тельца Кахаля), ядро содержит ряд других ядерных телец. К ним относятся полиморфная интерфазная кариосомная ассоциация (PIKA), тельца промиелоцитарного лейкоза (PML) и параспеклы . Хотя о некоторых из этих доменов известно немного, они важны тем, что показывают, что нуклеоплазма не является однородной смесью, а скорее содержит организованные функциональные субдомены. [41]
Другие субъядерные структуры появляются как часть аномальных патологических процессов. Например, наличие небольших внутриядерных стержней было отмечено в некоторых случаях немалиновой миопатии . Это состояние обычно возникает из-за мутаций в актине , а сами стержни состоят из мутантного актина, а также других цитоскелетных белков. [43]
Домены PIKA, или полиморфные интерфазные кариосомные ассоциации, были впервые описаны в микроскопических исследованиях в 1991 году. Их функция остается неясной, хотя считалось, что они не связаны с активной репликацией ДНК, транскрипцией или процессингом РНК. [44] Было обнаружено, что они часто ассоциируются с дискретными доменами, определяемыми плотной локализацией фактора транскрипции PTF, который способствует транскрипции малой ядерной РНК (мяРНК). [45]
Белок промиелоцитарного лейкоза (ядерные тельца ПМЛ) — это сферические тельца, разбросанные по всей нуклеоплазме, размером около 0,1–1,0 мкм. Они известны под рядом других названий, включая ядерный домен 10 (ND10), тельца Кремера и онкогенные домены ПМЛ. [46] Ядерные тельца ПМЛ названы в честь одного из их основных компонентов — белка промиелоцитарного лейкоза (ПМЛ). Они часто встречаются в ядре вместе с тельцами Кахаля и тельцами расщепления. [41] Мыши ПМЛ-/-, которые не способны создавать ядерные тельца ПМЛ, развиваются нормально без очевидных болезненных эффектов, показывая, что ядерные тельца ПМЛ не требуются для большинства важных биологических процессов. [47]
Обнаруженные Фоксом и соавторами в 2002 году, параспеклы представляют собой нерегулярные по форме компартменты в межхроматиновом пространстве ядра. [48] Впервые описанные в клетках HeLa, где их обычно 10–30 на ядро, [49] теперь известно, что параспеклы также существуют во всех первичных клетках человека, трансформированных клеточных линиях и тканевых срезах. [50] Их название происходит от их распределения в ядре; «пара» является сокращением от «параллельный», а «спеклы» относятся к сплайсинговым спеклам, к которым они всегда находятся в непосредственной близости. [49]
Параспеклы секвестрируют ядерные белки и РНК и, таким образом, по-видимому, функционируют как молекулярная губка [51] , которая участвует в регуляции экспрессии генов. [52] Кроме того, параспеклы являются динамическими структурами, которые изменяются в ответ на изменения клеточной метаболической активности. Они зависят от транскрипции [48] , и при отсутствии транскрипции РНК Pol II параспекл исчезает, а все его связанные белковые компоненты (PSP1, p54nrb, PSP2, CFI(m)68 и PSF) образуют полумесяцеобразный перинуклеолярный колпачок в ядрышке. Это явление демонстрируется во время клеточного цикла. В клеточном цикле параспеклы присутствуют во время интерфазы и во время всего митоза, за исключением телофазы . Во время телофазы, когда образуются два дочерних ядра, транскрипция РНК Pol II отсутствует, поэтому белковые компоненты вместо этого образуют перинуклеолярный колпачок. [50]
Перихроматиновые фибриллы видны только под электронным микроскопом. Они расположены рядом с транскрипционно активным хроматином и, как предполагается, являются участками активной пре-мРНК -обработки. [33]
Кластосомы — это небольшие ядерные тельца (0,2–0,5 мкм), которые описываются как имеющие толстую кольцевую форму из-за периферической капсулы вокруг этих тел. [40] Это название происходит от греческого klastos , сломанный, и soma , тело. [40] Кластосомы обычно не присутствуют в нормальных клетках, что затрудняет их обнаружение. Они образуются в условиях высокой протеолитической активности внутри ядра и разрушаются при снижении активности или если клетки обрабатываются ингибиторами протеасом . [40] [53] Недостаток кластосом в клетках указывает на то, что они не требуются для функционирования протеасом . [54] Было также показано, что осмотический стресс вызывает образование кластосом. [55] Эти ядерные тельца содержат каталитические и регуляторные субъединицы протеасомы и ее субстраты, что указывает на то, что кластосомы являются местами для разрушения белков. [54]
Ядро обеспечивает место для генетической транскрипции , которое отделено от места трансляции в цитоплазме, что позволяет осуществлять уровни регуляции генов , недоступные прокариотам . Основная функция клеточного ядра — контролировать экспрессию генов и опосредовать репликацию ДНК во время клеточного цикла. [1] : 171
Ядерная оболочка позволяет контролировать содержимое ядра и отделяет его от остальной цитоплазмы, где это необходимо. Это важно для контроля процессов по обе стороны ядерной мембраны: в большинстве случаев, когда цитоплазматический процесс необходимо ограничить, ключевой участник удаляется в ядро, где он взаимодействует с факторами транскрипции, чтобы подавить выработку определенных ферментов в пути. Этот регуляторный механизм происходит в случае гликолиза , клеточного пути расщепления глюкозы для получения энергии. Гексокиназа — это фермент, ответственный за первый этап гликолиза, образующий глюкозо-6-фосфат из глюкозы. При высоких концентрациях фруктозо-6-фосфата , молекулы, которая позже образуется из глюкозо-6-фосфата, регуляторный белок удаляет гексокиназу в ядро, [56] , где она образует комплекс транскрипционного репрессора с ядерными белками, чтобы снизить экспрессию генов, участвующих в гликолизе. [57]
Для того чтобы контролировать, какие гены транскрибируются, клетка отделяет некоторые белки факторов транскрипции, ответственные за регулирование экспрессии генов, от физического доступа к ДНК до тех пор, пока они не будут активированы другими сигнальными путями. Это предотвращает даже низкие уровни ненадлежащей экспрессии генов. Например, в случае генов, контролируемых NF-κB , которые участвуют в большинстве воспалительных реакций, транскрипция индуцируется в ответ на сигнальный путь, такой как инициируемый сигнальной молекулой TNF-α , связывается с рецептором клеточной мембраны, что приводит к набору сигнальных белков и в конечном итоге активирует фактор транскрипции NF-κB. Сигнал ядерной локализации на белке NF-κB позволяет ему транспортироваться через ядерную пору в ядро, где он стимулирует транскрипцию целевых генов. [15]
Компартментализация позволяет клетке предотвратить трансляцию несплайсированной мРНК. [58] Эукариотическая мРНК содержит интроны, которые должны быть удалены перед трансляцией для получения функциональных белков. Сплайсинг происходит внутри ядра, прежде чем мРНК может быть доступна рибосомам для трансляции. Без ядра рибосомы транслировали бы недавно транскрибированную (необработанную) мРНК, что привело бы к неправильно сформированным и нефункциональным белкам. [1] : 108–15
Основная функция клеточного ядра — контролировать экспрессию генов и опосредовать репликацию ДНК во время клеточного цикла. [1] : 171 Было обнаружено, что репликация происходит локализованным образом в клеточном ядре. В S-фазе интерфазы клеточного цикла происходит репликация. Вопреки традиционному взгляду на перемещение репликационных вилок вдоль застойной ДНК, возникла концепция репликационных фабрик , которая означает, что репликационные вилки концентрируются в некоторых иммобилизованных «фабричных» областях, через которые нити ДНК-матрицы проходят как конвейерные ленты. [59]

Экспрессия гена сначала включает транскрипцию, в которой ДНК используется в качестве шаблона для производства РНК. В случае генов, кодирующих белки, эта РНК, произведенная в этом процессе, является информационной РНК (мРНК), которая затем должна быть транслирована рибосомами для образования белка. Поскольку рибосомы расположены вне ядра, произведенная мРНК должна быть экспортирована. [60]
Поскольку ядро является местом транскрипции, оно также содержит множество белков, которые либо напрямую опосредуют транскрипцию, либо участвуют в регуляции этого процесса. К этим белкам относятся геликазы , которые раскручивают двухцепочечную молекулу ДНК, чтобы облегчить доступ к ней, РНК-полимеразы , которые связываются с промотором ДНК для синтеза растущей молекулы РНК, топоизомеразы , которые изменяют количество суперспирализации в ДНК, помогая ей скручиваться и раскручиваться, а также большое разнообразие факторов транскрипции, которые регулируют экспрессию. [61]
Недавно синтезированные молекулы мРНК известны как первичные транскрипты или пре-мРНК. Они должны пройти посттранскрипционную модификацию в ядре, прежде чем экспортироваться в цитоплазму; мРНК, которая появляется в цитоплазме без этих модификаций, деградирует, а не используется для трансляции белка. Три основные модификации — это 5'-кэпирование , 3'- полиаденилирование и сплайсинг РНК . Находясь в ядре, пре-мРНК связана с различными белками в комплексах, известных как гетерогенные рибонуклеопротеиновые частицы (hnRNP). Добавление 5'-кэпа происходит ко-транскрипционно и является первым шагом в посттранскрипционной модификации. 3'-полиадениновый хвост добавляется только после завершения транскрипции. [1] : 509–18
Сплайсинг РНК, осуществляемый комплексом, называемым сплайсосомой , представляет собой процесс, при котором интроны или области ДНК, которые не кодируют белок, удаляются из пре-мРНК, а оставшиеся экзоны соединяются для повторного формирования единой непрерывной молекулы. Этот процесс обычно происходит после 5'-кэпирования и 3'-полиаденилирования, но может начаться до завершения синтеза в транскриптах со многими экзонами. [1] : 494 Многие пре-мРНК могут быть сплайсерованы несколькими способами для получения различных зрелых мРНК, которые кодируют различные белковые последовательности . Этот процесс известен как альтернативный сплайсинг и позволяет производить большое разнообразие белков из ограниченного количества ДНК. [62]

Вход и выход крупных молекул из ядра строго контролируется комплексами ядерных пор. Хотя небольшие молекулы могут входить в ядро без регуляции, [63] макромолекулы, такие как РНК и белки, требуют ассоциации кариоферинов, называемых импортинами, для входа в ядро и экспортинов для выхода. «Грузовые» белки, которые должны быть перемещены из цитоплазмы в ядро, содержат короткие аминокислотные последовательности, известные как сигналы ядерной локализации , которые связываются импортинами, в то время как те, которые транспортируются из ядра в цитоплазму, несут сигналы ядерного экспорта, связанные экспортинами. Способность импортинов и экспортинов транспортировать свой груз регулируется ГТФазами , ферментами, которые гидролизуют молекулу гуанозинтрифосфата (ГТФ) для высвобождения энергии. Ключевой ГТФазой в ядерном транспорте является Ran , которая связана либо с ГТФ, либо с ГДФ (гуанозиндифосфатом), в зависимости от того, находится ли она в ядре или цитоплазме. В то время как импортины зависят от RanGTP для диссоциации от своего груза, экспортинам требуется RanGTP для связывания со своим грузом. [14]
Ядерный импорт зависит от импортина, связывающего свой груз в цитоплазме и переносящего его через ядерную пору в ядро. Внутри ядра RanGTP действует, отделяя груз от импортина, позволяя импортину выйти из ядра и быть повторно использованным. Ядерный экспорт похож, поскольку экспортин связывает груз внутри ядра в процессе, облегчаемом RanGTP, выходит через ядерную пору и отделяется от своего груза в цитоплазме. [64]
Специализированные экспортные белки существуют для транслокации зрелой мРНК и тРНК в цитоплазму после завершения посттранскрипционной модификации. Этот механизм контроля качества важен из-за центральной роли этих молекул в трансляции белка. Неправильная экспрессия белка из-за неполного удаления экзонов или неправильного включения аминокислот может иметь негативные последствия для клетки; таким образом, неполностью модифицированная РНК, которая достигает цитоплазмы, деградирует, а не используется в трансляции. [1]

В течение своей жизни ядро может быть разрушено или уничтожено либо в процессе деления клетки , либо в результате апоптоза (процесса запрограммированной гибели клетки ). Во время этих событий структурные компоненты ядра — оболочка и пластинка — могут систематически разрушаться. В большинстве клеток разборка ядерной оболочки знаменует собой конец профазы митоза . Однако эта разборка ядра не является универсальной особенностью митоза и происходит не во всех клетках. Некоторые одноклеточные эукариоты (например, дрожжи) претерпевают так называемый закрытый митоз , при котором ядерная оболочка остается нетронутой. При закрытом митозе дочерние хромосомы мигрируют к противоположным полюсам ядра, которое затем делится надвое. Однако клетки высших эукариот обычно претерпевают открытый митоз , который характеризуется разрывом ядерной оболочки. Затем дочерние хромосомы мигрируют к противоположным полюсам митотического веретена, и вокруг них собираются новые ядра. [1] : 854
В определенный момент во время клеточного цикла в открытом митозе клетка делится, образуя две клетки. Для того чтобы этот процесс был возможен, каждая из новых дочерних клеток должна иметь полный набор генов, процесс, требующий репликации хромосом, а также сегрегации отдельных наборов. Это происходит за счет того, что реплицированные хромосомы, сестринские хроматиды , прикрепляются к микротрубочкам , которые, в свою очередь, прикрепляются к разным центросомам . Затем сестринские хроматиды могут быть вытянуты в разные места в клетке. Во многих клетках центросома расположена в цитоплазме, вне ядра; микротрубочки не смогли бы прикрепиться к хроматидам в присутствии ядерной оболочки. [65] Таким образом, на ранних стадиях клеточного цикла, начиная с профазы и до прометафазы , ядерная мембрана демонтируется. [18] Аналогично, в тот же период ядерная пластинка также разбирается, процесс регулируется фосфорилированием ламинов протеинкиназами, такими как протеинкиназа CDC2 . [66] К концу клеточного цикла ядерная мембрана реформируется, и примерно в то же время ядерная пластинка собирается заново путем дефосфорилирования ламинов. [66]
Однако у динофлагеллят ядерная оболочка остается нетронутой, центросомы располагаются в цитоплазме, а микротрубочки контактируют с хромосомами, центромерные районы которых включены в ядерную оболочку (так называемый закрытый митоз с внеядерным веретеном). У многих других простейших (например, инфузорий , споровиков ) и грибов центросомы являются внутриядерными, и их ядерная оболочка также не разбирается во время деления клетки. [67]
Апоптоз — это контролируемый процесс, в котором структурные компоненты клетки разрушаются, что приводит к гибели клетки. Изменения, связанные с апоптозом, напрямую влияют на ядро и его содержимое, например, на конденсацию хроматина и распад ядерной оболочки и ламины. Разрушение сетей ламина контролируется специализированными апоптотическими протеазами , называемыми каспазами , которые расщепляют белки ламина и, таким образом, нарушают структурную целостность ядра. Расщепление ламина иногда используется в качестве лабораторного индикатора активности каспазы в анализах на раннюю апоптотическую активность. [18] Клетки, которые экспрессируют мутантные ламины, устойчивые к каспазе, лишены ядерных изменений, связанных с апоптозом, что позволяет предположить, что ламины играют роль в инициировании событий, которые приводят к апоптотической деградации ядра. [18] Ингибирование сборки ламина само по себе является индуктором апоптоза. [68]
Ядерная оболочка действует как барьер, который не позволяет как ДНК-, так и РНК-вирусам проникать в ядро. Некоторым вирусам требуется доступ к белкам внутри ядра для репликации и/или сборки. ДНК-вирусы, такие как вирус герпеса, реплицируются и собираются в ядре клетки и выходят, отпочковываясь через внутреннюю ядерную мембрану. Этот процесс сопровождается разборкой пластинки на ядерной поверхности внутренней мембраны. [18]
Первоначально предполагалось, что иммуноглобулины в целом и аутоантитела в частности не проникают в ядро. Теперь есть доказательства того, что при патологических состояниях (например, красная волчанка ) IgG может проникать в ядро. [69]
Большинство типов эукариотических клеток обычно имеют одно ядро, но некоторые не имеют ядер, а другие имеют несколько. Это может быть результатом нормального развития, как при созревании эритроцитов млекопитающих , или неправильного деления клеток. [70]
Безъядерная клетка не содержит ядра и, следовательно, неспособна делиться для производства дочерних клеток. Самая известная безъядерная клетка — это эритроцит млекопитающего, или эритроцит , в котором также отсутствуют другие органеллы, такие как митохондрии, и который в первую очередь служит транспортным сосудом для переноса кислорода из легких в ткани организма. Эритроциты созревают посредством эритропоэза в костном мозге , где они теряют свои ядра, органеллы и рибосомы. Ядро выталкивается в процессе дифференциации из эритробласта в ретикулоцит , который является непосредственным предшественником зрелого эритроцита. [71] Присутствие мутагенов может вызывать выброс некоторых незрелых «микроядерных» эритроцитов в кровоток. [72] [73] Безъядерные клетки также могут возникать в результате неправильного деления клеток, при котором у одной дочерней клетки отсутствует ядро, а у другой имеется два ядра.
У цветковых растений это состояние встречается в элементах ситовидных трубок . [74]
Многоядерные клетки содержат несколько ядер. Большинство видов простейших акантарей [75] и некоторые грибы в микоризе [76] имеют естественно многоядерные клетки. Другие примеры включают кишечных паразитов рода Giardia , которые имеют два ядра на клетку. [77] Инфузории имеют два вида ядер в одной клетке, соматический макронуклеус и зародышевый микронуклеус . [78] У людей клетки скелетных мышц , также называемые миоцитами и синцитием , становятся многоядерными в процессе развития; результирующее расположение ядер вблизи периферии клеток обеспечивает максимальное внутриклеточное пространство для миофибрилл . [1] Другие многоядерные клетки у человека — остеокласты, тип костных клеток . Многоядерные и двуядерные клетки также могут быть аномальными у людей; например, клетки, возникающие в результате слияния моноцитов и макрофагов , известные как гигантские многоядерные клетки , иногда сопровождают воспаление [79] и также участвуют в образовании опухолей. [80]
Известно, что ряд динофлагеллятов имеет два ядра. В отличие от других многоядерных клеток эти ядра содержат две различные линии ДНК: одну от динофлагеллята и другую от симбиотической диатомовой водоросли . [81]
Как основная определяющая характеристика эукариотической клетки, эволюционное происхождение ядра стало предметом многочисленных спекуляций. Было предложено четыре основные гипотезы для объяснения существования ядра, хотя ни одна из них пока не получила широкой поддержки. [82] [83] [84]
Первая модель, известная как «синтрофная модель», предполагает, что симбиотические отношения между археями и бактериями создали содержащую ядро эукариотическую клетку. (Организмы доменов архей и бактерий не имеют клеточного ядра. [85] ) Предполагается, что симбиоз возник, когда древние археи, похожие на современные метаногенные археи, вторглись и жили внутри бактерий, похожих на современные миксобактерии , в конечном итоге сформировав раннее ядро. Эта теория аналогична принятой теории происхождения эукариотических митохондрий и хлоропластов , которые, как считается, развились из схожих эндосимбиотических отношений между протоэукариотами и аэробными бактериями. [86] Одна из возможностей заключается в том, что ядерная мембрана возникла как новая мембранная система после возникновения митохондрий в хозяине -архебактерии . [87] Ядерная мембрана могла служить для защиты генома от повреждающих активных форм кислорода, производимых протомитохондриями. [88] Архейное происхождение ядра подтверждается наблюдениями, что археи и эукариоты имеют схожие гены для определенных белков, включая гистоны . Наблюдения, что миксобактерии подвижны, могут образовывать многоклеточные комплексы и обладают киназами и G-белками, подобными эукариотам, подтверждают бактериальное происхождение эукариотической клетки. [89]
Вторая модель предполагает, что протоэукариотические клетки произошли от бактерий без эндосимбиотической стадии. Эта модель основана на существовании современных бактерий Planctomycetota , которые обладают ядерной структурой с примитивными порами и другими компартментализированными мембранными структурами. [90] Аналогичное предложение утверждает, что эукариотоподобная клетка, хроноцит , возникла первой и фагоцитировала археи и бактерии, чтобы сформировать ядро и эукариотическую клетку. [91]
Самая спорная модель, известная как вирусный эукариогенез , утверждает, что связанное с мембраной ядро, наряду с другими эукариотическими особенностями, возникло в результате заражения прокариота вирусом. Это предположение основано на сходстве между эукариотами и вирусами, таком как линейные цепи ДНК, кэпирование мРНК и прочное связывание с белками (аналогично гистонам с вирусными оболочками ). Одна из версий предложения предполагает, что ядро эволюционировало совместно с фагоцитозом , чтобы сформировать раннего клеточного « хищника ». [92] Другая версия предполагает, что эукариоты произошли от ранних архей, инфицированных поксвирусами , на основе наблюдаемого сходства между ДНК-полимеразами у современных поксвирусов и эукариот. [93] [94] Было высказано предположение, что нерешенный вопрос об эволюции пола может быть связан с гипотезой вирусного эукариогенеза. [95]
Более позднее предложение, экзомембранная гипотеза , предполагает, что ядро вместо этого произошло от одной предковой клетки, которая развила вторую внешнюю клеточную мембрану; внутренняя мембрана, окружающая исходную клетку, затем стала ядерной мембраной и развила все более сложные пористые структуры для прохождения внутренне синтезированных клеточных компонентов, таких как рибосомные субъединицы. [96]


Ядро было первой открытой органеллой. То, что, скорее всего, является самым старым сохранившимся рисунком, относится к раннему микроскописту Антони ван Левенгуку (1632–1723). Он наблюдал «люмен», ядро, в эритроцитах лосося . [ 97] В отличие от эритроцитов млекопитающих, эритроциты других позвоночных все еще содержат ядра. [98]
Ядро было также описано Францем Бауэром в 1804 году [99] и более подробно в 1831 году шотландским ботаником Робертом Брауном в докладе в Линнеевском обществе Лондона . Браун изучал орхидеи под микроскопом, когда он заметил непрозрачную область, которую он назвал «ареолой» или «ядром», в клетках внешнего слоя цветка. [100] Он не предположил потенциальной функции.
В 1838 году Маттиас Шлейден предположил, что ядро играет роль в образовании клеток, поэтому он ввел название « цитобласт » («строитель клеток»). Он считал, что наблюдал, как новые клетки собираются вокруг «цитобластов». Франц Мейен был ярым противником этой точки зрения, уже описав клетки, размножающиеся путем деления, и полагая, что многие клетки не будут иметь ядер. Идея о том, что клетки могут быть созданы de novo, «цитобластом» или иным образом, противоречила работе Роберта Ремака (1852) и Рудольфа Вирхова (1855), которые решительно пропагандировали новую парадигму, согласно которой клетки создаются исключительно клетками (« Omnis cellula e cellula »). Функция ядра оставалась неясной. [101]
Между 1877 и 1878 годами Оскар Гертвиг опубликовал несколько исследований по оплодотворению яиц морского ежа , показав, что ядро сперматозоида проникает в ооцит и сливается с его ядром. Это был первый раз, когда было высказано предположение, что особь развивается из (единственной) ядросодержащей клетки. Это противоречило теории Эрнста Геккеля о том, что полная филогения вида будет повторяться в ходе эмбрионального развития, включая генерацию первой ядросодержащей клетки из «монерулы», бесструктурной массы первичной протоплазмы (« Urschleim »). Поэтому необходимость ядра сперматозоида для оплодотворения обсуждалась довольно долго. Однако Гертвиг подтвердил свое наблюдение в других группах животных, включая амфибий и моллюсков . Эдуард Страсбургер получил те же результаты для растений в 1884 году. Это проложило путь к приписыванию ядру важной роли в наследственности. В 1873 году Август Вейсман постулировал эквивалентность материнских и отцовских половых клеток для наследственности. Функция ядра как носителя генетической информации стала ясна лишь позже, после открытия митоза и переоткрытия правил Менделя в начале 20-го века; поэтому была разработана хромосомная теория наследственности . [101]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )