Рак мочевого пузыря — это один из нескольких типов рака , возникающих из тканей мочевого пузыря . [1] Симптомы включают кровь в моче , боль при мочеиспускании и боль в пояснице. [1] Он возникает, когда эпителиальные клетки , выстилающие мочевой пузырь, становятся злокачественными. [4]
Факторы риска рака мочевого пузыря включают курение , семейный анамнез, предшествующую лучевую терапию , частые инфекции мочевого пузыря и воздействие определенных химических веществ. [1] Наиболее распространенным типом является переходно-клеточная карцинома . [1] Другие типы включают плоскоклеточную карциному и аденокарциному . [1] Диагноз обычно ставится с помощью цистоскопии с биопсией тканей . [5] Стадию рака определяют с помощью трансуретральной резекции и медицинской визуализации . [1] [6] [7]
Лечение зависит от стадии рака . [1] Оно может включать комбинацию хирургического вмешательства, лучевой терапии, химиотерапии или иммунотерапии . [1] Хирургические варианты могут включать трансуретральную резекцию, частичное или полное удаление мочевого пузыря или отведение мочи . [1] Типичный пятилетний показатель выживаемости в Соединенных Штатах составляет 77%, в Канаде — 75%, а в Европе — 68%. [2] [8] [9]
По состоянию на 2018 год рак мочевого пузыря поразил около 1,6 миллиона человек во всем мире, при этом было зарегистрировано 549 000 новых случаев и 200 000 смертей. [3] Возраст начала заболевания чаще всего составляет от 65 до 84 лет. [2] Мужчины болеют чаще женщин. [2] В 2018 году самый высокий уровень заболеваемости раком мочевого пузыря наблюдался в Южной и Западной Европе, за которой следовала Северная Америка с показателями 15, 13 и 12 случаев на 100 000 человек. [3] Самые высокие показатели смертности от рака мочевого пузыря наблюдались в Северной Африке и Западной Азии, за которыми следовала Южная Европа. [3]

Наиболее распространенным симптомом рака мочевого пузыря является видимая кровь в моче (гематурия), несмотря на безболезненное мочеиспускание. Это касается примерно 75% людей, у которых в конечном итоге диагностируется это заболевание. [10] У некоторых вместо этого наблюдается «микроскопическая гематурия» — небольшое количество крови в моче, которое можно увидеть только под микроскопом во время анализа мочи — боль при мочеиспускании или вообще отсутствие симптомов (их опухоли обнаруживаются во время несвязанной медицинской визуализации ). [10] [11] Реже опухоль может блокировать поток мочи в мочевой пузырь, вызывая боль по бокам тела (между ребрами и бедрами). [12] У большинства людей с кровью в моче нет рака мочевого пузыря; до 22% людей с видимой гематурией и 5% с микроскопической гематурией диагностируют это заболевание. [10] Женщинам с раком мочевого пузыря и гематурией часто ошибочно ставят диагноз инфекции мочевыводящих путей , что задерживает надлежащую диагностику и лечение. [11]
У людей с запущенным заболеванием могут быть боли в области таза или костей, отеки нижних конечностей или боли в боку . [13]


Те, у кого подозревают рак мочевого пузыря, могут пройти несколько тестов, чтобы оценить наличие и степень опухолей. Во-первых, многие проходят физическое обследование, которое может включать пальцевое ректальное исследование и тазовое исследование , при котором врач ощупывает область таза на предмет необычных масс, которые могут быть опухолями. [14] Тяжелые опухоли мочевого пузыря часто выделяют клетки в мочу; их можно обнаружить с помощью цитологии мочи , когда клетки собираются из образца мочи и просматриваются под микроскопом . [14] [15] Цитология может обнаружить около двух третей опухолей высокой степени злокачественности, но обнаруживает только 1 из 8 опухолей низкой степени злокачественности. [16] Дополнительные анализы мочи могут использоваться для обнаружения молекул, связанных с раком мочевого пузыря. Некоторые обнаруживают белки антигена опухоли мочевого пузыря или NMP22 , которые, как правило, повышены в моче у людей с раком мочевого пузыря; некоторые обнаруживают мРНК генов, связанных с опухолью; некоторые используют флуоресцентную микроскопию для обнаружения раковых клеток более чувствительно, чем обычная цитология. [16]
Многие также проходят цистоскопию , при которой гибкая камера вводится в уретру и мочевой пузырь для визуального осмотра на предмет раковой ткани. [14] Цистоскопия наиболее чувствительна к папиллярным опухолям (опухолям пальцевидной формы, которые растут в удерживающую мочу часть мочевого пузыря); она менее чувствительна к небольшой, низко расположенной карциноме in situ (CIS). [17] Обнаружение CIS улучшается с помощью цистоскопии в синем свете , при которой краситель ( гексаминолевулинат ), который накапливается в раковых клетках, вводится в мочевой пузырь во время цистоскопии. Краситель флуоресцирует, когда цистоскоп освещает его синим светом, что позволяет более чувствительно обнаруживать небольшие опухоли. [14] [17]
Верхние мочевые пути ( мочеточники и почки ) также визуализируются на предмет опухолей, которые могут вызывать кровь в моче. Обычно это делается путем инъекции красителя в кровь, которую почки будут фильтровать в мочевыводящие пути, а затем визуализация с помощью компьютерной томографии . Те, чьи почки не функционируют достаточно хорошо, чтобы фильтровать краситель, могут вместо этого пройти сканирование с помощью магнитно-резонансной томографии . [12]
Подозреваемые опухоли удаляются путем введения устройства в уретру в процессе, называемом «трансуретральная резекция опухоли мочевого пузыря» (TURBT). Все опухоли удаляются, а также часть подлежащей мышцы мочевого пузыря. Удаленная ткань исследуется патологом, чтобы определить, является ли она раковой. [14] [18]
_pT1.JPG/440px-Bladder_urothelial_carcinoma_(1)_pT1.JPG)
Опухоли мочевого пузыря классифицируются по их внешнему виду под микроскопом и по типу клеток происхождения. Более 90% опухолей мочевого пузыря возникают из клеток, которые образуют внутреннюю оболочку мочевого пузыря, называемых уротелиальными клетками или переходными клетками; опухоль затем классифицируется как уротелиальный рак или переходноклеточный рак . [19] [20] Около 5% случаев - это плоскоклеточный рак (из более редкой клетки в оболочке мочевого пузыря), особенно распространенный в местах с шистосомозом . [20] До 2% случаев - это аденокарцинома (из клеток желез, продуцирующих слизь ). [20] Остальные случаи - это саркомы (из мышцы мочевого пузыря) или мелкоклеточный рак (из нейроэндокринных клеток ), оба из которых встречаются относительно редко. [20]
Патолог также оценивает образец опухоли на основе того, насколько раковые клетки отличаются от здоровых клеток. Рак мочевого пузыря делится на низкосортный (более похожий на здоровые клетки) или высокосортный (менее похожий). Высокосортный рак далее подразделяется на «немышечно-инвазивный рак мочевого пузыря» (NMIBC) или более агрессивный «мышечно-инвазивный рак мочевого пузыря» (MIBC) на основе того, проросла ли опухоль в окружающую мышцу мочевого пузыря. [19]
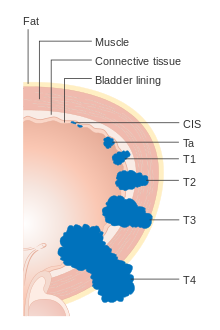




Каждому случаю рака мочевого пузыря присваивается стадия на основе системы TNM , определенной Американским объединенным комитетом по борьбе с раком . [19] Опухоли присваиваются три балла на основе степени распространения первичной опухоли (T), ее распространения на близлежащие лимфатические узлы (N) и метастазов в отдаленные места (M). [21] Балл T представляет степень распространения исходной опухоли: Ta или Tis для опухолей, которые ограничены самым внутренним слоем мочевого пузыря; T1 для опухолей, которые распространяются на соединительную ткань мочевого пузыря; T2 для распространения в мышцу; T3 для распространения через мышцу в окружающую жировую ткань; и T4 для распространения полностью за пределы мочевого пузыря. [21] Балл N представляет распространение на близлежащие лимфатические узлы: N0 — отсутствие распространения; N1 — распространение на один близлежащий лимфатический узел; N2 — распространение на несколько близлежащих лимфатических узлов; N3 — распространение на более отдаленные лимфатические узлы за пределами таза. [21] Балл M обозначает распространение на более отдаленные органы: M0 — опухоль, которая не распространилась; M1 — опухоль, которая распространилась. [21]
Баллы TNM объединяются для определения стадии рака по шкале от 0 до 4, при этом более высокая стадия соответствует более обширному раку с худшим прогнозом. [22]
Люди с немышечно-инвазивным раком мочевого пузыря (NMIBC) стратифицируются по степени риска на основе клинических и патологических факторов, чтобы их лечили соответствующим образом в зависимости от вероятности прогрессирования и/или рецидива. [24] Люди с немышечно-инвазивными опухолями классифицируются на группы низкого, среднего и высокого риска или им присваивается числовая оценка риска. Структура стратификации риска предоставляется Американской ассоциацией урологов/Обществом урологической онкологии (стратификация AUA/SUO), руководящими принципами Европейской ассоциации урологов (EAU), таблицами риска Европейской организации по исследованиям и лечению рака (EORTC) и моделью оценки Club Urológico Español de Tratamiento Oncológico (CUETO). [25] [26] [27]

Лечение рака мочевого пузыря зависит от того, насколько глубоко опухоль проникла в стенку мочевого пузыря. Первым шагом является хирургическое вмешательство, трансуретральная резекция опухоли мочевого пузыря (TURBT), которая является как диагностической процедурой, так и начальным этапом лечения. [28]
Стратегии лечения рака мочевого пузыря включают: [29] [30]
NMIBC в первую очередь лечится путем хирургического удаления всех опухолей с помощью TURBT в той же процедуре, которая используется для сбора биопсийной ткани для диагностики. [31] [32] Для тех, у кого относительно низкий риск рецидива опухолей, однократная доза химиотерапии ( митомицин С , эпирубицин или гемцитабин ), введенная в мочевой пузырь после TURBT, снижает риск возникновения опухоли примерно на 12%. [31] Те, у кого более высокий риск, вместо этого лечатся инъекциями в мочевой пузырь вакцины БЦЖ (живая бактериальная вакцина, обычно используемая для лечения туберкулеза ), вводимыми еженедельно в течение шести недель. Это почти вдвое снижает частоту рецидивов опухоли. [31] Те, у кого опухоли рецидивируют, могут получить второй раунд инъекций БЦЖ. [31] Опухоли, которые не реагируют на БЦЖ, можно лечить альтернативными иммуностимуляторами надофарагеном фираденовеком (продается как «Адстиладрин», генная терапия , которая заставляет клетки мочевого пузыря вырабатывать иммуностимулирующий белок), ногапендекином альфа, инбакицептом («Анктива», комбинация иммуностимулирующих белков) или пембролизумабом («Кейтруда», ингибитор иммунных контрольных точек ). [33]
Людям, чьи опухоли продолжают расти, часто проводят хирургическое лечение, чтобы удалить мочевой пузырь и окружающие органы, называемое радикальной цистэктомией . [34] Мочевой пузырь, несколько прилегающих лимфатических узлов , нижние мочеточники и близлежащие половые органы — у мужчин простата и семенные пузырьки ; у женщин матка и часть стенки влагалища — все удаляются. [34] Хирурги также создают новый путь для вывода мочи из организма. Наиболее распространенным методом является уростомия , когда мочеточники прикрепляются к части подвздошной кишки , а затем к новому хирургическому отверстию ( стоме ) в брюшной полости. Моча пассивно стекает в мешок для стомы , который может регулярно опорожняться носителем. [35]

Однократное введение химиотерапии в мочевой пузырь после первичной ТУР показало пользу в снижении рецидивов на 35% при немышечно-инвазивном заболевании. [36] Лекарства, которые можно использовать для этой цели, - это митомицин С (ММС), эпирубицин , пирарубицин и гемцитабин . Инстилляция послеоперационной химиотерапии должна проводиться в течение первых нескольких часов после ТУР. Известно, что с течением времени остаточные опухолевые клетки прочно прилипают и покрываются внеклеточным матриксом, что снижает эффективность инстилляции. [37] Наиболее распространенным побочным эффектом является химический цистит и раздражение кожи. [36] Если есть подозрение на перфорацию мочевого пузыря во время ТУР, химиотерапию не следует вводить в мочевой пузырь, поскольку известно, что из-за экстравазации препарата могут возникнуть серьезные побочные эффекты. Исследования показали, что эффективность химиотерапии повышается при использовании химиотерапии с использованием устройств. [38] Эти технологии используют различные механизмы для облегчения абсорбции и действия химиотерапевтического препарата, вводимого непосредственно в мочевой пузырь. Другая технология — электромоторное введение лекарств (ЭМДА) — использует электрический ток для улучшения абсорбции лекарств после хирургического удаления опухоли. [39] [40] Другая технология, термотерапия , использует радиочастотную энергию для непосредственного нагрева стенки мочевого пузыря, что вместе с химиотерапией (химиогипертермией) демонстрирует синергетический эффект, усиливая способность друг друга убивать опухолевые клетки. [41]
Для группы среднего риска рекомендуется дополнительная инстилляция химиотерапии в мочевой пузырь, поскольку было показано, что она снижает рецидив в течение 1 года на 38–44%, а рецидив в течение 3 лет — до 70% по сравнению с одной лишь ТУР (хирургией). [6] [28] Обычно ее назначают один раз в неделю в течение 4–6 недель. [8]
Иммунотерапия с помощью доставки бациллы Кальметта-Герена ( БЦЖ ) в мочевой пузырь также используется для лечения и профилактики рецидивов неинвазивного рака мочевого пузыря. [42] БЦЖ — это вакцина против туберкулеза , которая готовится из аттенуированной (ослабленной) живой бычьей туберкулезной палочки, Mycobacterium bovis , которая утратила свою вирулентность у людей. Иммунотерапия БЦЖ эффективна в 2/3 случаев на этой стадии, и в рандомизированных испытаниях было показано, что она превосходит стандартную химиотерапию . [43] Точный механизм, с помощью которого БЦЖ предотвращает рецидив, неизвестен. Однако было показано, что бактерии поглощаются раковыми клетками. [44] Инфицирование этих клеток в мочевом пузыре может вызвать локальную иммунную реакцию, которая очищает остаточные раковые клетки. [45] [46]
БЦЖ проводится в виде индукционного и поддерживающего курса. Индукционный курс состоит из 6-недельного курса внутрипузырьковой и чрескожной БЦЖ. [47] За этим следует поддерживающий курс. Нет единого мнения относительно поддерживающего графика, однако наиболее часто используется график Юго-западной онкологической группы (SWOG). [48] Поддерживающий график SWOG состоит из внутрипузырьковой и чрескожной БЦЖ каждую неделю в течение 3 недель, вводимых через 3, 6, 12, 18, 24, 30 и 36 месяцев. [47] Трехнедельный поддерживающий режим с индукцией показал полный уровень ответа 84% по сравнению с 69% у людей, которые получили 6-недельную индукционную БЦЖ только через 6 месяцев. Во многих исследованиях изучались альтернативные графики лечения и режимы БЦЖ , но не было выявлено клинической значимости. [47] Было показано, что эффективность различных штаммов БЦЖ (Connaught, TICE, Pasteur, Tokio-172) не отличается, однако нет никаких убедительных доказательств. [49]
Побочные эффекты терапии БЦЖ включают цистит , простатит , эпидидимоорхит , баланит , обструкцию мочеточника , сокращение мочевого пузыря, микобактериальный остеомиелит , реактивный артрит , микобактериальную пневмонию, гранулематозный гепатит , гранулематозный нефрит, интерстициальный нефрит , инфекционный васкулит и диссеминированную инфекцию. [50] [51]
Локальную инфекцию (то есть простатит , эпидидимоорхит , баланит ) из-за БЦЖ следует лечить тройной противотуберкулезной терапией, причем одним из препаратов является фторхинолон в течение 3–6 месяцев. У людей с системными инфекциями терапию БЦЖ следует прекратить и начать противотуберкулезное комбинированное лечение в течение как минимум 6 месяцев. Лекарства, которые можно использовать для этого лечения, включают изониазид , рифампицин , этамбутол , фторхинолоны , кларитромицин , аминогликозиды и доксициклин . Штаммы БЦЖ не чувствительны к пиразинамиду , поэтому он не должен быть частью противотуберкулезного лечения. [52]
Ногапендекин альфа инбакисепт (Anktiva), используемый в сочетании с бациллой Кальметта-Герена, был одобрен для медицинского применения в Соединенных Штатах в апреле 2024 года. [53]
Неудачи лечения БЦЖ можно разделить на 3 группы: рецидив БЦЖ, рефрактерность к БЦЖ и непереносимость БЦЖ. При рецидиве БЦЖ опухоль рецидивирует после периода без заболевания. Рефрактерные к БЦЖ опухоли — это те, которые не реагируют на индукционные и поддерживающие дозы БЦЖ или которые прогрессируют во время терапии. При непереносимости БЦЖ опухоль рецидивирует из-за неполного лечения, поскольку человек, получающий ее, не может переносить индукционный курс БЦЖ. Около 50% людей не переносят лечение БЦЖ и нуждаются в дальнейшем лечении. [47]
Людей, у которых опухоли рецидивировали после лечения БЦЖ или которые не поддавались лечению, лечить сложнее. [54] Таким людям рекомендуется радикальная цистэктомия [55] [56] Людям, у которых нет ответа на терапию БЦЖ и которые не подходят или не желают проходить радикальную цистэктомию , можно рассмотреть методы терапии спасения. Терапия спасения включает внутрипузырную химиотерапию такими препаратами, как валрубицин , гемцитабин или доцетаксел , химиолучевую терапию или химиогипертермию. [57]
Фотодинамическая терапия (ФДТ) — это вариант лечения, включающий введение фотосенсибилизирующего агента с последующим воздействием на внутреннюю оболочку мочевого пузыря светом определенной длины волны через цистоскоп. Световая активация фотосенсибилизатора помогает уничтожить раковые клетки, сохраняя при этом большую часть окружающих здоровых тканей. [59] [60]
PDT особенно полезна для пациентов, которые могут подвергаться высокому риску хирургического вмешательства или тех, кто предпочитает менее инвазивный вариант. Процедура известна своей точностью и возможностью повторения, что важно для управления рецидивирующим характером NMIBC. Клинические испытания и исследования показали, что PDT может быть эффективна в снижении частоты рецидивов опухоли и связана с благоприятным профилем безопасности, подчеркивая ее потенциал в качестве основного или вспомогательного метода лечения. [61]
Продолжаются исследования по оценке долгосрочных результатов ФДТ при раке мочевого пузыря и изучению потенциальных улучшений в фотосенсибилизаторах и системах доставки света для повышения эффективности лечения и улучшения результатов для пациентов. [62]

Нелеченые, не инвазивные в мышечную ткань опухоли могут постепенно начать инфильтрировать мышечную стенку мочевого пузыря (инвазивный рак мочевого пузыря с мышечной тканью). Опухоли, инфильтрирующие стенку мочевого пузыря, требуют более радикальной операции, при которой часть ( частичная цистэктомия ) или весь ( радикальная цистэктомия ) мочевой пузырь удаляется (цистэктомия), а мочевой поток отводится в изолированную петлю кишечника (называемую подвздошным каналом или уростомой ). В некоторых случаях опытные хирурги могут создать заменитель мочевого пузыря ( неопузырь ) из сегмента кишечной ткани, но это во многом зависит от предпочтений человека, его возраста, функции почек и места заболевания. [ необходима цитата ]
Двусторонняя тазовая лимфаденэктомия должна сопровождать радикальную цистэктомию. Как минимум, стандартный шаблон лимфаденэктомии должен сопровождаться удалением наружного и внутреннего подвздошного и запирательного лимфатического узла. [63] При выполнении лимфаденэктомии хирург может удалить лимфатические узлы либо из меньшей (стандартной), либо из большей (расширенной) области. По сравнению со стандартной диссекцией лимфатических узлов, расширенная диссекция может снизить вероятность смерти человека по любой причине, включая смерть от рака мочевого пузыря. [64] Расширенная процедура может привести к более серьезным нежелательным эффектам и может или не может повлиять на вероятность рецидива рака с течением времени. [64] Частота не столь серьезных побочных эффектов может быть одинаковой для обеих операций. [64]
Радикальная цистэктомия имеет значительную заболеваемость, связанную с ней. Около 50-65% людей испытывают осложнения в течение 90 дней после операции. [65] [66] Уровень смертности составил 7% в течение 90 дней после операции. Центры с большим объемом имеют лучшие результаты, чем центры с малым объемом. [67] Некоторые центры внедряют рекомендации общества Enhanced Recovery After Surgery (ERAS) для снижения заболеваемости после радикальной цистэктомии. Однако из-за отсутствия конкретных доказательств в урологической хирургии протокол ERAS не был широко включен в урологическую клиническую помощь. [68]
Даже после хирургического удаления мочевого пузыря у 50% людей с инвазивным заболеванием мышц (T2-T4) в течение двух лет развиваются метастатические заболевания из-за микрометастазов . [69] При этом неоадъювантная химиотерапия (химиотерапия перед основным лечением, т. е. хирургическим вмешательством) показала увеличение общей выживаемости за 5 лет с 45% до 50% с абсолютным преимуществом в выживании 5%. [70] [71] [72] В настоящее время два наиболее используемых режима химиотерапии для неоадъювантной химиотерапии основаны на платине: метотрексат , винбластин , доксорубицин , цисплатин (MVAC) и гемцитабин с цисплатином (GC). [73] Другие режимы включают дозозависимый MVAC (DDMVC) и цисплатин, метотрексат и винбластин (CMV). Хотя оптимальный режим не установлен, предпочтительным режимом для неоадъювантной терапии является MVAC. [73]
Роль адъювантной химиотерапии (химиотерапии после основного лечения) ограничена людьми с опухолями высокой степени злокачественности (pT3/T4 и/или N+) и теми, кто не проходил неоадъювантную терапию. [63] Адъювантная лучевая терапия не показала никаких преимуществ при лечении рака мочевого пузыря. [74]
Сочетание лучевой терапии и химиотерапии (химиолучевой терапии) в сочетании с трансуретральной (эндоскопической) резекцией опухоли мочевого пузыря может использоваться в качестве альтернативы у некоторых людей. [77] Обзор имеющихся больших серий данных по этой так называемой тримодальной терапии показал схожие долгосрочные показатели выживаемости при раке с улучшением общего качества жизни, как у людей, перенесших радикальную цистэктомию с реконструкцией мочевыводящих путей. Однако в настоящее время нет рандомизированных контролируемых испытаний, которые сравнивали бы тримодальную терапию с радикальной цистэктомией. Люди, проходящие тримодальную терапию, обычно проходят тщательный отбор и, как правило, имеют заболевание T2 без гидронефроза и/или карциномы in situ. [78] Пятилетняя выживаемость при раке и общая выживаемость после тримодальной терапии составляют от 50% до 82% и от 36% до 74%. [77]
При тримодальной терапии проводится максимальная TURBT с последующей химиолучевой терапией. Используются схемы радиосенсибилизирующей химиотерапии, состоящие из цисплатина или 5-фторурацила и митомицина С. Лучевая терапия осуществляется посредством внешней лучевой терапии бобами ( EBRT ) с целевой лечебной дозой 64-66 Гр. [79] Наблюдение за прогрессированием или рецидивом должно проводиться с помощью КТ , цистоскопии и цитологии мочи. [63] Побочные эффекты химиолучевой терапии включают тошноту , рвоту , потерю аппетита , выпадение волос , язвы во рту , диарею , запор , повышенный риск инфекций и кровотечений , а также усталость. [80]
У людей, которым не помогла тримодальная терапия, радикальная цистэктомия рассматривается, если есть мышечно-инвазивные или рецидивирующие опухоли. Около 25-30% не справляются с лечением и подвергаются спасительной радикальной цистэктомии. [77] TURBT с внутрипузырной терапией показана после неудачи лечения немышечно-инвазивного заболевания. [63]
У людей с одиночной опухолью без сопутствующей карциномы in situ в области, где можно достичь чистых хирургических краев, можно рассмотреть частичную цистэктомию с лимфаденэктомией . План лечения, включающий частичную цистэктомию , должен сопровождаться неоадъювантной химиотерапией. [30] У людей с урахальной аденокарциномой мочевого пузыря можно рассмотреть частичную цистэктомию с резекцией урахальной связки и пупка единым блоком . [81]
Комбинированная химиотерапия с цисплатином является стандартом лечения метастатического мочевого пузыря. [82] Пригодность для получения химиотерапии на основе цисплатина оценивается до начала лечения. Человек считается непригодным, если выполняется хотя бы одно из следующих условий. [83]
Люди, которые считаются подходящими, получают схемы на основе платины; метотрексат , винбластин , доксорубицин с цисплатином (MVAC) или гемцитабин с цисплатином (GC). Альтернативные схемы включают паклитаксел с гемцитабином и цисплатином (PCG, тройная терапия) и цисплатин, метотрексат и винбластин (CMV). Частота ответа для комбинации на основе цисплатина колеблется от 39 до 65%, а полный ответ наблюдается у 12-35% людей. [84] MVAC лучше переносится, если его сочетать с гранулоцитарным колониестимулирующим фактором , и этот режим известен как режим MVAC с высокой плотностью дозы (DDMVAC). Было показано, что эта комбинация снижает смертность от всех причин. [85] Режим MVAC является агрессивным. Фебрильная нейтропения (лихорадка из-за снижения количества лейкоцитов) встречается у 10–14 %, а смерть из-за токсичности — примерно у 3–4 %. Распространенные побочные эффекты MVAC включают подавление костного мозга , лихорадку из-за снижения количества лейкоцитов, сепсис , мукозит , тошноту и рвоту . [84] Напротив, режим GC показал более низкие показатели нейтропенического сепсиса и мукозита 3/4 степени по сравнению с MVAC. [86] Были предприняты попытки повысить переносимость режима на основе цисплатина путем замены его химиотерапией на основе карбоплатина . Однако терапия на основе цисплатина превосходит химиотерапию на основе карбоплатина в достижении общего и полного ответа. [87] Тем не менее, почти половина людей с метастатическим заболеванием «не подходят» для терапии на основе цисплатина. У таких людей в качестве химиотерапии первой линии можно использовать комбинацию карбоплатина и гемцитабина (GemCarbo) . [88] У людей, которым не подходит ни одна химиотерапия на основе платины и у которых наблюдается экспрессия PD-L1 , можно использовать атезолизумаб и пембролизумаб . [ необходима цитата ]
Людям с метастазами в костях следует принимать бисфосфонаты или деносумаб для предотвращения осложнений, связанных со скелетом (например, переломов , компрессии спинного мозга , боли в костях). [89]
Рак мочевого пузыря, который является рефрактерным или прогрессирует после химиотерапии на основе платины, можно лечить с помощью химиотерапии второй линии или иммунотерапии. [ необходима цитата ]
Наиболее часто используемая химиотерапия второй линии — это схемы с одним агентом таксанов ( паклитаксел , наб-паклитаксел и доцетаксел ). Другие схемы с одним агентом включают винфлунин , алкалоид барвинка третьего поколения (одобренный в Европе), гемцитабин , пеметрексед , оксалиплатин и ифосфамид . [90] [91] [92] Побочные эффекты винфлунина включают нейтропению , запор , усталость и анемию , что ограничивает его использование в качестве агента второй линии. Ответ на химиотерапию второй линии наблюдается у 5%–20% людей. Медиана выживаемости без прогрессирования при химиотерапии второй линии составляет 3–4 месяца. [93]
У людей с мутациями рецепторов фактора роста фибробластов ( FGFR ) и неэффективностью стандартной платиновой химиотерапии можно использовать эрдафитиниб . Эрдафитиниб показал частоту ответа 40% у этих пациентов. [94]
Пять иммунотерапевтических агентов были одобрены в США для использования при метастатическом раке мочевого пузыря. Они действуют путем ингибирования белка запрограммированной клеточной смерти 1 (PD-1) или лиганда запрограммированной клеточной смерти 1 (PD-L1) . Пембролизумаб и ниволумаб являются ингибиторами лиганда запрограммированной клеточной смерти 1 (PD-1) . Авелумаб , атезолизумаб и дурвалумаб являются ингибиторами PD-L1 . [95] [96]
Пембролизумаб, вероятно, немного улучшает общую выживаемость и может немного улучшить качество жизни людей с уротелиальным раком , состояние которых ухудшилось после первоначального лечения по сравнению с продолжающейся химиотерапией. [97] Однако пембролизумаб может иметь лишь минимальное влияние на уровень смертности в результате лечения или скорость прогрессирования рака. [97] Пембролизумаб может вызывать менее серьезные побочные эффекты, чем химиотерапия. [97]
Контрастная КТ используется для мониторинга метастазов в легких, печени и лимфатических узлах. Сканирование костей используется для обнаружения и мониторинга метастазов в костях. [98] Ответ на лечение измеряется с использованием критериев оценки ответа при солидных опухолях ( RECIST ) в одной из следующих групп: ответ (полный или частичный), стабильное заболевание и прогрессирующее заболевание. [99]
Рак мочевого пузыря вызывается генетическим повреждением ДНК клеток мочевого пузыря. Эти изменения могут быть случайными или могут быть вызваны воздействием на мочевой пузырь токсичных веществ, таких как употребление табака. Накопление этого генетического повреждения нарушает нормальное функционирование клеток мочевого пузыря, заставляя их неконтролируемо расти и образовывать опухоль. [100]
Табакокурение является основным известным фактором, способствующим развитию рака мочевого пузыря; в большинстве популяций курение связано с более чем половиной случаев рака мочевого пузыря у мужчин и одной третью случаев среди женщин, [101] однако эти пропорции снизились за последние годы, поскольку в Европе и Северной Америке стало меньше курильщиков. [102] Существует почти линейная зависимость между продолжительностью курения (в годах), пачкой-лет и риском рака мочевого пузыря. Можно наблюдать плато риска при выкуривании около 15 сигарет в день (это означает, что те, кто выкуривает 15 сигарет в день, подвергаются примерно такому же риску, как и те, кто выкуривает 30 сигарет в день). Курение в любой форме (сигары, сигареты, трубка, египетский кальян и бездымный табак) увеличивает риск рака мочевого пузыря. [103] Отказ от курения снижает риск. Риск рака мочевого пузыря снижается на 30% в течение 1–4 лет и продолжает снижаться на 60% через 25 лет после прекращения курения. [104] Однако бывшие курильщики, скорее всего, всегда будут подвержены более высокому риску рака мочевого пузыря по сравнению с людьми, которые никогда не курили. [102] Пассивное курение также, по-видимому, представляет риск. [105] [106]
Потребление опиума увеличивает риск рака мочевого пузыря в три раза, в то время как одновременное употребление опиума и табака увеличивает риск рака мочевого пузыря в пять раз по сравнению с общей популяцией. [107]
Тридцать процентов опухолей мочевого пузыря, вероятно, являются результатом профессионального воздействия канцерогенов на рабочем месте. Профессиональное или случайное воздействие следующих веществ рассматривается как причина рака мочевого пузыря: бензидин (производство красителей), 4-аминобифенил (резиновая промышленность), 2-нафтиламин (производство азокрасителей, литейные пары, резиновая промышленность, сигаретный дым и исследования рака), фенацетин (анальгетик), мышьяк и хлорированные алифатические углеводороды в питьевой воде, аурамин (производство красителей), фуксин (производство красителей), орто-толуидин (производство красителей), отвердители эпоксидных и полиуретановых смол (производство пластмасс), хлорнафазин , каменноугольный пек . [108] [109] [110] [111] [112] В группу риска входят водители автобусов, рабочие резиновых изделий, маляры, автомеханики, кожевенники (включая обувщиков), кузнецы, наладчики машин и механики. [113] [114] Парикмахеры также, как полагают, подвержены риску из-за частого воздействия перманентных красок для волос. [115]
Инфекция Schistosoma haematobium (бильгарциоз или шистосомоз ) может вызвать рак мочевого пузыря, особенно плоскоклеточный. [116] Яйца шистосомы вызывают хроническое воспалительное состояние в стенке мочевого пузыря, что приводит к фиброзу тканей. [117] В образцах мочи людей с шистосомозом обнаружены более высокие уровни соединений N-нитрозо . [118] Соединения N-нитрозо участвуют в патогенезе рака мочевого пузыря, связанного с шистосомозом. Они вызывают повреждение ДНК алкилированием, особенно мутации перехода гуанина в аденин в гене HRAS и супрессоре опухолей p53 . [119] Мутации p53 обнаружены в 73% опухолей, мутации BCL-2 составляют 32%, а их сочетание — 13%. [120] Другие причины плоскоклеточного рака мочевого пузыря включают хроническую катетеризацию у людей с повреждением спинного мозга и анамнезом лечения циклофосфамидом. [121] [122]
Американский институт исследований рака заявил, что существуют веские доказательства того, что употребление воды, содержащей мышьяк, увеличивает риск рака мочевого пузыря. [123]
Высокое потребление животных жиров и пищевого холестерина увеличивает риск рака мочевого пузыря у мужчин. [124]
Было показано, что прием аристолохиевой кислоты , присутствующей во многих китайских травяных лекарствах, вызывает уротелиальную карциному и почечную недостаточность . [125] Аристолохиевая кислота активирует пероксидазу в уротелии и вызывает трансверсионную мутацию в гене- супрессоре опухолей TP53 . [ необходима ссылка ]
Люди, проходящие внешнюю лучевую терапию (EBRT) при раке предстательной железы, имеют более высокий риск развития инвазивного рака мочевого пузыря. [126]
В дополнение к этим основным факторам риска существует также множество других модифицируемых факторов, которые менее сильно (т.е. увеличивают риск на 10–20%) связаны с раком мочевого пузыря, например, ожирение . [127] Хотя их можно рассматривать как незначительные эффекты, снижение риска среди населения в целом все равно может быть достигнуто путем снижения распространенности ряда более мелких факторов риска вместе. [128]
Мутации в генах FGFR3 , TP53 , PIK3CA , KDM6A , ARID1A , KMT2D , HRAS , TERT , KRAS , CREBBP , RB1 и TSC1 могут быть связаны с некоторыми случаями рака мочевого пузыря. [129] [130] [131] Делеции частей или всей хромосомы 9 распространены при раке мочевого пузыря. [132] Известно, что низкозлокачественный рак содержит мутации в пути RAS и гене рецептора фактора роста фибробластов 3 (FGFR3), оба из которых играют роль в пути MAPK/ERK . Мутации генов p53 и RB связаны с высокозлокачественными мышечно-инвазивными опухолями. [133] Восемьдесят девять процентов мышечно-инвазивных раков имеют мутации в генах ремоделирования хроматина и модификации гистонов. [134] Удаление обеих копий гена GSTM1 имеет умеренное увеличение риска рака мочевого пузыря. Продукт гена GSTM1 глутатион S-трансфераза M1 (GSTM1) участвует в процессе детоксикации канцерогенов, таких как полициклические ароматические углеводороды , обнаруженные в сигаретном дыме. [135] Аналогично, мутации в NAT2 ( N-ацетилтрансфераза ) связаны с повышенным риском рака мочевого пузыря. N-ацетилтрансфераза помогает в детоксикации канцерогенов , таких как ароматические амины (также присутствуют в сигаретном дыме). [136] Различные однонуклеотидные полиморфизмы в гене PSCA, присутствующем на хромосоме 8, показали увеличение риска рака мочевого пузыря. Промоторная область гена PSCA имеет область ответа на андрогены . Потеря реактивности этой области к андрогенам предположительно является причиной более агрессивных опухолей у женщин (в отличие от мужчин, у которых больше андрогенов). [137]
Мышечно-инвазивный рак мочевого пузыря по своей природе неоднороден. В целом, их можно генетически классифицировать на базальный и люминальный подтипы. Базальный подтип показывает изменения, связанные с RB и NFE2L2 , а люминальный тип показывает изменения в генах FGFR3 и KDM6A. [138] Базальный подтип подразделяется на базальную и низкоклаудиновую группу, они агрессивны и показывают метастазы при постановке диагноза, однако они реагируют на химиотерапию на основе платины. Люминальный подтип можно подразделить на p53-подобные и люминальные. p53-подобные опухоли люминального подтипа, хотя и не такие агрессивные, как базальный тип, показывают устойчивость к химиотерапии [139]
Наиболее распространенными местами метастазов рака мочевого пузыря являются лимфатические узлы, кости, легкие, печень и брюшина . [140] Наиболее распространенными сторожевыми лимфатическими узлами, дренирующими рак мочевого пузыря, являются запирательные и внутренние подвздошные лимфатические узлы . Местоположение лимфатического распространения зависит от местоположения опухолей. Опухоли на верхнелатеральной стенке мочевого пузыря распространяются на наружные подвздошные лимфатические узлы . Опухоли на шее, передней стенке и дне обычно распространяются на внутренние подвздошные лимфатические узлы. [141] Из регионарных лимфатических узлов (т. е. запирательных, внутренних и наружных лимфатических узлов) рак распространяется в отдаленные места, такие как общие подвздошные лимфатические узлы и парааортальные лимфатические узлы . [142] Пропущенные поражения лимфатических узлов не наблюдаются при раке мочевого пузыря. [141]
По состоянию на 2019 год имеется ограниченное количество доказательств высокого уровня, позволяющих предположить, что употребление овощей и фруктов снижает риск рака мочевого пузыря. [136] Фрукты и желто-оранжевые овощи , особенно морковь и те, которые содержат селен , цитрусовые и крестоцветные овощи, были идентифицированы как имеющие возможный защитный эффект.
Хотя предполагается, что полифенольные соединения в чае могут оказывать ингибирующее действие на образование и рост опухоли мочевого пузыря, имеются ограниченные доказательства того, что употребление чая снижает риск рака мочевого пузыря. [136] Обзор 2022 года показал, что средиземноморская диета оказывает защитное действие на риск рака мочевого пузыря. [143] Более высокое потребление мононенасыщенных жиров и растительных масел снижает риск рака мочевого пузыря у женщин. [124] Более высокое потребление общей пищевой клетчатки и цельного зерна связано со снижением риска рака мочевого пузыря. [144]
По состоянию на 2019 год недостаточно данных, чтобы определить, эффективен ли скрининг на рак мочевого пузыря у людей без симптомов. [145]
У людей с неинвазивными опухолями в мышечную ткань прогноз благоприятный (5-летняя выживаемость составляет 95% по сравнению с 69% при инвазивном раке мочевого пузыря в мышечную ткань). [146] [147] Однако у 70% из них будет рецидив после первоначального лечения, а у 30% из них будет наблюдаться инвазивное заболевание в мышечную ткань. [148] Рецидив и прогрессирование до более высокой стадии заболевания имеют менее благоприятный прогноз. [149]
Выживаемость после радикальной цистэктомии и тазовой лимфодиссекции зависит от патологической стадии. Если заболевание не распространилось на лимфоузел и ограничено мочевым пузырем (T1 или T2, N0), то 5-летняя выживаемость составляет 78%. Если заболевание распространилось локально вокруг области мочевого пузыря без вовлечения лимфоузлов (T3, N0), то 5-летняя выживаемость снижается до 47%. При заболевании с распространением на лимфоузлы (N+, независимо от стадии T) 5-летняя выживаемость составляет 31%. Местно-распространенное и метастатическое заболевание резко снижает выживаемость, медиана выживаемости без химиотерапии составляет 3–6 месяцев. Химиотерапия на основе цисплатина увеличила медиану выживаемости до 15 месяцев. Однако 5-летняя выживаемость по-прежнему составляет 15%. [150]
Существует несколько прогностических факторов, которые определяют специфическую для рака выживаемость после радикальной цистэктомии. Факторами с отрицательным эффектом на специфическую для рака выживаемость являются пожилой возраст, более высокая степень злокачественности опухоли и патологическая стадия, метастазы в лимфатические узлы , наличие лимфоваскулярной инвазии и положительный край мягких тканей. [151] Плотность лимфатических узлов (положительные лимфатические узлы/общее количество лимфатических узлов , наблюдаемых в образце после операции) является предиктором выживаемости при положительном по отношению к лимфатическим узлам заболевании. Чем выше плотность, тем ниже выживаемость. [152]
После радикальной цистэктомии мочевая и сексуальная функции остаются ниже, чем у населения в целом. Люди с неоцистисом имеют лучшую эмоциональную функцию и образ тела по сравнению с теми, у кого кожное отведение мочи (кому необходимо носить мешок для сбора мочи на животе). [153] Социальные факторы, такие как семья, отношения, здоровье и финансы, вносят значительный вклад в определение хорошего качества жизни у людей, у которых диагностирован рак мочевого пузыря. [154]
Высокий процент людей с раком мочевого пузыря страдает от тревожности и депрессии . [155] Молодые, одинокие люди с запущенным клиническим заболеванием имеют высокий риск диагностирования психического заболевания после лечения. Люди с психическим заболеванием после лечения, по-видимому, имеют худшую специфическую для рака и общую выживаемость. [156] [157]

Около 500 000 человек ежегодно диагностируют рак мочевого пузыря, и 200 000 умирают от этой болезни. [161] Это делает рак мочевого пузыря десятым наиболее часто диагностируемым видом рака и тринадцатой причиной смерти от рака. [162] Рак мочевого пузыря наиболее распространен в более богатых регионах мира, где воздействие определенных канцерогенов наиболее велико. Он также распространен в местах, где распространена инфекция шистосом , например, в Северной Африке. [162]
Рак мочевого пузыря встречается гораздо чаще у мужчин, чем у женщин; примерно у 1,1% мужчин и 0,27% женщин развивается рак мочевого пузыря. [11] Это делает рак мочевого пузыря шестым по распространенности видом рака у мужчин и семнадцатым у женщин. [163] Когда женщинам диагностируют рак мочевого пузыря, у них, как правило, более запущенное заболевание и, следовательно, более плохой прогноз. [163] Эта разница в результатах объясняется многочисленными факторами, такими как разница в воздействии канцерогенов, генетика , социальные факторы и качество медицинской помощи. [137] Одним из распространенных признаков рака мочевого пузыря является гематурия, и довольно часто его ошибочно диагностируют как инфекцию мочевыводящих путей у женщин, что приводит к задержке в диагностике. [137] Курение может лишь частично объяснить эти более высокие показатели у мужчин в западном полушарии. [164] В Африке мужчины более склонны к полевым работам и подвержены заражению шистосомой , это может в определенной степени объяснить разрыв в заболеваемости плоскоклеточным раком в районах, где рак мочевого пузыря является эндемичным. [164]
Как и большинство видов рака, рак мочевого пузыря чаще встречается у пожилых людей; в среднем рак мочевого пузыря диагностируется в возрасте 73 лет. [165]
{{cite book}}: CS1 maint: местоположение отсутствует издатель ( ссылка ) CS1 maint: другие ( ссылка ){{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка )