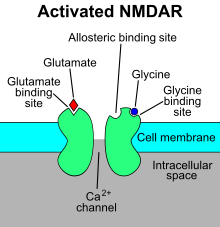
Рецептор N -метил- D -аспартата (также известный как рецептор NMDA или NMDAR ) представляет собой рецептор глутамата и ионный канал, обнаруженный в нейронах . Рецептор NMDA — один из трех типов ионотропных рецепторов глутамата , два других — AMPA и каинатные рецепторы . В зависимости от субъединичного состава его лигандами являются глутамат и глицин (или D -серин ). Однако связывания лигандов обычно недостаточно для открытия канала, поскольку он может блокироваться ионами Mg 2+ , которые удаляются только тогда, когда нейрон достаточно деполяризован. Таким образом, канал действует как «детектор совпадений», и только при выполнении обоих этих условий канал открывается и позволяет положительно заряженным ионам (катионам) проходить через клеточную мембрану . [3] Считается, что NMDA-рецептор очень важен для контроля синаптической пластичности и обеспечения функций обучения и памяти . [4]
Рецептор NMDA является ионотропным , то есть представляет собой белок, который позволяет ионам проходить через клеточную мембрану. [5] Рецептор NMDA назван так потому, что молекула -агонист N -метил- D -аспартат (NMDA) избирательно связывается с ним, а не с другими глутаматными рецепторами . Активация NMDA-рецепторов приводит к открытию ионного канала, неселективного по отношению к катионам , с комбинированным реверсивным потенциалом около 0 мВ. Хотя открытие и закрытие ионного канала в первую очередь регулируется связыванием лиганда, ток через ионный канал зависит от напряжения. Определенно локализованные на рецепторе, внеклеточные ионы магния (Mg 2+ ) и цинка (Zn 2+ ) могут связывать и предотвращать прохождение других катионов через открытый ионный канал. Зависимый от напряжения поток ионов натрия (Na + ), кальция (Ca 2+ ) и калия (K + ) в клетку и из нее становится возможным благодаря деполяризации клетки, которая вытесняет и отталкивает Mg 2+. и ионы Zn 2+ из поры. [6] [7] [8] [9] Поток Ca 2+ через NMDA-рецепторы, в частности, считается критически важным для синаптической пластичности, клеточного механизма обучения и памяти, благодаря белкам, которые связываются с Ca 2 и активируются им. + ионы.
Активность рецептора NMDA блокируется многими психоактивными препаратами, такими как фенциклидин (PCP), алкоголь ( этанол ) и декстрометорфан (DXM). Анестезирующее и обезболивающее действие препаратов кетамина и закиси азота также частично обусловлено их действием на блокирование активности рецепторов NMDA . Напротив, чрезмерная активация NMDAR агонистами NMDA увеличивает цитозольные концентрации кальция и цинка , что значительно способствует гибели нейронов , эффект, который, как известно, предотвращается каннабиноидами , опосредованный активацией рецептора CB 1 , что заставляет белок HINT1 противодействовать токсические эффекты NMDAR-опосредованного производства NO и высвобождения цинка. [10] Помимо предотвращения нейротоксичности , вызванной метамфетамином , посредством ингибирования экспрессии синтазы оксида азота (nNOS) и активации астроцитов , наблюдается уменьшение вызванного метамфетамином повреждения головного мозга посредством CB1-зависимого и независимого механизмов соответственно, а также ингибирование астроглиоза , вызванного метамфетамином. вероятно, происходит через механизм, зависящий от рецептора CB 2 для ТГК . [11] С 1989 года мемантин признан неконкурентным антагонистом рецептора NMDA, попадая в канал рецептора после его активации и тем самым блокируя поток ионов. [12] [13] [14]
Сверхактивация рецептора, вызывающая чрезмерный приток Ca 2+ , может привести к эксайтотоксичности , которая, как предполагается, участвует в некоторых нейродегенеративных заболеваниях. Таким образом, блокирование рецепторов NMDA теоретически может быть полезно при лечении таких заболеваний. [14] [15] [16] [17] Однако гипофункция NMDA-рецепторов (из-за дефицита глутатиона или других причин) может быть вовлечена в нарушение синаптической пластичности [18] и может иметь другие негативные последствия. Основная проблема использования антагонистов рецепторов NMDA для нейропротекции заключается в том, что физиологические действия рецепторов NMDA необходимы для нормальной функции нейронов. Чтобы быть клинически полезными, антагонисты NMDA должны блокировать чрезмерную активацию, не нарушая нормальных функций. Мемантин обладает этим свойством. [19]
За открытием NMDA-рецепторов последовал синтез и исследование N -метил- D -аспарагиновой кислоты (NMDA) в 1960-х годах Джеффом Уоткинсом и его коллегами. В начале 1980-х годов было показано, что NMDA-рецепторы участвуют в нескольких центральных синаптических путях. [20] [21] Селективность субъединиц рецепторов была обнаружена в начале 1990-х годов, что привело к признанию нового класса соединений, которые избирательно ингибируют субъединицу NR2B . Эти открытия привели к энергичной кампании в фармацевтической промышленности. [9] На основании этого считалось, что NMDA-рецепторы связаны с различными неврологическими расстройствами , такими как эпилепсия , болезнь Паркинсона , болезнь Альцгеймера , болезнь Хантингтона и другие расстройства ЦНС. [6]
В 2002 году Хилмар Бадинг и его коллеги обнаружили , что клеточные последствия стимуляции рецептора NMDA зависят от местоположения рецептора на поверхности нейрональных клеток. [22] [23] Синаптические NMDA-рецепторы способствуют экспрессии генов, событиям, связанным с пластичностью, и приобретенной нейропротекции . Внесинаптические рецепторы NMDA способствуют передаче сигналов смерти; они вызывают отключение транскрипции, митохондриальную дисфункцию и структурный распад. [22] [23] Эта патологическая триада внесинаптической передачи сигналов рецептора NMDA представляет собой общую точку конверсии в этиологии нескольких острых и хронических нейродегенеративных состояний. [24] Молекулярная основа передачи сигналов токсических внесинаптических рецепторов NMDA была открыта Хилмаром Бадингом и его коллегами в 2020 году. [25] Внесинаптические рецепторы NMDA образуют сигнальный комплекс смерти с TRPM4. Ингибиторы интерфейса взаимодействия NMDAR/TRPM4 (также известные как ингибиторы интерфейса) разрушают комплекс NMDAR/TRPM4 и детоксицируют экстрасинаптические рецепторы NMDA. [25]
Случайное открытие было сделано в 1968 году, когда женщина, принимавшая амантадин в качестве лекарства от гриппа, испытала значительную ремиссию симптомов болезни Паркинсона. Это открытие, о котором сообщили Скаваб и др., положило начало медицинской химии производных адамантана в контексте заболеваний, поражающих ЦНС. [26] До этого открытия мемантин, другое производное адамантана, был синтезирован компанией Eli Lilly and Company в 1963 году. Целью была разработка гипогликемического препарата , но он не показал такой эффективности . Лишь в 1972 году была открыта возможная терапевтическая значимость мемантина для лечения нейродегенеративных заболеваний. С 1989 года мемантин признан неконкурентным антагонистом рецептора NMDA. [13]

Функциональные NMDA-рецепторы представляют собой гетеротетрамеры, содержащие различные комбинации субъединиц GluN1, GluN2 (AD) и GluN3 (AB), происходящих из разных семейств генов ( Grin1 - Grin3 ). Все NMDAR содержат одну или несколько обязательных субъединиц GluN1, которые при сборке с субъединицами GluN2 того же типа дают канонические дигетеромерные ( d- ) NMDAR (например, GluN1-2A-1-2A). Тригетеромерные NMDAR, напротив, содержат три различных типа субъединиц (например, GluN1-2A-1-2B) и включают рецепторы, состоящие из одной или нескольких субъединиц каждого из трех семейств генов, обозначенных t -NMDAR (например, ГлуН1-2А-3А-2А). [27] Существует один ген GluN1, четыре GluN2 и два гена, кодирующих субъединицу GluN3, и каждый ген может производить более одного варианта сплайсинга.

Рецептор NMDA представляет собой белковый рецептор глутамата и ионного канала , который активируется, когда с ним связываются глицин и глутамат. [3] Рецептор представляет собой очень сложный и динамичный гетеромерный белок, который взаимодействует со множеством внутриклеточных белков через три отдельные субъединицы, а именно GluN1, GluN2 и GluN3. Субъединица GluN1, кодируемая геном GRIN1, благодаря альтернативному сплайсингу имеет восемь различных изоформ. С другой стороны, субъединица GluN2, имеющая четыре различных типа (AD), а также субъединица GluN3, имеющая два типа (A и B), каждая кодируется шестью отдельными генами. Эта сложная молекулярная структура и генетическое разнообразие позволяют рецептору выполнять широкий спектр физиологических функций в нервной системе . [28] [29] Все субъединицы имеют общую топологию мембраны, в которой преобладает большой внеклеточный N-конец, область мембраны, содержащая три трансмембранных сегмента, петля возвратной поры, внеклеточная петля между трансмембранными сегментами, которые структурно малоизвестные, а также внутриклеточные С-концы, которые различаются по размеру в зависимости от субъединицы и обеспечивают множество сайтов взаимодействия со многими внутриклеточными белками. [28] [30] На рисунке 1 показана базовая структура субъединиц GluN1/GluN2, которая образует сайт связывания мемантина, Mg 2+ и кетамина .
Mg 2+ блокирует канал рецептора NMDA зависимым от напряжения образом. Каналы также обладают высокой проницаемостью для Ca 2+ . Активация рецептора зависит от связывания глутамата, связывания D -серина или глицина в его сайте связывания с GluN1 и опосредованной рецептором AMPA деполяризации постсинаптической мембраны, которая снимает потенциал-зависимую блокировку каналов с помощью Mg 2+ . Таким образом, активация и открытие рецепторного канала обеспечивает поток ионов K + , Na + и Ca2 + , а приток Ca2 + запускает внутриклеточные сигнальные пути. [12] [31] Сайты связывания аллостерических рецепторов цинка, белков и полиаминов спермидина и спермина также являются модуляторами каналов рецепторов NMDA. [32]
Субъединица GluN2B участвует в модуляции активности, такой как обучение, память, обработка информации и пищевое поведение, а также участвует в ряде человеческих расстройств. Основная структура и функции, связанные с рецептором NMDA, могут быть отнесены к субъединице GluN2B. Например, сайт связывания глутамата и контроль блока Mg 2+ образованы субъединицей GluN2B. Сайты с высоким сродством к антагонисту глицина также обнаруживаются исключительно рецептором GluN1/GluN2B. [29]
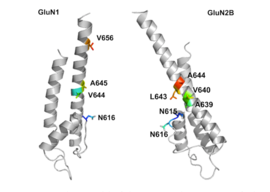
Трансмембранные сегменты GluN1/GluN2B считаются частью рецептора, которая образует карманы связывания для неконкурентных антагонистов рецептора NMDA, но структуры трансмембранных сегментов, как указано выше, полностью не известны. Утверждается, что три сайта связывания внутри рецептора: A644 на субъединице GluNB и A645 и N616 на субъединице GluN1, важны для связывания мемантина и родственных соединений, как показано на рисунке 2. [30]
Рецептор NMDA образует гетеротетрамер между двумя субъединицами GluN1 и двумя субъединицами GluN2 (субъединицы ранее обозначались как GluN1 и GluN2), двумя обязательными субъединицами GluN1 и двумя регионально локализованными субъединицами GluN2. Родственное семейство генов субъединиц A и B GluN3 оказывает ингибирующее действие на активность рецепторов. Множественные изоформы рецепторов с различным распределением в мозге и функциональными свойствами возникают в результате селективного сплайсинга транскриптов GluN1 и дифференциальной экспрессии субъединиц GluN2.
Каждая субъединица рецептора имеет модульную конструкцию и каждый структурный модуль также представляет собой функциональную единицу:
Глицин-связывающие модули субъединиц GluN1 и GluN3 и глутамат-связывающий модуль субъединицы GluN2A были выражены в виде растворимых белков, а их трехмерная структура была решена с атомным разрешением с помощью рентгеновской кристаллографии . Это выявило общую структуру со связывающими аминокислоты бактериальными белками и с глутамат-связывающим модулем АМРА-рецепторов и каинатных рецепторов.
NMDA-рецепторы играют важную роль в развитии центральной нервной системы. Процессы обучения, памяти и нейропластичности зависят от механизма NMDA-рецепторов. NMDA-рецепторы представляют собой катионные каналы, управляемые глутаматом, которые позволяют увеличить проницаемость кальция . Активация каналов NMDA-рецепторов происходит в результате связывания двух коагонистов глицина и глутамата .
Гиперактивация NMDA-рецепторов, вызывающая чрезмерный приток Са 2+ , может привести к эксайтотоксичности. Предполагается, что эксайтотоксичность связана с некоторыми нейродегенеративными расстройствами, такими как болезнь Альцгеймера, болезнь Паркинсона и болезнь Хантингтона. [14] [15] [16] [17] Таким образом, блокирование рецепторов NMDA теоретически может быть полезно при лечении таких заболеваний. [14] [15] [16] Однако важно сохранить физиологическую активность рецептора NMDA, одновременно пытаясь блокировать его чрезмерную эксайтотоксическую активность. Возможно, этого можно достичь с помощью неконкурентных антагонистов, блокирующих ионный канал рецептора, когда он чрезмерно открыт. [16]
Неконкурентные антагонисты рецептора NMDA, или блокаторы каналов, попадают в канал рецептора NMDA после его активации и тем самым блокируют поток ионов. [12] [14] МК-801 , кетамин , амантадин и мемантин являются примерами таких антагонистов, [12] см. рисунок 1. Скорость выхода антагониста из рецепторного канала является важным фактором, поскольку слишком медленная скорость выхода может мешают нормальной функции рецептора, а слишком быстрое снижение скорости может привести к неэффективной блокаде чрезмерно открытого рецептора. [16]
Мемантин является примером неконкурентного блокатора каналов рецептора NMDA с относительно быстрым действием и низким сродством. При физиологическом pH его аминогруппа заряжена положительно, а ее антагонизм к рецепторам зависит от напряжения. [16] Таким образом, он имитирует физиологическую функцию Mg 2+ как блокатора каналов. [13] Мемантин блокирует каналы, связанные с NMDA-рецептором, только во время длительной активации рецептора, как это происходит в эксайтотоксических условиях, путем замены магния в месте связывания. При нормальной активности рецепторов каналы остаются открытыми только в течение нескольких миллисекунд, и в этих обстоятельствах мемантин не может связываться внутри каналов и, следовательно, не мешает нормальной синаптической активности. [19]
Существует восемь вариантов субъединицы GluN1 , полученных путем альтернативного сплайсинга GRIN1 : [33]
.jpg/440px-Model_of_NR2_Subunit_of_NMDA_receptor_(vertebrate_and_invertebrate).jpg)
Хотя у беспозвоночных организмов обнаружена одна субъединица GluN2 , у позвоночных экспрессируются четыре различные изоформы субъединицы GluN2, которые обозначаются номенклатурой от GluN2A до GluN2D (кодируются GRIN2A , GRIN2B , GRIN2C , GRIN2D ). Убедительные доказательства показывают, что гены, кодирующие субъединицы GluN2 у позвоночных, претерпели как минимум два раунда генной дупликации . [34] Они содержат сайт связывания глутамата . Что еще более важно, каждая субъединица GluN2 имеет отдельный внутриклеточный С-концевой домен, который может взаимодействовать с разными наборами сигнальных молекул. [35] В отличие от субъединиц GluN1, субъединицы GluN2 экспрессируются по-разному в разных типах клеток и в разные моменты развития и контролируют электрофизиологические свойства рецептора NMDA. В классических схемах GluN2B в основном присутствует в незрелых нейронах и во внесинаптических местах , таких как конусы роста [36] и содержит сайт связывания селективного ингибитора ифенпродила . [37] Однако в синапсах пирамидальных клеток недавно развившейся дорсолатеральной префронтальной коры приматов GluN2B находится исключительно в пределах постсинаптической плотности и опосредует высшие когнитивные операции, такие как рабочая память . [38] Это согласуется с расширением действия и экспрессии GluN2B по всей кортикальной иерархии у обезьян [39] и людей [40], а также с эволюцией коры головного мозга приматов . [41]
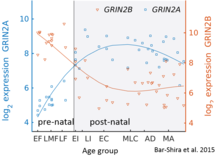
Хотя GluN2B преобладает в раннем постнатальном мозге, количество субъединиц GluN2A увеличивается во время раннего развития; со временем субъединиц GluN2A становится больше, чем GluN2B. Это называется переключением развития GluN2B-GluN2A, и оно примечательно тем, что каждая субъединица GluN2 вносит свой вклад в функцию рецептора по-разному. [43] Например, большее соотношение субъединицы GluN2B приводит к тому, что рецепторы NMDA остаются открытыми дольше по сравнению с рецепторами с большим количеством GluN2A. [44] Частично это может объяснить более высокие способности памяти в ближайшем послеродовом периоде по сравнению с поздним возрастом, что является принципом генетически измененных « мышей-дуги ». Подробный временной ход этого переключения в мозжечке человека был оценен с использованием экспрессионного микрочипа и секвенирования РНК и показан на рисунке справа.
Существует три гипотетические модели, описывающие этот механизм переключения:
Субъединицы GluN2B и GluN2A также играют различную роль в обеспечении эксайтотоксической гибели нейронов. [45] Считается, что изменение в составе субъединиц в процессе развития объясняет изменения нейротоксичности NMDA в процессе развития. [46] Гомозиготное нарушение гена GluN2B у мышей вызывает перинатальную летальность , тогда как нарушение гена GluN2A приводит к жизнеспособным мышам, хотя и с нарушенной пластичностью гиппокампа. [47] Одно исследование предполагает, что рилин может играть роль в созревании рецептора NMDA за счет увеличения подвижности субъединицы GluN2B. [48]
Предшественники гранулярных клеток (GCP) мозжечка после симметричного клеточного деления [49] во внешнем слое гранулярных клеток (EGL) мигрируют во внутренний слой гранулярных клеток (IGL), где они подавляют GluN2B и активируют GluN2C, процесс, который не зависит от передачи сигналов бета-нейрегулина через рецепторы ErbB2 и ErbB4. [50]
Ряд исследований показал, что NMDA-рецепторы тесно связаны с эксайтотоксичностью . [51] [52] [53] Поскольку NMDA-рецепторы играют важную роль в здоровье и функционировании нейронов , было много дискуссий о том, как эти рецепторы могут влиять как на выживаемость клеток, так и на их гибель. [54] Недавние данные подтверждают гипотезу о том, что чрезмерная стимуляция экстрасинаптических NMDA-рецепторов больше связана с эксайтотоксичностью, чем со стимуляцией их синаптических аналогов. [51] [22] Кроме того, хотя стимуляция экстрасинаптических рецепторов NMDA, по-видимому, способствует гибели клеток, есть данные, позволяющие предположить, что стимуляция синаптических рецепторов NMDA способствует здоровью и долговечности клетки. Существует множество доказательств в поддержку двойственной природы рецепторов NMDA в зависимости от местоположения, а гипотеза, объясняющая два разных механизма, известна как «гипотеза локализации». [51] [54]
Чтобы поддержать гипотезу локализации, было бы необходимо показать, что различные клеточные сигнальные пути активируются рецепторами NMDA в зависимости от их местоположения внутри клеточной мембраны. [51] Эксперименты были разработаны для стимуляции исключительно синаптических или несинаптических NMDA-рецепторов. Эксперименты такого типа показали, что в зависимости от места происхождения сигнала активируются или регулируются разные пути. [55] Многие из этих путей используют одни и те же белковые сигналы , но регулируются NMDAR по-разному в зависимости от их местоположения. Например, синаптическое возбуждение NMDA вызывало снижение внутриклеточной концентрации митоген-активируемой протеинкиназы р38 ( p38MAPK ). Внесинаптическая стимуляция NMDAR регулирует p38MAPK противоположным образом, вызывая увеличение внутриклеточной концентрации. [56] [57] С тех пор эксперименты этого типа были повторены, и результаты показали, что эти различия распространяются на многие пути, связанные с выживанием клеток и эксайтотоксичностью. [51]
Два специфических белка были идентифицированы как основной путь, ответственный за эти различные клеточные ответы: ERK1/2 и Jacob. [51] ERK1/2 отвечает за фосфорилирование Jacob при возбуждении синаптическими NMDAR. Эта информация затем переносится в ядро . Фосфорилирование Джейкоба не происходит при внесинаптической стимуляции NMDA. Это позволяет факторам транскрипции в ядре реагировать по-разному в зависимости от состояния фосфорилирования Джейкоба. [58]
Рецепторы NMDA (NMDAR) критически влияют на индукцию синаптической пластичности. NMDAR вызывают как долговременную потенциацию (LTP), так и долговременную депрессию (LTD) посредством быстрой синаптической передачи. [59] Экспериментальные данные показывают, что экстрасинаптические NMDA-рецепторы ингибируют LTP, одновременно производя LTD. [60] Ингибирование LTP можно предотвратить введением антагониста NMDA . [51] Стимуляция тета -всплеска , которая обычно вызывает LTP с помощью синаптических NMDAR, при избирательном применении к внесинаптическим NMDAR приводит к LTD. [61] Эксперименты также показывают, что экстрасинаптическая активность не требуется для формирования LTP. Кроме того, в экспрессии полной LTD участвует как синапсическая, так и внесинаптическая активность. [62]
Еще одним фактором, который, по-видимому, влияет на токсичность, вызванную NMDAR, является наблюдаемое изменение состава субъединиц . Рецепторы NMDA представляют собой гетеротетрамеры с двумя субъединицами GluN1 и двумя вариабельными субъединицами. [51] [63] Было показано, что две из этих вариабельных субъединиц, GluN2A и GluN2B, преимущественно приводят к каскадам выживания и гибели клеток соответственно. Хотя обе субъединицы обнаружены в синаптических и экстрасинаптических NMDAR, есть некоторые свидетельства того, что субъединица GluN2B чаще встречается во внесинаптических рецепторах. Это наблюдение может помочь объяснить двойственную роль, которую NMDA-рецепторы играют в эксайтотоксичности. [64] [65] t-NMDA-рецепторы участвуют в эксайтотоксичности, опосредованной гибели нейронов при височной эпилепсии . [66]
Несмотря на убедительные доказательства и относительную простоту этих двух теорий, работающих в тандеме, до сих пор существуют разногласия по поводу значимости этих утверждений. Некоторые проблемы в доказательстве этих теорий возникают из-за сложности использования фармакологических средств для определения подтипов конкретных NMDAR. [51] [67] Кроме того, теория вариации субъединиц не объясняет, почему этот эффект может преобладать, поскольку широко распространено мнение, что наиболее распространенный тетрамер, состоящий из двух субъединиц GluN1 и по одному из каждой субъединицы GluN2A и GluN2B, составляет высокий процент NMDAR. [51] Субъединичный состав t -NMDA-рецепторов недавно был обнаружен в тканях головного мозга. [68]
С конца 1950-х годов считалось, что эксайтотоксичность играет роль в дегенеративных свойствах нейродегенеративных состояний . [69] NMDA-рецепторы, по-видимому, играют важную роль во многих из этих дегенеративных заболеваний, поражающих мозг. В частности, эксайтотоксические явления, связанные с NMDA-рецепторами, связаны с болезнью Альцгеймера и болезнью Хантингтона, а также с другими заболеваниями, такими как инсульты и эпилепсия. [51] [70] Однако лечение этих состояний одним из многих известных антагонистов рецепторов NMDA приводит к множеству нежелательных побочных эффектов, некоторые из которых могут быть серьезными. Эти побочные эффекты частично наблюдаются потому, что рецепторы NMDA не только сигнализируют о гибели клеток, но и играют важную роль в их жизнеспособности. [54] Лечение этих состояний может быть найдено в блокировании рецепторов NMDA, не обнаруженных в синапсе. [51] [23] Один класс эксайтотоксичности при заболевании включает мутации усиления функции в GRIN2B и GRIN1, связанные с корковыми пороками развития, такими как полимикрогирия . [71] D-серин, антагонист/обратный коагонист t -NMDA-рецепторов, который вырабатывается в головном мозге, смягчает потерю нейронов на животной модели височной эпилепсии . [66]

Активация рецепторов NMDA требует связывания глутамата или аспартата (аспартат не так сильно стимулирует рецепторы). [72] Кроме того, NMDAR также требуют связывания коагониста глицина для эффективного открытия ионного канала, который является частью этого рецептора.
Также было обнаружено, что D -серин коагонизирует рецептор NMDA с еще большей эффективностью, чем глицин. [73] Он вырабатывается сериновой рацемазой и обогащен теми же участками, что и NMDA-рецепторы. Удаление D -серина может блокировать NMDA-опосредованную возбуждающую нейротрансмиссию во многих областях. Недавно было показано, что D -серин может высвобождаться как нейронами, так и астроцитами для регулирования NMDA-рецепторов. Обратите внимание, что D-серин также действует как антагонист/обратный коагонист t -NMDA-рецепторов. [74] [66]
Токи, опосредованные NMDA-рецептором (NMDAR), напрямую связаны с деполяризацией мембраны. Таким образом, агонисты NMDA демонстрируют быструю кинетику отсоединения Mg 2+ , увеличивая вероятность открытия каналов при деполяризации. Это свойство имеет фундаментальное значение для роли рецептора NMDA в памяти и обучении , и было высказано предположение, что этот канал является биохимическим субстратом Хеббианского обучения , где он может действовать как детектор совпадений для деполяризации мембраны и синаптической передачи.
Некоторые известные агонисты рецепторов NMDA включают:
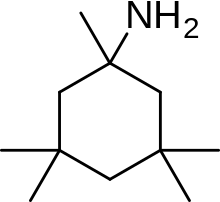
Примером производного мемантина является нерамексан , который был открыт путем изучения ряда аминоалкилциклогексанов с мемантином в качестве матрицы в качестве антагонистов рецептора NMDA. Нерамексан связывается с тем же сайтом, что и мемантин, в канале, связанном с рецептором NMDA, и с сопоставимым сродством. Он также демонстрирует очень схожую биодоступность и кинетику блокирования in vivo с мемантином. Нерамексан прошел клинические испытания по четырем показаниям, включая болезнь Альцгеймера. [26]

N -Метил- D -аспарагиновая кислота (NMDA), в честь которой был назван рецептор NMDA, является частичным агонистом активного сайта узнавания глутамата.
3,5-Дибром -L -фенилаланин, встречающееся в природе галогенированное производное L -фенилаланина , является слабым частичным агонистом рецептора NMDA, действующим на глициновом участке. [75] 3,5-Дибром- L -фенилаланин был предложен в качестве нового терапевтического препарата-кандидата для лечения нервно-психических расстройств и заболеваний, таких как шизофрения , [76] и неврологических расстройств, таких как ишемический инсульт и эпилептические припадки . [77]
Другие частичные агонисты рецептора NMDA, действующие на новые сайты, такие как рапастинел (GLYX-13) и апимостинел (NRX-1074), в настоящее время рассматриваются для разработки новых препаратов с антидепрессивным и анальгетическим действием без явной психотомиметической активности. [78]
К положительным аллостерическим модуляторам относятся:

Антагонисты рецептора NMDA используются в качестве анестетиков для животных, а иногда и для людей, и часто используются в качестве рекреационных наркотиков из-за их галлюциногенных свойств, а также их уникальных эффектов при повышенных дозах, таких как диссоциация . Когда определенные антагонисты рецепторов NMDA вводятся грызунам в больших дозах, они могут вызвать форму повреждения головного мозга , называемую поражениями Олни . Антагонисты рецепторов NMDA, которые, как было показано, вызывают поражения Олни, включают кетамин , фенциклидин и декстрорфан (метаболит декстрометорфана ), а также некоторые антагонисты рецепторов NMDA, используемые только в исследовательской среде. На данный момент опубликованные исследования поражений Олни не дали окончательных результатов в отношении их возникновения в тканях мозга человека или обезьяны в отношении увеличения присутствия антагонистов рецепторов NMDA. [80]
Большинство антагонистов NMDAR являются неконкурентными или неконкурентными блокаторами пор канала или являются антагонистами центра корегуляции глицина, а не антагонистами активного/глутаматного сайта.
Распространенные агенты, у которых антагонизм к рецептору NMDA является основным или основным механизмом действия:
Некоторые распространенные агенты, у которых слабый антагонизм к рецептору NMDA является вторичным или дополнительным действием, включают:
Рецептор NMDA регулируется посредством нитрозилирования , а аминоадамантан можно использовать в качестве целенаправленного челнока для доставки оксида азота (NO) близко к участку внутри рецептора NMDA, где он может нитрозилировать и регулировать проводимость ионного канала. [26] Донором NO, который можно использовать для снижения активности рецептора NMDA, является алкилнитрат нитроглицерин. В отличие от многих других доноров NO, алкилнитраты не обладают потенциальными нейротоксическими эффектами, связанными с NO. Алкилнитраты отдают NO в форме нитрогруппы, как показано на рисунке 7, -NO 2 -, который является безопасным донором, позволяющим избежать нейротоксичности. Нитрогруппа должна быть направлена на рецептор NMDA, в противном случае могут возникнуть другие эффекты NO, такие как расширение кровеносных сосудов и последующая гипотония . [96] Нитромемантин является производным мемантина второго поколения. Он снижает эксайтотоксичность, опосредованную сверхактивацией глутаматергической системы, блокируя рецептор NMDA, не жертвуя при этом безопасностью. Предварительные исследования на животных моделях показывают, что нитромантины более эффективны, чем мемантин, в качестве нейропротекторов как in vitro , так и in vivo. Мемантин и новые его производные могут стать очень важным оружием в борьбе с повреждением нейронов. [16]

К отрицательным аллостерическим модуляторам относятся:
Рецептор NMDA модулируется рядом эндогенных и экзогенных соединений: [98]
Основная проблема при разработке антагонистов NMDA для нейропротекции заключается в том, что физиологическая активность рецепторов NMDA необходима для нормальной функции нейронов. Полная блокада активности всех рецепторов NMDA приводит к таким побочным эффектам, как галлюцинации , возбуждение и анестезия . Чтобы быть клинически значимым, антагонист рецептора NMDA должен ограничивать свое действие блокадой чрезмерной активации, не ограничивая нормальную функцию рецептора. [19]
Конкурентные антагонисты рецептора NMDA, которые были разработаны первыми, не являются хорошим вариантом, поскольку они конкурируют и связываются с тем же сайтом (субъединицей NR2) на рецепторе, что и агонист, глутамат, и, следовательно, также блокируют нормальную функцию. [19] [111] Они будут блокировать здоровые области мозга, прежде чем оказать воздействие на патологические области, поскольку здоровые области содержат более низкие уровни агониста, чем патологические области. Эти антагонисты могут быть вытеснены из рецептора высокой концентрацией глутамата, который может существовать в условиях эксайтотоксичности. [14]

Неконкурентные антагонисты NMDA-рецепторов блокируют ионный канал в месте Mg 2+ (область пор) и предотвращают чрезмерный приток Ca 2+ . Неконкурентный антагонизм относится к типу блокады, которую не может преодолеть повышенная концентрация глутамата, и зависит от предварительной активации рецептора агонистом, т.е. он входит в канал только тогда, когда он открывается агонистом. [19] [112]
Из-за этих неблагоприятных побочных эффектов блокаторов с высоким сродством поиск клинически успешных антагонистов рецепторов NMDA для лечения нейродегенеративных заболеваний продолжился и был сосредоточен на разработке блокаторов с низким сродством. Однако сродство не может быть слишком низким, а время пребывания не может быть слишком коротким (как видно для Mg 2+ ), когда деполяризация мембраны снимает блокировку. Таким образом, открытием стало создание неконкурентного антагониста с более длительным временем пребывания, чем у Mg 2+ в канале, но более коротким, чем у МК-801. Таким образом, полученное лекарство будет блокировать только чрезмерно открытые каналы, связанные с рецептором NMDA, но не нормальную нейротрансмиссию. [19] [112] Мемантин и есть этот препарат. Это производное амантадина, который сначала был противогриппозным средством, но позже по совпадению обнаружил, что он эффективен при болезни Паркинсона. Химическую структуру мемантина и амантадина можно увидеть на рисунке 5. Сначала считалось, что это соединение является дофаминергическим или антихолинергическим , но позже было обнаружено, что оно является антагонистом рецептора NMDA. [13] [19]
Мемантин — первый препарат, одобренный для лечения тяжелой и более запущенной болезни Альцгеймера , для которой, например, антихолинергические препараты не приносят особой пользы. [112] Он помогает восстановить синаптические функции и тем самым улучшает нарушенную память и способность к обучению. [17] В 2015 году мемантин также проходит испытания на предмет его терапевтического значения при других неврологических расстройствах. [96]
Многие производные мемантина второго поколения находятся в стадии разработки, которые могут показать еще лучшие нейропротекторные эффекты, при этом основная идея заключается в использовании других безопасных, но эффективных модулирующих участков на рецепторе NMDA в дополнение к связанному с ним ионному каналу. [96]
Мемантин (1-амино-3,5-диметиладамантан) представляет собой производное аминоалкилциклогексана и атипичное лекарственное соединение с неплоской трехмерной трициклической структурой. На рисунке 8 показан SAR для производного аминоалкилциклогексана. Мемантин имеет несколько важных особенностей в своей структуре, обеспечивающих его эффективность:
Несмотря на небольшую структурную разницу между мемантином и амантадином, двумя производными адамантана, сродство к сайту связывания субъединицы NR1/NR2B у мемантина намного выше. При измерениях с помощью патч-клампа мемантин имеет IC 50 (2,3+0,3) мкМ, тогда как амантадин имеет IC 50 (71,0+11,1) мкМ. [26] Сайт связывания с самым высоким сродством называется доминантным сайтом связывания. Он включает соединение между аминогруппой мемантина и связывающим карманом NR1-N161 субъединицы NR1/NR2B. Боковые метильные группы играют важную роль в увеличении сродства к открытым каналам рецептора NMDA и делают его гораздо лучшим нейропротекторным препаратом, чем амантадин. Считается, что карманы связывания метильных групп находятся в NR1-A645 и NR2B-A644 NR1/NR2B. [30] Карманы связывания показаны на рисунке 2. Мемантин связывается на сайте Mg 2+ или рядом с ним внутри канала, связанного с рецептором NMDA. Группа -NH 2 мемантина, которая протонируется при физиологическом pH организма, представляет собой область, которая связывается с сайтом Mg 2+ или рядом с ним . [16] Добавление двух метильных групп к -N в структуре мемантина показало снижение сродства, что дает значение IC 50 (28,4+1,4) мкМ. [26]
Несколько производных нитромемантина, производного мемантина второго поколения, были синтезированы для того, чтобы определить детальную взаимосвязь структура-активность (SAR) этих новых препаратов. Один класс, содержащий нитрогруппу (NO 2 ), противоположную амину-мостику-мостику (NH 2 ), показал многообещающий результат. Нитромемантин использует сайт связывания мемантина на рецепторе NMDA для нацеливания на группу NO x (X = 1 или 2) для взаимодействия с сайтом S-нитрозилирования/окислительно-восстановительного процесса, внешним по отношению к сайту связывания мемантина. Удлинение боковых цепей мемантина компенсирует худшее сродство препарата в канале, связанное с добавлением группы –ONO 2 [113].
Предполагается, что эксайтотоксичность связана с некоторыми нейродегенеративными заболеваниями, такими как болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона и боковой амиотрофический склероз . [14] [15] [16] [17] Таким образом, блокирование рецепторов NMDA теоретически может быть полезно при лечении таких заболеваний. [14] [15] [16] Однако важно сохранить физиологическую активность рецептора NMDA, одновременно пытаясь блокировать его чрезмерную эксайтотоксическую активность. Возможно, этого можно достичь с помощью неконкурентных антагонистов, блокирующих ионный канал рецептора при чрезмерном открытии [16].
Мемантин является примером неконкурентного антагониста рецептора NMDA, который одобрен для лечения нейродегенеративного заболевания — болезни Альцгеймера. В 2015 году мемантин все еще находится на стадии клинических испытаний при лечении других неврологических заболеваний. [30] [96]
Рецептор NMDA представляет собой неспецифический катионный канал, который может обеспечивать прохождение Ca 2+ и Na + в клетку и K + из клетки. Возбуждающий постсинаптический потенциал (ВПСП), возникающий при активации рецептора NMDA, увеличивает концентрацию Са 2+ в клетке. Ca 2+, в свою очередь, может выступать в качестве вторичного мессенджера в различных сигнальных путях . Однако катионный канал NMDA-рецептора блокируется Mg 2+ при мембранном потенциале покоя. [114] Разблокировка магния не происходит мгновенно; чтобы разблокировать все доступные каналы, постсинаптическая клетка должна быть деполяризована на достаточно длительный период времени (в масштабах миллисекунд). [115]
Таким образом, рецептор NMDA функционирует как « детектор молекулярных совпадений ». Его ионный канал открывается только при выполнении следующих двух условий: глутамат связывается с рецептором и постсинаптическая клетка деполяризуется (что удаляет блокирующий канал Mg 2+ ). Это свойство рецептора NMDA объясняет многие аспекты долговременной потенциации (ДП) и синаптической пластичности . [116]
В состоянии покоя мембраны поры рецептора NMDA открываются, обеспечивая приток внешних ионов магния, связывающихся для предотвращения дальнейшего проникновения ионов. [117] Внешние ионы магния находятся в миллимолярном диапазоне, тогда как внутриклеточные ионы магния находятся в микромолярном диапазоне, что приводит к отрицательному мембранному потенциалу. NMDA-рецепторы модулируются рядом эндогенных и экзогенных соединений и играют ключевую роль в широком спектре физиологических (например, память ) и патологических процессов (например, эксайтотоксичность ). Магний усиливает NMDA-индуцированные реакции при положительных мембранных потенциалах, блокируя при этом канал NMDA. Использование кальция, калия и натрия используется для модуляции активности NMDAR, проходящих через мембрану NMDA. Изменения концентрации H + могут частично ингибировать активность NMDA-рецепторов в различных физиологических условиях.
Антагонисты NMDAR, такие как кетамин , эскетамин , тилетамин , фенциклидин , закись азота и ксенон , используются в качестве общих анестетиков . Эти и подобные наркотики, такие как декстрометорфан и метоксетамин, также производят диссоциативные , галлюциногенные и эйфорические эффекты и используются в качестве рекреационных наркотиков .
Соединения, нацеленные на NMDAR, включая кетамин, эскетамин (JNJ-54135419), рапастинель (GLYX-13), апимостинел (NRX-1074), зелквистинел (AGN-241751), 4-хлоркинуренин (AV-101) и рисленемдаз (CERC- 301, МК-0657), находятся в стадии разработки для лечения расстройств настроения , включая большое депрессивное расстройство и резистентную к лечению депрессию . [81] [82] [118] Кроме того, кетамин уже используется для этой цели в качестве терапии не по назначению в некоторых клиниках. [119] [120]
Исследования показывают, что тианептин оказывает антидепрессивное действие за счет непрямого изменения и ингибирования активности рецепторов глутамата и высвобождения BDNF., что, в свою очередь, влияет на нейронную пластичность . [121] [122] [123] [124] [125] Тианептин также действует на рецепторы NMDA и AMPA . [121] [125] На животных моделях тианептин ингибирует вызванные стрессом патологические изменения глутаматергической нейротрансмиссии в миндалевидном теле и гиппокампе.
Мемантин , антагонист NMDAR с низким уровнем улавливания, одобрен в США и Европе для лечения болезни Альцгеймера от умеренной до тяжелой степени [126] и в настоящее время получил ограниченную рекомендацию Национального института здравоохранения и передового опыта Великобритании . пациенты, у которых другие варианты лечения оказались неэффективными. [127]
Кохлеарные NMDAR являются объектом интенсивных исследований с целью поиска фармакологических решений для лечения шума в ушах . NMDAR связаны с редким аутоиммунным заболеванием, анти-NMDA-рецепторным энцефалитом (также известным как NMDAR-энцефалит [128] ), который обычно возникает из-за перекрестной реактивности антител, продуцируемых иммунной системой против эктопических тканей головного мозга, например, обнаруженных у тератома . Они известны как антитела к рецепторам глутамата .
По сравнению с дофаминергическими стимуляторами, такими как метамфетамин , антагонист NMDAR фенциклидин может вызывать более широкий спектр симптомов, напоминающих шизофрению, у здоровых добровольцев, что привело к глутаматной гипотезе шизофрении . [129] Эксперименты, в которых грызунов лечат антагонистом рецептора NMDA, сегодня являются наиболее распространенной моделью, когда дело доходит до тестирования новых методов лечения шизофрении или изучения точного механизма действия лекарств, уже одобренных для лечения шизофрении.
Антагонисты NMDAR, например элипродил , гавестинел , ликостинел и селфотел , широко исследовались для лечения нейротоксичности , опосредованной эксайтотоксичностью , в таких ситуациях, как ишемический инсульт и черепно-мозговая травма , но в клинических испытаниях, применявшихся в малых дозах во избежание седативного эффекта, они оказались безуспешными. Антагонисты NMDAR могут блокировать распространяющуюся деполяризацию у животных и пациентов с травмой головного мозга. [130] Это использование еще не было проверено в клинических испытаниях.
Поскольку считается, что для активации канала необходимы по две молекулы глутамата и глицина (3, 6), это означает, что рецептор NMDA должен состоять как минимум из четырех субъединиц.